Clear Sky Science · it
Sbloccare le vulnerabilità del glioma: mirare alle vie di morte cellulare regolate per terapie innovative
Perché la morte delle cellule tumorali cerebrali conta
I gliomi sono tra i tumori cerebrali più comuni e letali negli adulti. Anche con chirurgia, radioterapia e chemioterapia, spesso recidivano e sono difficili da controllare. Questo articolo di revisione esplora un nuovo punto di attacco: sfruttare i diversi modi in cui le cellule possono essere programmate per morire. Comprendendo e indirizzando queste vie di “autodistruzione”, i ricercatori sperano di mettere in luce le debolezze delle cellule di glioma e rendere i trattamenti futuri più efficaci e personalizzati.
Come i gliomi eludono i trattamenti standard
I gliomi originano dalle cellule di supporto del cervello e vanno da forme a crescita lenta a varianti altamente aggressive come il glioblastoma. I loro scarsi risultati terapeutici derivano da diversi problemi intrecciati: mutazioni genetiche, cambiamenti epigenetici, cellule staminali difficili da eliminare, un apporto ematico anomalo e un microambiente immunitario fortemente soppressivo. Inoltre, la barriera emato-encefalica limita la capacità dei farmaci di raggiungere il tumore. Nel loro insieme, questi fattori permettono alle cellule tumorali di sopravvivere a interventi chirurgici e terapie standard, adattarsi allo stress e infine ricrescere. 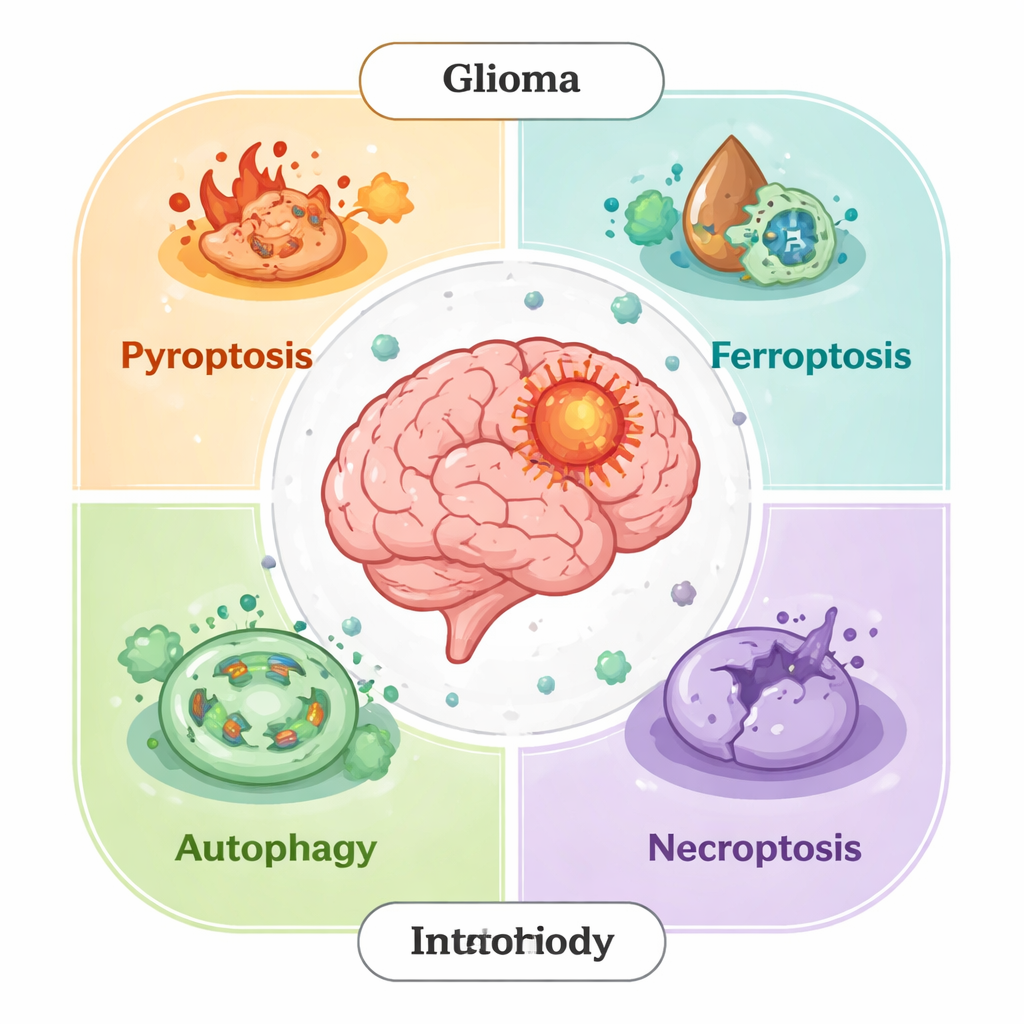
Le molte facce dell’autodistruzione cellulare
Trasformare le vie di morte in terapie
Invece di considerare queste vie di morte come un problema, i ricercatori stanno imparando a trasformarle in armi. Le strategie che inducono la piroptosi utilizzano nanoparticelle intelligenti, riscaldamento basato sulla luce, virus ingegnerizzati o idrogel caricati di farmaci per far gonfiare, esplodere e rilasciare segnali di pericolo dalle cellule di glioma, allertando così il sistema immunitario. Gli approcci basati sulla ferroptosi spingono le cellule tumorali verso il collasso alimentato dal ferro bloccando enzimi protettivi chiave come GPX4, disturbando la produzione di glutatione o alterando il metabolismo dei lipidi nelle cellule tumorali. Molte di queste tattiche vengono veicolate con vettori avanzati, inclusi graphdiyne e altre nanoparticelle, per aiutare i farmaci a superare la barriera emato-encefalica e concentrarsi all’interno del tumore risparmiando il tessuto cerebrale sano. 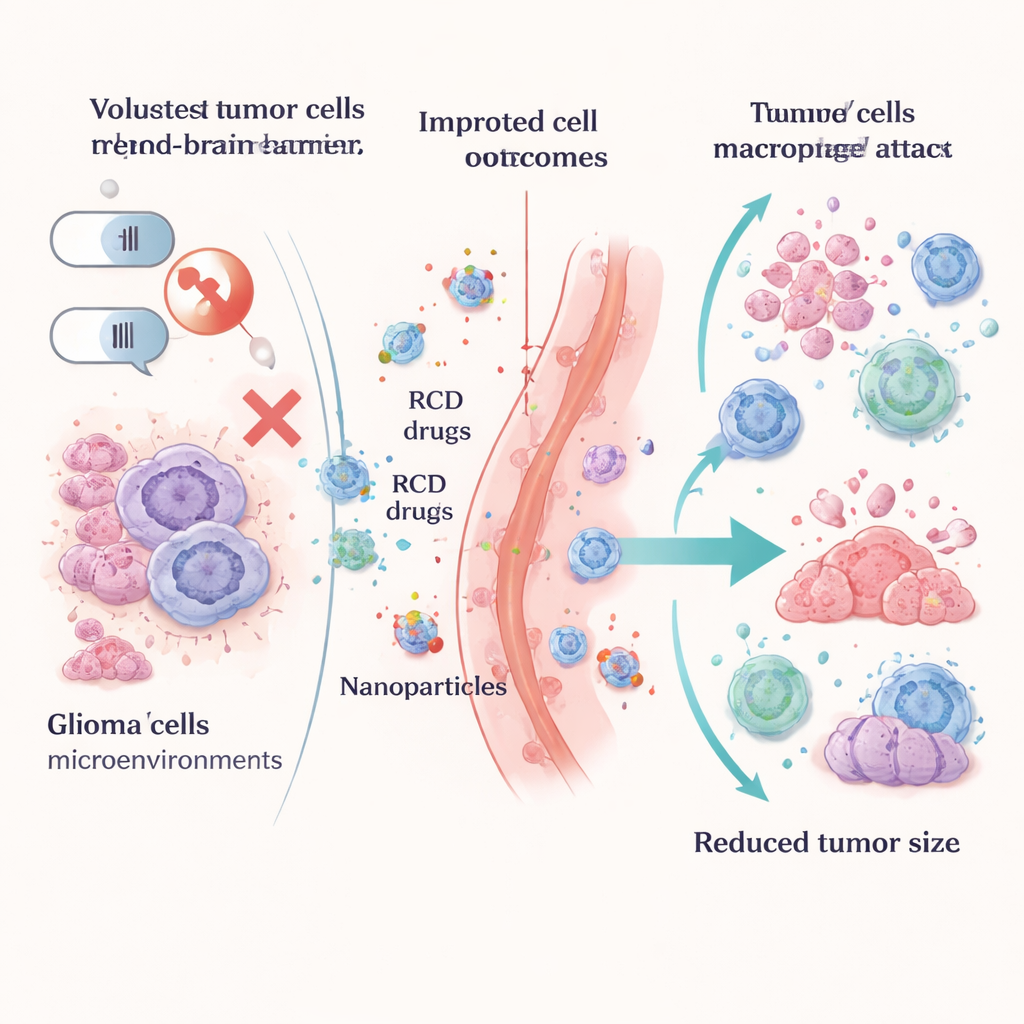
Riavviare il panorama immunitario del tumore
Le terapie incentrate sulla necroptosi mirano a superare la resistenza nelle cellule che non rispondono più ai segnali di morte standard. Prodotti naturali come shikonin, emodina e derivati della celastrol possono spingere le cellule di glioma verso la necroptosi, che non solo le uccide ma rilascia anche molecole che richiamano cellule immunitarie nel tumore. Allo stesso tempo, gli scienziati stanno esplorando l’autofagia, talvolta bloccandola per impedire che le cellule tumorali usino la “pulizia” per sopravvivere a radiazioni e chemioterapia, e talaltra spingendola oltre i limiti per scatenare la morte cellulare. I primi trial clinici con farmaci come la clorochina e l’idrossiclorochina mostrano che l’autofagia può essere modulata in sicurezza nei pazienti, sebbene benefici di sopravvivenza chiari non siano ancora stati dimostrati.
Dalle scoperte di laboratorio alla cura personalizzata
Traslare questi concetti in trattamenti reali rimane una sfida. I gliomi sono altamente variabili da paziente a paziente, e anche all’interno dello stesso tumore, quindi nessuna singola strategia basata su una via di morte si adatterà a tutti. La barriera emato-encefalica ostacola ancora la distribuzione dei farmaci e il microambiente immunitario può attenuare anche combinazioni terapeutiche sofisticate. Gli autori evidenziano direzioni promettenti: associare induttori di ferroptosi con inibitori dei checkpoint immunitari, combinare virus oncolitici con farmaci che potenziano i segnali “mangiami” delle cellule tumorali, o aggiungere modulatori dell’autofagia a regimi selezionati di chemo-radioterapia. Profilaggi multi-omici e biomarcatori migliori dovrebbero aiutare a identificare quali pazienti hanno maggiori probabilità di beneficiare di una specifica combinazione di strategie.
Guardando avanti: far scegliere ai tumori l’autodistruzione
In termini semplici, questo articolo conclude che il futuro del trattamento dei gliomi potrebbe consistere nel costringere le cellule tumorali ad attivare i propri pulsanti di autodistruzione in modi accuratamente controllati. Imparando a innescare e coordinare piroptosi, ferroptosi, necroptosi e morte dipendente dall’autofagia—e associando queste strategie a immunoterapie moderne e a sistemi di somministrazione di farmaci di precisione—i ricercatori sperano di trasformare una diagnosi oggi grave in una condizione più gestibile e, in ultima analisi, più curabile.
Citazione: Guo, J., Zong, L., Huang, Y. et al. Unlocking glioma vulnerabilities: targeting regulated cell death pathways for innovative therapies. Cell Death Discov. 12, 95 (2026). https://doi.org/10.1038/s41420-026-02949-8
Parole chiave: glioma, morte cellulare regolata, piropotosi, ferroptosi, terapia del glioblastoma