Clear Sky Science · it
Mitofagia nel cancro pancreatico: approfondimenti meccanistici e implicazioni per nuove strategie terapeutiche
Perché le centrali energetiche delle nostre cellule contano nel cancro pancreatico
L'adenocarcinoma duttale del pancreas è uno dei tumori più letali, in parte perché le neoplasie imparano rapidamente a resistere quasi a ogni trattamento che i medici tentano. Questo articolo di sintesi esplora un protagonista sorprendente nella storia di questa resistenza: la mitofagia, il sistema intrinseco della cellula per individuare e riciclare i mitocondri usurati, le minuscole “centrali” che producono energia. Capire come il cancro pancreatico sfrutti questo processo di pulizia potrebbe aprire nuove strade verso terapie più efficaci e durature.
Le squadre di pulizia cellulare e gli stratagemmi di sopravvivenza del cancro
I mitocondri fanno molto più che generare energia; partecipano al controllo del metabolismo, alla regolazione della morte cellulare e alla gestione delle molecole dannose chiamate specie reattive dell'ossigeno. Quando i mitocondri sono danneggiati o troppo numerosi, le cellule si affidano alla mitofagia per segnalarli e rimuoverli. Questo può avvenire attraverso due vie principali. Una, nota come via PINK1/Parkin, si basa su un sensore di danno (PINK1) e un enzima di marcatura (Parkin) per etichettare i mitocondri difettosi per la distruzione. L'altra utilizza proteine recettori come BNIP3, NIX e FUNDC1 presenti sulla superficie mitocondriale per collegarli direttamente agli organelli di smaltimento cellulare, gli autofagosomi, senza lo stesso passaggio di marcatura. Queste vie spesso collaborano, offrendo alle cellule modi flessibili di adattare il loro patrimonio mitocondriale a stress come la carenza di ossigeno o l'esposizione a farmaci. 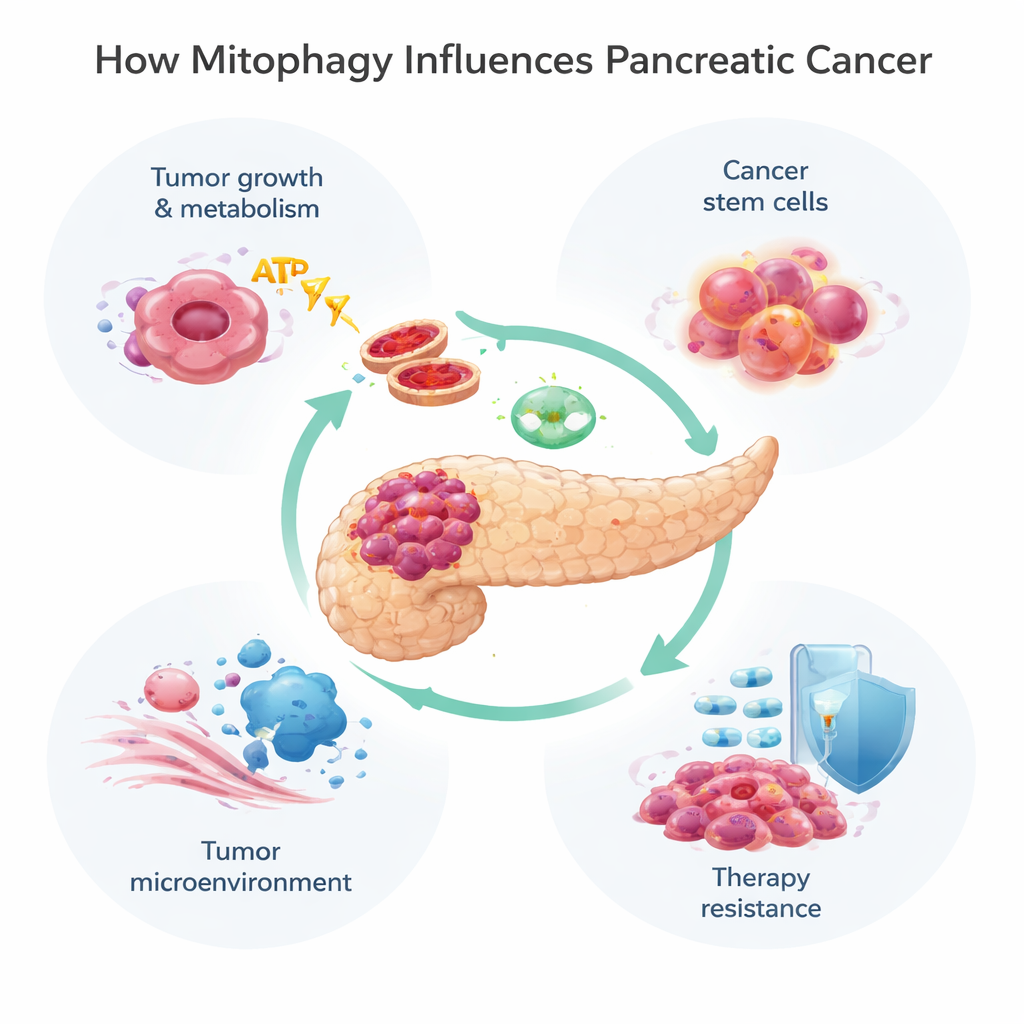
Come i tumori pancreatici rimodellano il loro uso energetico
I tumori pancreatici vivono in un contesto ostile: sono poveramente irrorati da sangue e ossigeno e circondati da tessuto denso simile a cicatrice. Per sopravvivere, le cellule tumorali riorganizzano i loro sistemi energetici, spesso spostandosi dalla respirazione mitocondriale dipendente dall'ossigeno verso un processo più primitivo di combustione degli zuccheri noto come glicolisi. La mitofagia aiuta a perfezionare questo spostamento. Nelle fasi iniziali dello sviluppo tumorale, la perdita di PINK1 o Parkin accelera la formazione del cancro permettendo l'accumulo di ferro, l'aumento delle specie reattive dell'ossigeno e una spinta verso la glicolisi. Allo stesso tempo, un'altra proteina di mitofagia, NIX, può contribuire a rimuovere mitocondri ancora funzionanti, spingendo le cellule ulteriormente verso il metabolismo glicolitico e una crescita più rapida. Per contro, BNIP3 mostra un pattern più complesso: compare precocemente, viene poi silenziato in molti tumori avanzati e, quando viene ristabilito, può rallentare la crescita delle cellule tumorali, suggerendo che alcune vie di mitofagia frenano il cancro mentre altre lo alimentano.
Cellule staminali tumorali e il microambiente del tumore
Non tutte le cellule tumorali sono uguali. Una piccola sottopopolazione, spesso chiamata cellule staminali cancerose, può auto-rinnovarsi, dare origine a nuovi tumori e resistere particolarmente bene alla chemioterapia. Nel cancro pancreatico, queste cellule dipendono dalla mitofagia per mantenere la flessibilità metabolica. Una proteina modificatrice chiamata ISG15 supporta questo processo e aiuta a conservare le caratteristiche di tipo staminale, collegando la mitofagia direttamente a recidiva e fallimento terapeutico. Oltre alle stesse cellule tumorali, la mitofagia plasma anche il microambiente tumorale — il mix di cellule di supporto, cellule immunitarie e tessuto connettivo intorno al tumore. I fibroblasti associati al cancro, per esempio, possono essere indotti a entrare in un “effetto Warburg inverso”, in cui aumentano la propria mitofagia e glicolisi e poi forniscono al tumore sottoprodotti ricchi di energia. La mitofagia influenza anche il modo in cui le cellule immunitarie riconoscono e attaccano il cancro, alterando l'esposizione di segnali immunitari come MHC‑I e i freni come PD‑L1 che i tumori usano per nascondersi.
Perché bloccare o potenziare la pulizia può modificare la risposta ai farmaci
Molti trattamenti standard ed emergenti per il cancro pancreatico, incluso il chemioterapico gemcitabina e un nuovo farmaco mirato contro la comune mutazione KRAS‑G12D, danneggiano i mitocondri. Le cellule tumorali spesso rispondono attivando la mitofagia, eliminando il danno ed evitando la morte. Studi mostrano che la mitofagia guidata da PINK1 può attenuare gli effetti citotossici della chemioterapia e di alcuni composti naturali, aiutando le cellule tumorali a sopravvivere. D'altra parte, in certe condizioni, spingere la mitofagia oltre una soglia — in particolare attraverso BNIP3 e NIX — può privare le cellule di troppi mitocondri funzionanti, precipitando una crisi energetica e promuovendo la morte cellulare. Questa natura duplice implica che la mitofagia può o proteggere i tumori dal trattamento o, se stimolata nel modo giusto, renderli più vulnerabili. 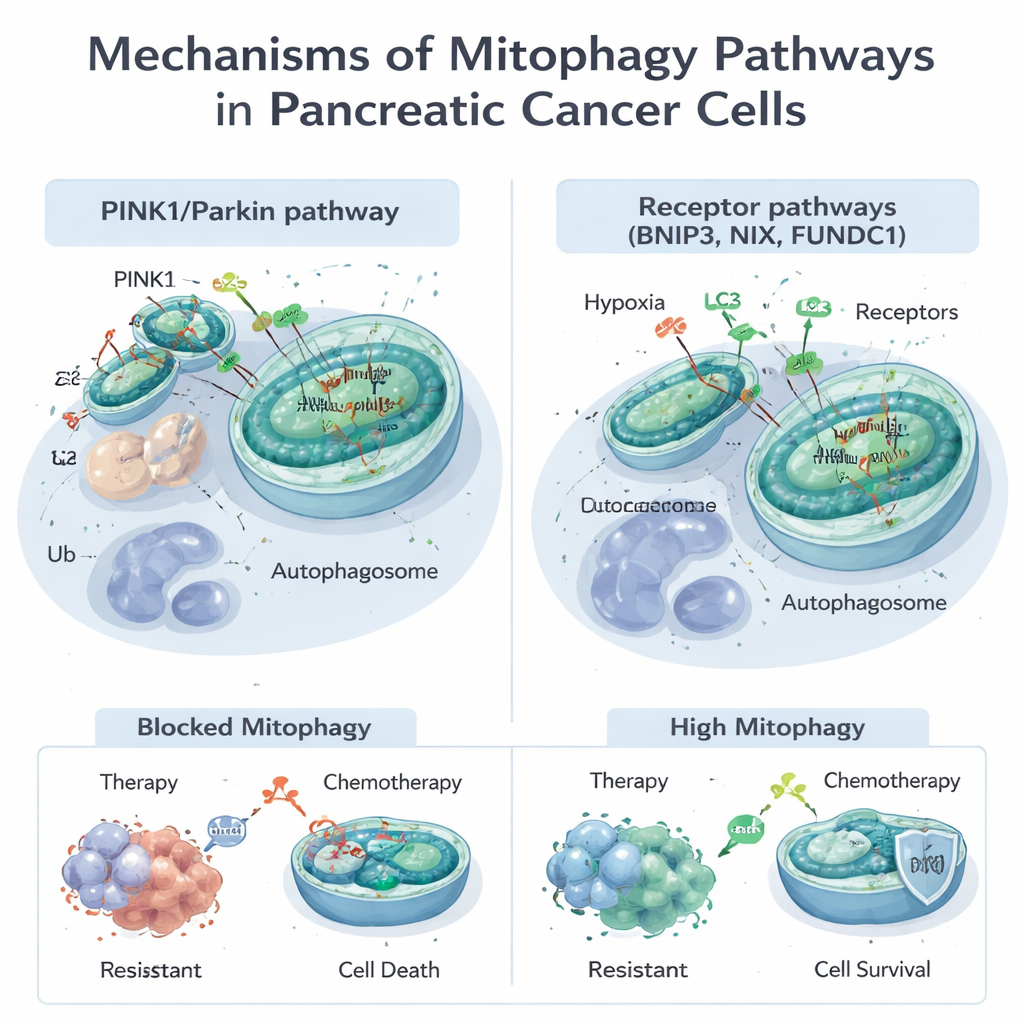
Nuove idee terapeutiche e la necessità di abbinare i pazienti con intelligenza
Poiché la mitofagia si trova all'incrocio tra metabolismo, risposte allo stress e morte cellulare, rappresenta un bersaglio attraente per terapie combinate. Le strategie farmacologiche attuali agiscono per lo più in modo indiretto: alcuni composti interferiscono con la fissione e la fusione mitocondriale; altri, come clorochina e idrossiclorochina, bloccano le fasi finali del processo di riciclaggio disabilitando la fusione degli organelli di scarto con i compartimenti acidi di degradazione. Diversi trial clinici stanno testando questi farmaci in combinazione con la chemioterapia standard nel cancro pancreatico. Tuttavia i risultati finora sono contrastanti — alcuni pazienti traggono beneficio, altri no. Parte del problema è che i tumori variano ampiamente nei loro profili metabolici e nei livelli baseline di mitofagia: alcuni dipendono fortemente dalla respirazione mitocondriale, altri dalla glicolisi. Gli autori sostengono che il successo futuro dipenderà da migliori biomarcatori e firme genetiche per raggruppare i pazienti in base all'attività di mitofagia e all'uso energetico, e dallo sviluppo di farmaci più precisi che modulino selettivamente specifiche vie di mitofagia invece di accendere o spegnere bruscamente l'autofagia. Per i lettori non specialisti, la conclusione chiave è che imparare a leggere e modulare con cura questo sistema di pulizia mitocondriale potrebbe aiutare a trasformare il cancro pancreatico da un avversario ostinato in una malattia più gestibile.
Citazione: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Parole chiave: cancro pancreatico, mitofagia, mitocondri, resistenza alla chemioterapia, metabolismo tumorale