Clear Sky Science · it
La osteopontina derivata dal cancro colorettale riconfigura i macrofagi in uno stato M2 pro-metastatico attraverso l’asse PI3K/AKT/CSF1-CSF1R
Perché questo interessa le persone con cancro al colon
La maggior parte dei decessi per cancro colorettale (colon e retto) non è causata dal tumore primario, ma dalla sua diffusione in altri organi. Questo studio esamina come le cellule tumorali "comunichino" con le cellule immunitarie vicine per favorire la diffusione. Scoprendo un messaggio chiave che le cellule tumorali inviano per riprogrammare le cellule immunitarie da nemiche ad alleate, il lavoro indica nuove strategie terapeutiche che potrebbero rallentare o fermare le metastasi nel cancro colorettale avanzato.
Una proteina appiccicosa con un lato oscuro
I ricercatori si sono concentrati su una proteina chiamata osteopontina, o OPN, prodotta sia dalle cellule tumorali sia da alcune cellule immunitarie all’interno dei tumori. L’OPN è da tempo associata a esiti peggiori in molti tumori, ma il modo in cui promuove la diffusione nel cancro colorettale era poco chiaro. Analizzando ampi database di pazienti e campioni tumorali, il team ha scoperto che i livelli di OPN erano molto più alti nei tessuti del cancro colorettale rispetto al tessuto colico normale, soprattutto nei pazienti con malattia avanzata e metastasi a distanza. I pazienti i cui tumori presentavano più OPN avevano in genere una sopravvivenza peggiore, suggerendo che l’OPN è strettamente legata a tumori aggressivi e difficili da trattare.
Non sono solo le cellule tumorali
Sorprendentemente, quando gli scienziati costrinsero le cellule di cancro colorettale in laboratorio a produrre più o meno OPN, le cellule non divennero più invasive o mobili da sole. Crescita, migrazione e capacità di invadere attraverso membrane artificiali cambiarono pochissimo. Ciò mette in discussione l’idea comune che l’OPN agisca principalmente potenziando direttamente la forza intrinseca delle cellule tumorali. Il team rivolse quindi l’attenzione al quartiere del tumore—il cosiddetto microambiente tumorale—e in particolare a un gruppo di cellule immunitarie chiamate macrofagi, che possono attaccare i tumori (stato “M1”) o supportarli (stato “M2”).
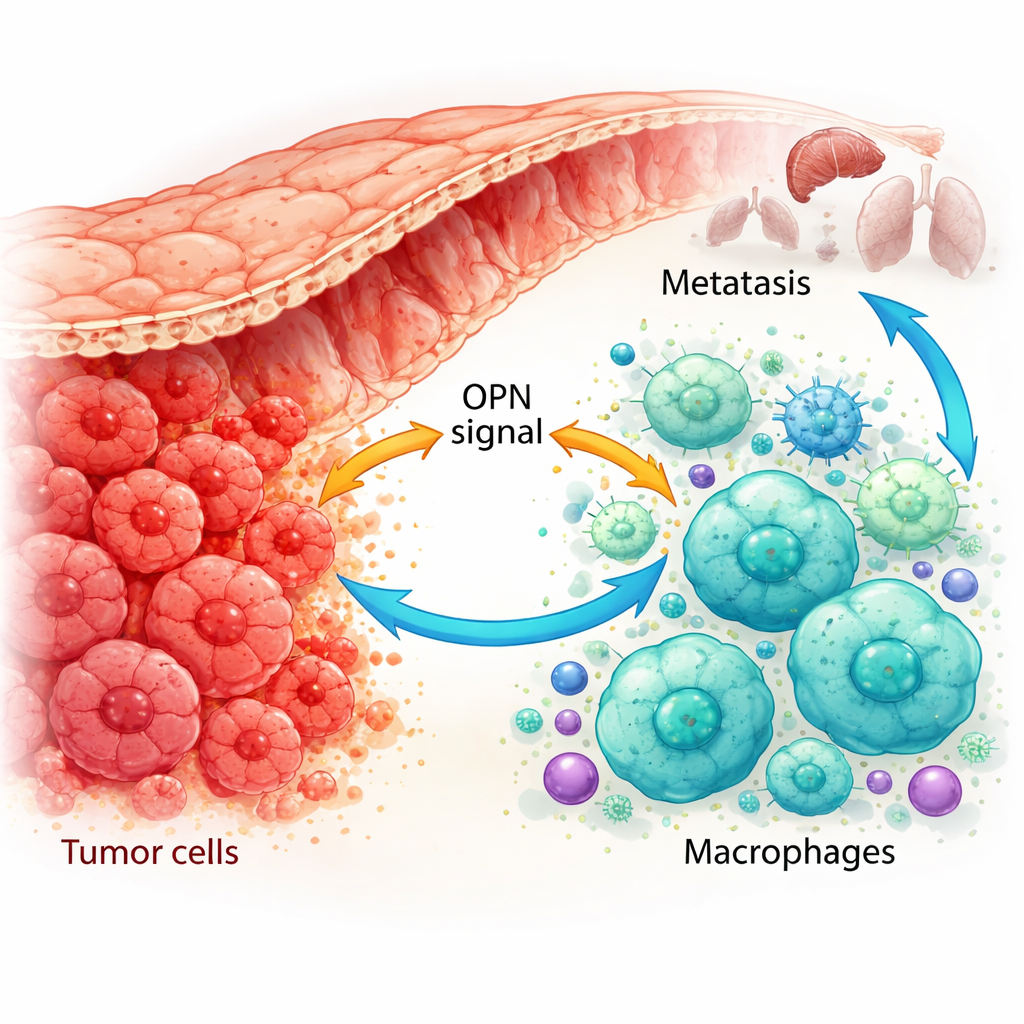
Come le cellule immunitarie vengono riprogrammate in aiutanti del tumore
Usando mappe genetiche a singola cellula e colorazioni avanzate dei tessuti dei pazienti, i ricercatori hanno mostrato che l’OPN è prodotta non solo dalle cellule tumorali ma anche dai macrofagi associati al tumore. Nei tumori che avevano già metastatizzato, sia le cellule tumorali sia un sottotipo specifico di macrofagi erano ricchi di OPN. Questi macrofagi tendevano a trovarsi in uno stato simile a M2, di supporto al tumore, e risultavano più abbondanti quando i livelli tumorali di OPN erano elevati. In modelli murini, tumori ingegnerizzati per produrre più OPN attirarono un numero maggiore di questi macrofagi M2-like e crebbero più velocemente, mentre tumori con OPN ridotta presentavano meno macrofagi M2 e crescita più lenta. Ciò suggerisce che l’OPN è un potente reclutatore e riprogrammatore di macrofagi nel microambiente tumorale.
La catena di segnalazione nascosta: dall’OPN alle metastasi
Per chiarire la catena molecolare degli eventi, il team coltivò macrofagi umani insieme a cellule di cancro colorettale che producevano quantità diverse di OPN. Scoprirono che le cellule tumorali ad alto contenuto di OPN spingevano i macrofagi verso lo stato M2 e favorivano un movimento bidirezionale: i macrofagi migravano verso il tumore e le cellule tumorali divenivano più invasive in risposta ai segnali provenienti da questi macrofagi. Approfondendo, gli scienziati identificarono che l’OPN attiva nei macrofagi una via di segnalazione chiamata PI3K/AKT. Tale attivazione, a sua volta, induce i macrofagi a rilasciare grandi quantità di un’altra molecola, CSF1, e ad aumentare il recettore per quella molecola, CSF1R, sulla loro superficie. CSF1 agisce poi in un circuito che rinforza ulteriormente lo stato M2 pro-metastatico e continua ad attrarre macrofagi nel tumore.
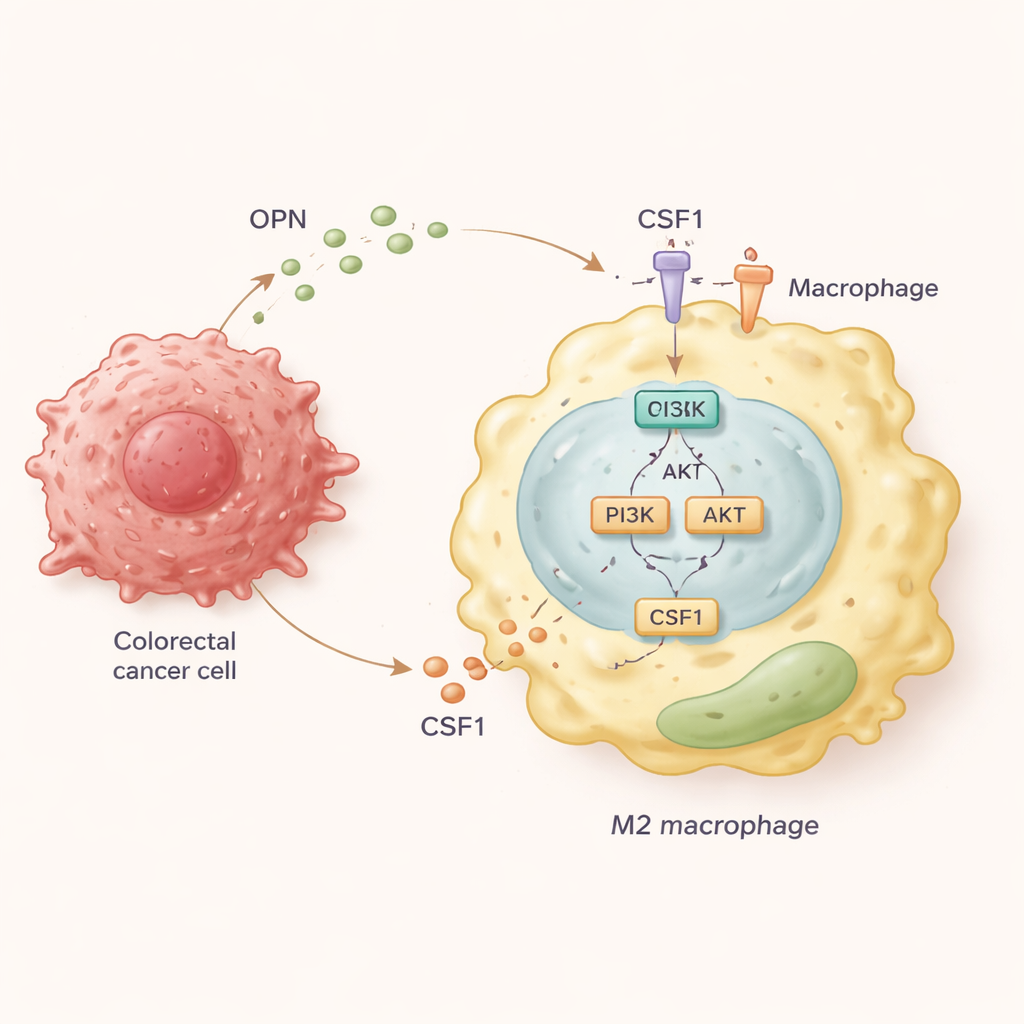
Interrompere il circuito per rallentare la diffusione
In modelli murini di cancro colorettale con diffusione addominale, i ricercatori testarono un farmaco che blocca CSF1R chiamato PLX3397. I topi con tumori ad alto contenuto di OPN svilupparono numerosi noduli metastatici, ma il trattamento con l’inibitore di CSF1R ridusse in modo significativo sia il numero di metastasi sia la presenza di macrofagi di tipo M2 nei tumori. Le cellule tumorali mostrarono minore proliferazione e maggiori segnali di morte cellulare programmata. È importante che il farmaco abbia principalmente depletato i macrofagi promotori del tumore senza influenzare in modo significativo il tipo più infiammatorio, suggerendo un modo relativamente mirato per indebolire il sistema di supporto del tumore.
Cosa significa per i trattamenti futuri
Per un lettore non esperto, il messaggio principale è che alcuni tumori colorettali riescono a diffondersi non solo perché le cellule tumorali sono aggressive, ma perché dirottano le cellule immunitarie vicine trasformandole in complice. In questo studio, l’OPN derivata dalle cellule tumorali agisce come un interruttore maestro che riprogramma i macrofagi attraverso la catena di segnalazione PI3K/AKT e CSF1/CSF1R, creando un terreno favorevole alle metastasi. Interrompendo questa catena—in particolare al livello di CSF1R—i ricercatori sono riusciti a ridurre la diffusione tumorale nei topi. Ciò suggerisce che misurare i livelli di OPN potrebbe aiutare a identificare i pazienti che potrebbero beneficiare di farmaci mirati ai macrofagi e che combinare questi farmaci con trattamenti esistenti o immunoterapie potrebbe offrire nuove speranze per le persone con cancro colorettale avanzato.
Citazione: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Parole chiave: cancro colorettale, osteopontina, macrofagi associati al tumore, metastasi, inibizione di CSF1R