Clear Sky Science · it
TIA1 degli epatociti limita la steatoepatite metabolica sopprimendo tradizionalmente l’mRNA di Srebf1 nei corpi di stress
Perché questo studio sul fegato è rilevante
La malattia del fegato grasso è oggi uno dei problemi cronici epatici più comuni nel mondo, strettamente legata all’obesità e al diabete di tipo 2. Per molte persone rimane silente, ma in alcuni casi progredisce verso una forma infiammatoria pericolosa che può portare a cicatrizzazione, insufficienza epatica e cancro. Questo studio pone una domanda semplice ma cruciale: le cellule epatiche hanno un “freno” interno che aiuta a limitare l’accumulo di grasso e l’infiammazione — e cosa succede quando quel freno viene meno?
Un problema in crescita nei fegati moderni
Gli autori si concentrano su una condizione oggi chiamata malattia epatica steatosica associata a disfunzione metabolica (MASLD) e sulla sua fase infiammatoria più grave, MASH. Queste patologie nascono quando l’apporto energetico supera cronicamente il dispendio, promuovendo l’accumulo di grasso all’interno degli epatociti, stress tossico e infiammazione persistente. Al momento è approvato un solo farmaco che offre benefici parziali, pertanto i ricercatori cercano vie molecolari che possano diventare nuovi bersagli terapeutici. Un campo promettente riguarda come le cellule modulano finemente l’uso dei messaggi genetici dopo la loro sintesi, invece di controllare solo quali geni vengono attivati o spenti.
Un protettore inaspettato all’interno delle cellule epatiche
Il team ha focalizzato l’attenzione su una proteina chiamata TIA1, che lega l’RNA e aiuta ad assemblare piccole goccioline nella cellula note come corpi di stress. Questi corpi immagazzinano temporaneamente i messaggi genetici bloccati quando la cellula è sotto stress. Analizzando campioni di fegato umano e diversi modelli murini di fegato grasso indotto dalla dieta, i ricercatori hanno osservato che i livelli di TIA1 aumentano negli epatociti durante le fasi iniziali di MASLD e MASH. Paradossalmente, persone e topi con cancro epatico avanzato tendono ad avere livelli più bassi di TIA1, suggerendo che possa agire come un fattore protettivo nelle fasi iniziali della malattia ma venga perso in seguito. Nei topi alimentati con diverse diete dannose per il fegato, TIA1 risultava particolarmente abbondante negli epatociti, i principali responsabili del metabolismo epatico.
Cosa succede quando il freno viene rimosso
Per testare la funzione di TIA1, gli scienziati hanno creato topi privi di TIA1 specificamente negli epatociti ed esposti a diete ricche di grassi e ad altri regimi che stressano il fegato. Rispetto ai conspecifici normali, questi animali knockout hanno sviluppato fegati molto più grandi e pallidi, carichi di grasso, accompagnati da maggiore infiammazione, stress ossidativo e fibrosi. I marker di danno epatico sono aumentati nel sangue. Al contrario, ripristinare TIA1 nel fegato mediante un vettore di terapia genica ha ridotto l’accumulo di grasso, attenuato l’infiammazione e migliorato i parametri epatici. Esperimenti paralleli in cellule epatiche murine in coltura esposte a un grasso saturo tossico hanno mostrato che TIA1 è necessario per formare i corpi di stress e che questi corpi contribuiscono a limitare l’accumulo di lipidi e lo stress cellulare.
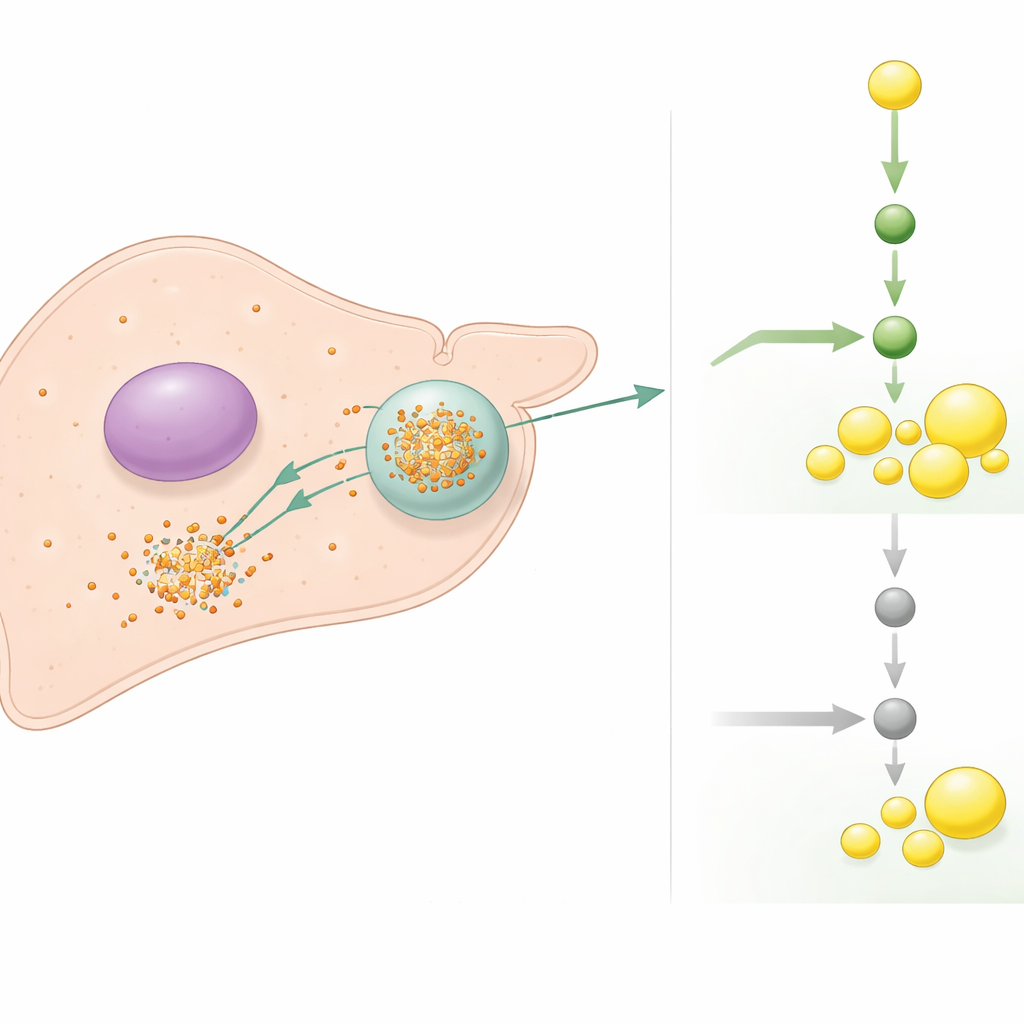
Un semaforo molecolare per i segnali di sintesi lipidica
Approfondendo, gli autori hanno scoperto che TIA1 riconosce direttamente e si lega all’estremità terminale dell’mRNA che codifica per SREBP1, un interruttore maestro della sintesi lipidica negli epatociti. In condizioni di lipotossicità, TIA1 indirizza questo messaggio di SREBP1 nei corpi di stress, dove viene sia impedita la traduzione in proteina sia accelerata la sua degradazione. Quando TIA1 viene rimosso, il messaggio di SREBP1 sfugge a questa sequestrazione, persiste più a lungo ed è tradotto in modo più efficiente, determinando un forte aumento degli enzimi sintetici dei lipidi e peggiorando steatosi e infiammazione. Farmaci che bloccano l’attività di SREBP1 sono stati in grado di attenuare gran parte del danno causato dalla perdita di TIA1 sia nelle cellule epatiche che nei topi, sottolineando che questa via di produzione lipidica è il principale responsabile a valle del malfunzionamento di TIA1.
Cosa significa per i pazienti e per le terapie future
Complessivamente, lo studio rivela un sistema di sicurezza intrinseco negli epatociti: durante lo stress metabolico, TIA1 organizza i corpi di stress che catturano e silenziano il messaggio per SREBP1, frenando la sintesi lipidica e il danno infiammatorio. Quando questo asse TIA1–corpi di stress–SREBP1 è compromesso, la malattia del fegato grasso progredisce più rapidamente verso steatoepatite e fibrosi. Pur restando molto da fare — compresa la conferma di questi meccanismi in coorti più ampie di pazienti e sia nelle donne che negli uomini — i risultati indicano nuovi angoli terapeutici. Potenziare l’attività di TIA1, stabilizzare i corpi di stress protettivi o ridurre più direttamente SREBP1 potrebbero tutti offrire modi per rafforzare le difese del fegato contro le pressioni metaboliche moderne.
Citazione: Liu, R., Chen, J., Wang, J. et al. Hepatocyte TIA1 constrains metabolic steatohepatitis by translationally suppressing Srebf1 mRNA in stress granules. Cell Death Dis 17, 357 (2026). https://doi.org/10.1038/s41419-026-08682-5
Parole chiave: malattia del fegato grasso, corpi di stress, proteine leganti l'RNA, metabolismo dei lipidi, SREBP1