Clear Sky Science · it
La perdita di DIAPH3 accelera la genesi del glioma nei topi
Perché questo studio sul cervello è importante
Il glioblastoma è uno dei tumori cerebrali più letali e, nonostante interventi chirurgici, radioterapia e chemioterapia, la maggior parte dei pazienti sopravvive poco più di un anno. Questo studio pone una domanda fondamentale: quali cambiamenti precoci all’interno delle cellule cerebrali le spingono a diventare tumori così aggressivi e perché questi tumori sono così difficili da eliminare con la radioterapia? Tracciando una singola proteina strutturale nelle cellule cerebrali di topo, i ricercatori mostrano come la sua perdita destabilizzi i cromosomi, acceleri la comparsa dei tumori e aiuti le cellule con caratteristiche staminali del cancro a sopportare radiazioni che dovrebbero distruggerle.
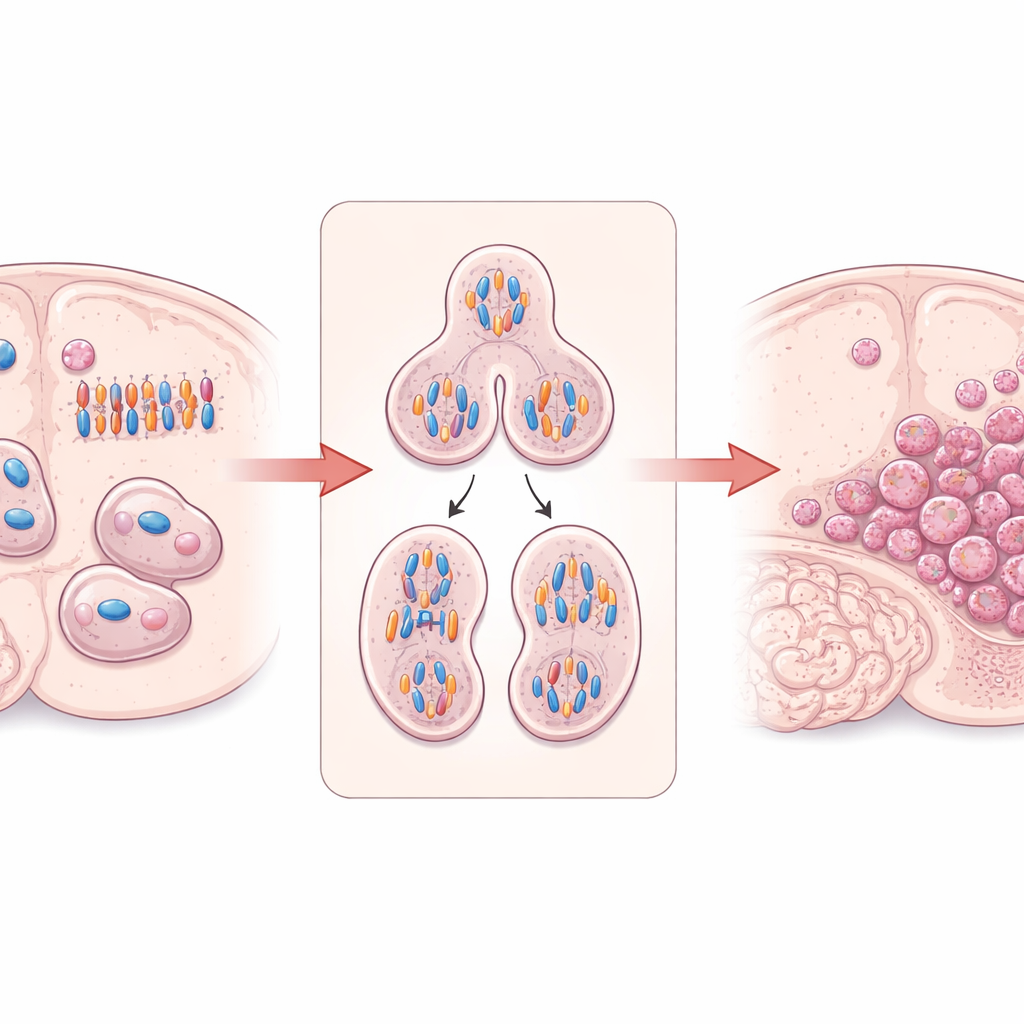
Un “costruttore” cellulare che mantiene l’ordine durante la divisione
Il lavoro si concentra su DIAPH3, una proteina che contribuisce a costruire e organizzare l’impalcatura interna della cellula fatta di filamenti di actina e microtubuli. Nelle cellule staminali cerebrali in divisione, DIAPH3 è fondamentale per formare un fuso corretto — la struttura che separa i cromosomi duplicati — e per dividere una cellula in due. Ricerche precedenti avevano mostrato che, quando DIAPH3 manca nei cervelli in sviluppo dei topi, le cellule in divisione spesso gestiscono male i cromosomi, portando a numeri cromosomici anomali (aneuploidia), blocchi del ciclo cellulare e morte cellulare. È interessante che una piccola regione del cromosoma 13 umano che contiene il gene DIAPH3 sia frequentemente deleta nel glioblastoma, e che livelli più alti di DIAPH3 siano stati associati a una migliore sopravvivenza in alcuni pazienti, suggerendo che questa proteina possa agire come soppressore tumorale nel cervello.
Ingegnerizzare cervelli di topo per far crescere tumori
Per verificare se la perdita di DIAPH3 promuove davvero il cancro cerebrale, il gruppo ha creato topi nei quali due geni potevano essere cancellati selettivamente nelle cellule staminali che formano la corteccia: Diaph3 e Trp53, quest’ultimo codificante il noto guardiano del genoma, p53. I topi privi solo di Diaph3 in questa regione non hanno sviluppato tumori nemmeno dopo due anni, il che implica che p53 può ancora eliminare cellule fortemente anomale. Al contrario, i topi privi di Trp53 da soli, o di entrambi Trp53 e Diaph3, hanno infine formato gliomi diffusi di alto grado che al microscopio assomigliavano molto alla malattia umana. Tramite ripetute risonanze magnetiche ad altissimo campo, i ricercatori hanno mostrato che gli animali privi di entrambi i geni sviluppavano tumori rilevabili prima e che, a mezza età, ospitavano più spesso grandi gliomi, in particolare nei bulbi olfattivi, rispetto ai topi privi solo di Trp53. Il tasso di crescita del tumore, una volta iniziato, era simile tra i gruppi: ciò che cambiava era quanto presto i tumori comparivano.
Caos cromosomico e attività genica riorganizzata
Per approfondire perché la perdita di DIAPH3 accelera l’insorgenza tumorale, il team ha esaminato l’attività genica nei bulbi olfattivi di topi giovani prima che fossero visibili tumori. Negli animali privi sia di Diaph3 sia di Trp53, 126 geni erano espressi a livelli diversi rispetto ai mutanti con solo Trp53, e quasi la metà di questi era già stata collegata al cancro. Molte modificazioni si raggruppavano in vie che guidano crescita cellulare, migrazione e formazione di vasi sanguigni, incluse le vie VEGF, MAPK, RAS, Rap1 e cAMP, oltre a reti di recettori accoppiati a proteine G. Questo panorama molecolare alterato suggeriva che le cellule venivano spinte verso uno stato simile al cancro in una fase più precoce. L’analisi del numero di copie genomiche sui tumori completamente formati ha rivelato che la carenza di DIAPH3 non aumentava molto le piccole alterazioni focali del DNA ma, al contrario, favoriva ampie perdite e guadagni a livello di interi cromosomi — esattamente l’aneuploidia prevista da una segregazione cromosomica difettosa.
Danno al DNA incorporato e cellule staminali tumorali più resistenti
Le cellule tumorali aneuploidi mostravano più danni interni al DNA, rilevati da livelli elevati del marcatore di rotture del DNA γ‑H2AX diffuso nei nuclei cellulari. Eppure questi tumori continuavano a crescere, il che implica che avevano acquisito modi per tollerare tale stress. Confrontando l’espressione genica nei tumori consolidati, i ricercatori hanno trovato centinaia di geni alterati dalla perdita di DIAPH3, inclusa una marcata amplificazione e sovrapproduzione del recettore per il fattore di crescita FGFR2 in molti tumori doppiamente mutati. Si sa che FGFR2 potenzia i meccanismi di riparazione del DNA nelle cellule di glioblastoma e che la sua attivazione è stata collegata alla resistenza alle radiazioni. Il team ha isolato cellule con caratteristiche staminali di glioma dai tumori dei topi e ha testato la loro risposta a una dose clinicamente rilevante di radiazioni ionizzanti. Prima del trattamento, la frequenza delle cellule staminali era simile in entrambi i genotipi, ma dopo l’irradiazione, le colture provenienti dai tumori privi di DIAPH3 mantenevano all’incirca il doppio delle cellule staminali attive rispetto a quelle dei tumori con solo Trp53, dimostrando una maggiore radioresistenza.
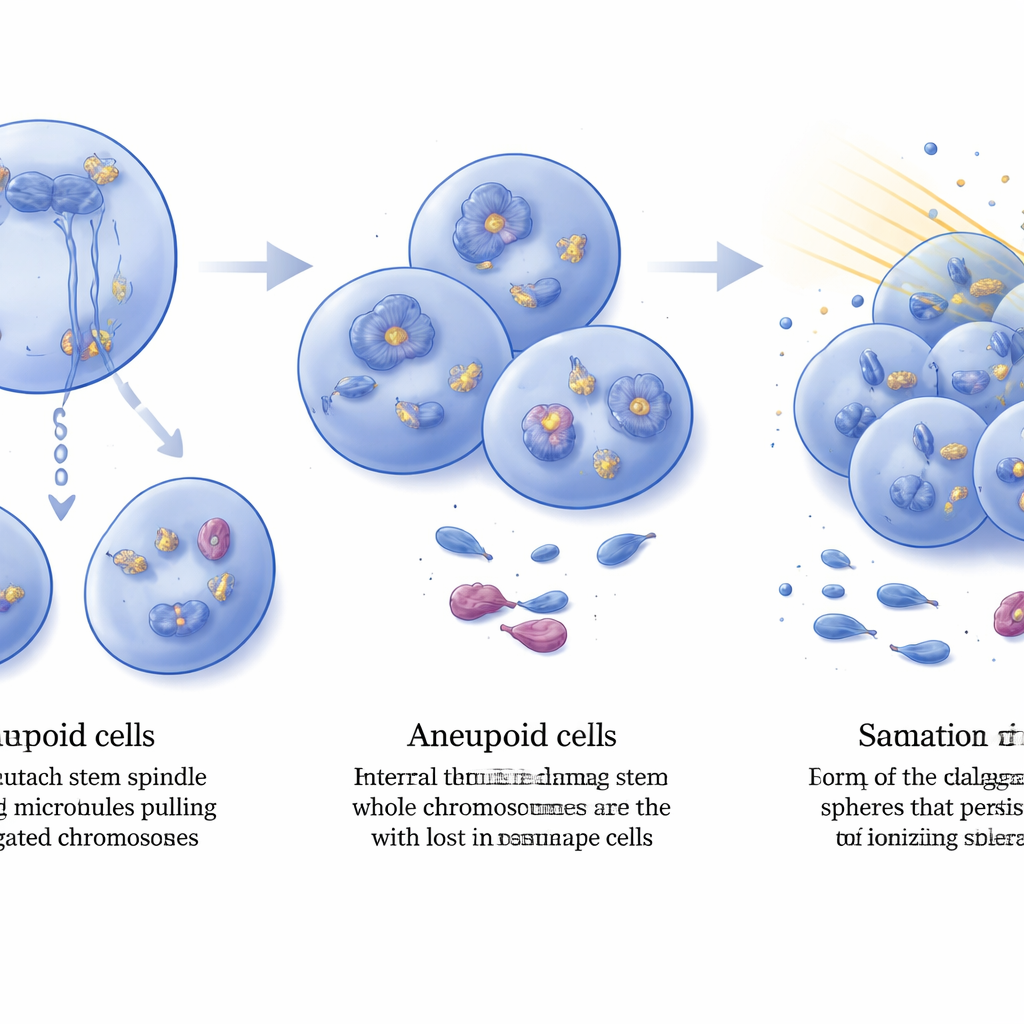
Cosa significa per il cancro cerebrale
Nel complesso, lo studio dipinge DIAPH3 come un guardiano che aiuta le cellule staminali cerebrali a dividersi mantenendo il corretto numero di cromosomi. Quando sia DIAPH3 sia p53 vengono a mancare, la divisione cellulare diventa incline all’errore, interi cromosomi vengono persi o guadagnati e il danno al DNA si accumula. Invece di morire, alcune cellule si adattano amplificando fattori legati alla riparazione, come FGFR2, trasformandosi in gliomi aneuploidi di alto grado le cui cellule con tratti staminali sono particolarmente resistenti alle radiazioni. Sebbene i modelli murini non riproducano ogni aspetto del glioblastoma umano, questi risultati indicano DIAPH3 come possibile biomarcatore prognostico e come punto nodale nelle reti che controllano l’inizio del tumore, la stabilità del genoma e la risposta terapeutica — aprendo nuove strade per terapie che un giorno potrebbero rendere questo devastante tumore cerebrale più vulnerabile ai trattamenti esistenti.
Citazione: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Parole chiave: glioblastoma, instabilità cromosomica, cellule staminali dei tumori cerebrali, resistenza alle radiazioni, geni soppressori del tumore