Clear Sky Science · it
Cellule di glioblastoma che sfuggono alla morte indotta da chemioradioterapia mostrano un programma glicolitico biforcuto
Perché questo studio sul cancro cerebrale è importante
Il glioblastoma è uno dei tumori cerebrali più letali negli adulti e quasi sempre ricresce dopo intervento chirurgico, chemioterapia e radioterapia. Questo studio pone una domanda cruciale: che cosa distingue il piccolo gruppo di cellule tumorali che sopravvive al trattamento e in seguito riaccende la malattia? Seguendo nel tempo come queste cellule gestiscono gli zuccheri, i ricercatori rivelano una strategia di sopravvivenza nascosta che potrebbe spiegare perché i trattamenti attuali falliscono così spesso—e suggeriscono nuovi modi per recidere il sostentamento del tumore.
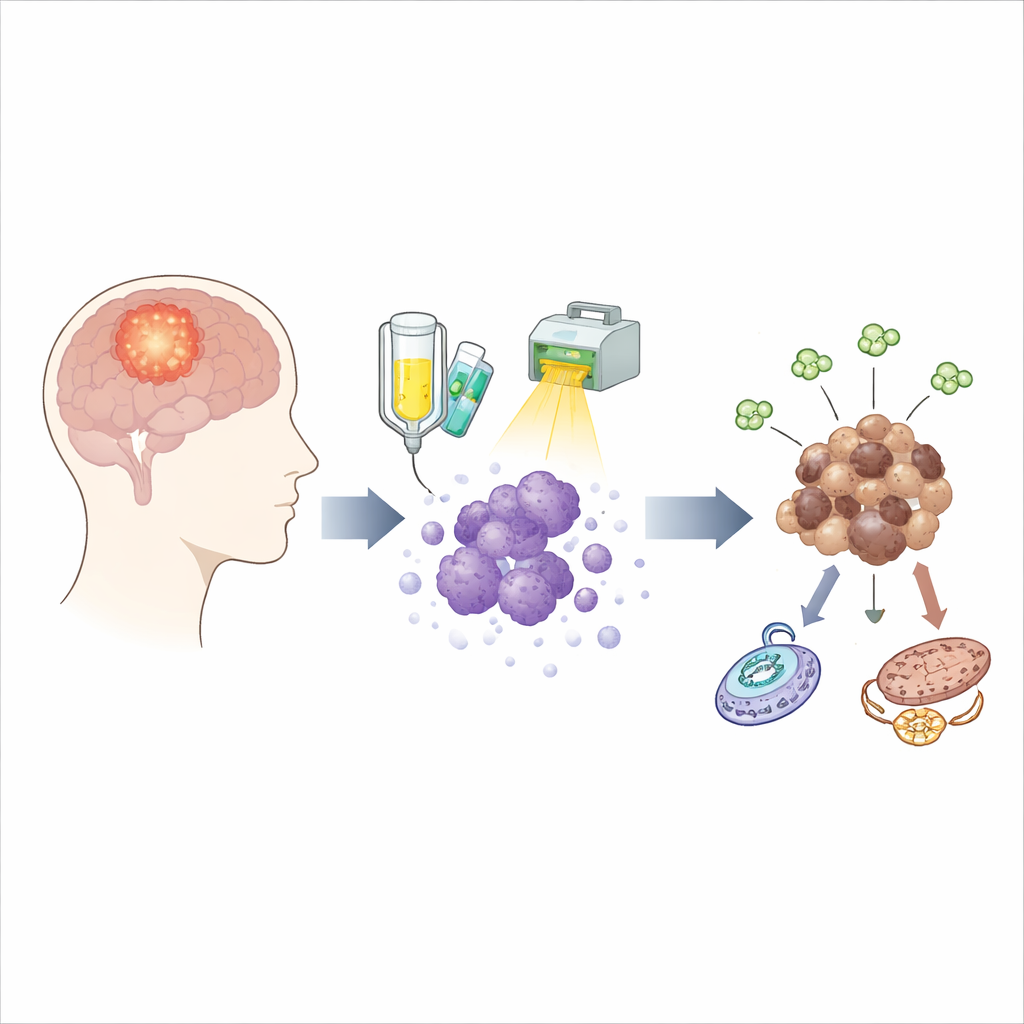
I sopravvissuti nascosti dopo il trattamento
La cura standard per il glioblastoma combina un farmaco chiamato temozolomide con la radioterapia. Mentre questa combinazione uccide la maggior parte delle cellule tumorali, una minoranza tenace sopravvive e può dare origine a un nuovo tumore mesi dopo. Per cogliere questi sopravvissuti in azione, il team ha usato cellule tumorali prelevate direttamente da dieci diversi pazienti ed è stato esposto a uno schema di trattamento progettato per imitare da vicino quanto somministrato in clinica. Hanno campionato le cellule vive in diversi momenti durante e dopo il trattamento e hanno anche studiato tumori corrispondenti cresciuti nei topi, permettendo loro di seguire come i sopravvissuti cambiano nel tempo anziché limitarsi a confrontare tumori prima e dopo la recidiva.
Come le cellule tumorali cambiano il modo in cui usano lo zucchero
Il tessuto cerebrale consuma una quota notevole dello zucchero del corpo, e le cellule di glioblastoma ne sono particolarmente ghiotte. I ricercatori hanno scoperto che, con il progredire del trattamento, le cellule sopravvissute assorbivano ancora più glucosio dall’ambiente. Tuttavia, inaspettatamente, non bruciavano semplicemente questo carburante in modo più rapido. Invece queste cellule riducevano la produzione di lattato, il tipico prodotto di scarto della rapida demolizione dello zucchero nei tumori. Misurazioni di proteine chiave hanno mostrato uno schema sorprendente e biforcuto: i componenti che importano lo zucchero nella cellula e ne avviano la degradazione aumentavano, mentre quelli che gestiscono le fasi successive e la produzione di lattato diminuivano. Questo programma “biforcuto” significa che lo zucchero entra e comincia a essere processato, ma la via d’uscita abituale verso il lattato è in parte bloccata.
Deviare il carburante verso mattoni di costruzione e centrali energetiche
Dove va lo zucchero deviato? Usando glucosio appositamente marcato e misure avanzate dei metaboliti, il gruppo ha mostrato che le cellule sopravvissute convogliano gran parte di questo carbonio in due principali destinazioni. Una è una via collaterale chiamata via del pentoso fosfato, che genera i materiali di base necessari per fabbricare i mattoni del DNA e dell’RNA. In queste cellule molti componenti nucleotidici e geni correlati erano aumentati, suggerendo una forte spinta verso la ricostruzione e la preparazione per una nuova crescita. La seconda destinazione sono le centrali energetiche della cellula, i mitocondri. Gli enzimi del ciclo energetico mitocondriale aumentavano, e lavori precedenti dello stesso gruppo avevano mostrato un maggiore import di combustibile derivato dallo zucchero in queste strutture. Nel complesso, ciò rivela una riorganizzazione coordinata: meno fermentazione sprecona verso il lattato e più investimento in riparazione, materiali per la crescita e produzione energetica flessibile.
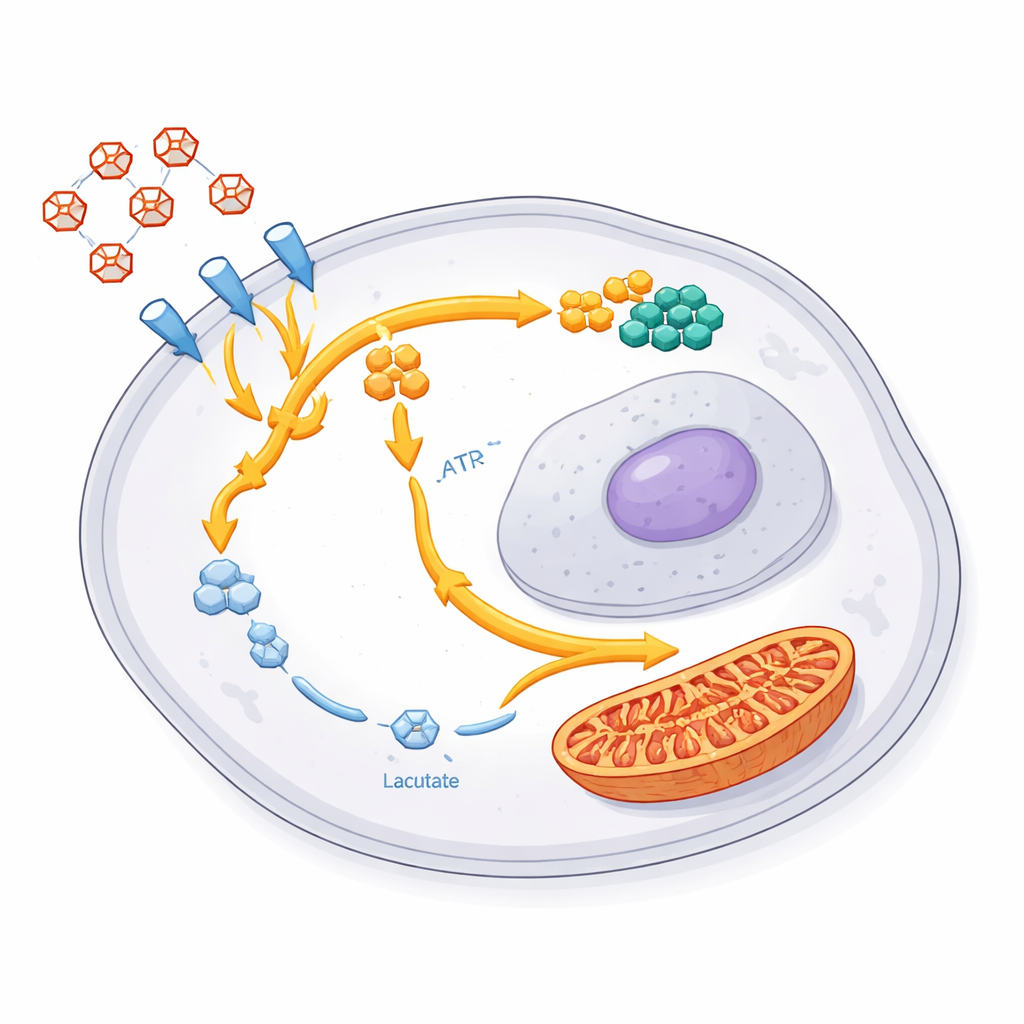
Un copione di sopravvivenza condiviso fra tumori e negli animali
I tumori di glioblastoma variano molto da paziente a paziente, il che spesso vanifica terapie standardizzate. Nonostante questa diversità, tutti e dieci i modelli derivati da pazienti hanno mostrato lo stesso spostamento fondamentale dopo chemioradioterapia: aumento delle fasi iniziali di gestione dello zucchero, diminuzione delle fasi tardive e dell’emissione di lattato, e maggiore attività mitocondriale. È importante che la stessa firma sia apparsa nei tumori cerebrali dei topi cresciuti a partire da cellule di pazienti e trattati con versioni adattate della terapia standard. I tumori recidivanti in questi animali mantenevano ancora il programma glicolitico alterato, indicando che non si tratta di un effetto passeggero ma di un tratto stabile delle cellule che riescono a sopravvivere al trattamento e a ricostruire il cancro.
Cosa significa per i trattamenti futuri
Per un lettore non specialista, il messaggio centrale è che le cellule di glioblastoma sopravvissute non si limitano a “nascondersi” dal trattamento; riorganizzano attivamente il modo in cui usano lo zucchero per restare vive. Assorbono più glucosio, evitano di trasformarlo in scarto e lo incanalano invece nella produzione di mattoni del DNA e nel potenziamento dei mitocondri—aiutandole a riparare i danni, mantenere uno stato flessibile simile alle cellule staminali e, infine, rigenerare il tumore. Rivelando questo stato metabolico di sopravvivenza condiviso, lo studio indica nuove idee terapeutiche: mirare alle fasi iniziali del processamento dello zucchero, alla via collaterale per la sintesi dei nucleotidi o alla dipendenza mitocondriale di queste cellule potrebbe rendere la chemioradioterapia standard più completa, lasciando meno fuggitivi in grado di riavviare la malattia.
Citazione: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Parole chiave: glioblastoma, metabolismo del cancro, utilizzo del glucosio, resistenza alla terapia, via del pentoso fosfato