Clear Sky Science · it
Orchestrazione metabolica guidata da GGCT: deviare il glutamine verso la biosintesi del glutatione aumentando l’anaplerosi del glucosio per la proliferazione tumorale
Perché questo è importante per il trattamento del cancro
Le cellule tumorali crescono rapidamente e per farlo consumano grandi quantità di carburante, dovendo al tempo stesso proteggersi costantemente dai sottoprodotti tossici del loro stesso metabolismo. Questo studio rivela come un enzima poco conosciuto, GGCT, aiuti i tumori del fegato e della prostata a deviare in modo intelligente due nutrienti comuni — glutamina e glucosio — in modo che possano sia alimentare la crescita sia mantenere sotto controllo le molecole dannose chiamate specie reattive dell’ossigeno. Capire questo gioco di prestigio metabolico potrebbe aprire nuove strategie per affamare i tumori o sopraffare le loro difese.
Come le cellule tumorali bilanciano carburante e protezione
Le cellule tumorali dipendono fortemente dalla glutamina, un amminoacido che svolge un doppio ruolo: può essere degradato per alimentare il ciclo energetico principale della cellula e fornisce anche i mattoni per il glutatione, un potente antiossidante che neutralizza le specie reattive dell’ossigeno. Gli autori hanno prima confermato che i livelli di glutamina sono più alti nei tumori epatici rispetto ai tessuti sani circostanti e che le cellule tumorali coltivate con più glutamina si dividono più rapidamente sia in coltura sia nei topi. Quando la glutamina scarseggia, le cellule rallentano, proteine chiave del ciclo cellulare diminuiscono e i tumori negli animali si riducono — in parte perché le difese antiossidanti si indeboliscono e le specie reattive dell’ossigeno si accumulano.
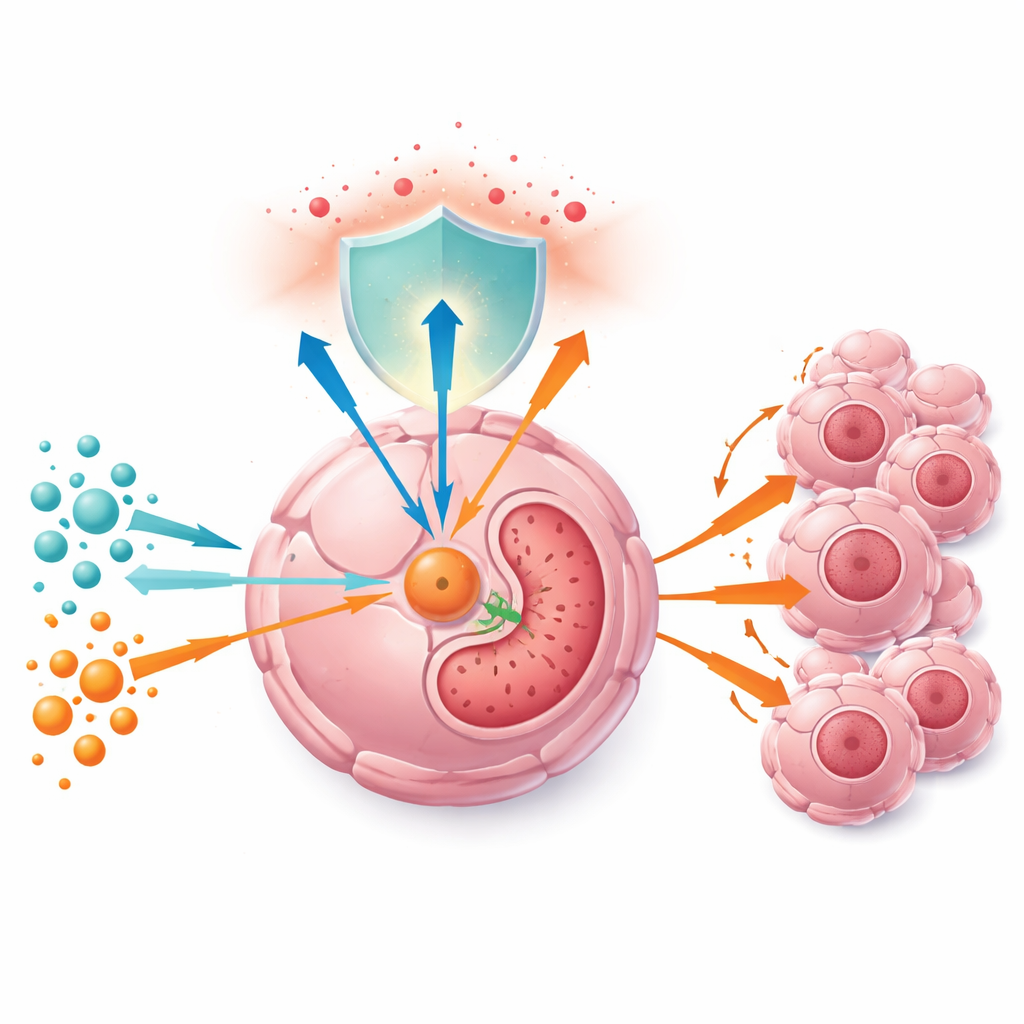
Un interruttore metabolico nascosto in bella vista
Analizzando campioni di pazienti e ampi database sul cancro, il team ha scoperto che l’enzima GGCT è costantemente più abbondante nei tumori del fegato e della prostata rispetto ai tessuti normali, e che livelli più alti di GGCT prevedono esiti peggiori. Sia nei campioni tumorali sia nelle cellule in coltura, i livelli di GGCT aumentano in parallelo con la concentrazione di glutamina, suggerendo che i tumori “leggono” la disponibilità di glutamina tramite questa proteina. I ricercatori hanno delineato una catena di controllo: la glutamina mantiene attivo il fattore pro‑crescita c‑Myc, che sopprime un piccolo RNA regolatorio chiamato miR‑29b‑3p; quando miR‑29b‑3p è basso, GGCT viene liberato dalla sua inibizione e si accumula. In condizioni di carenza di glutamina, questa catena si inverte, miR‑29b‑3p aumenta, i messaggi di GGCT vengono degradati più rapidamente e il livello dell’enzima diminuisce.
Reindirizzare la glutamina e assorbire più glucosio
Per capire cosa fa effettivamente GGCT all’interno della cellula, gli autori ne hanno ridotto o aumentato l’espressione e hanno misurato sia il comportamento cellulare sia centinaia di metaboliti. Il silenziamento di GGCT bloccava le cellule nel ciclo di divisione, riduceva le loro colonie e abbassava nettamente il glutatione aumentando le specie reattive dell’ossigeno; l’aggiunta di un antiossidante chimico ha parzialmente ripristinato la crescita. Al microscopio i mitocondri apparivano anormalmente allungati e meno efficienti nel consumo di ossigeno, mentre le cellule cercavano di compensare aumentando la glicolisi, il primo passo della degradazione degli zuccheri. Un profilo metabolico dettagliato ha mostrato che gli intermedi del ciclo energetico centrale calavano quando GGCT veniva perso e aumentavano quando era sovraespresso.
Tracciare il percorso degli atomi di carbonio
Il gruppo ha poi seguito atomi di glutamina e glucosio marcati mentre scorrevano attraverso il metabolismo tumorale. Quando GGCT era sovraespresso, meno glutamina marcata finiva nel ciclo energetico e una quota maggiore veniva incanalata nel glutatione di nuova sintesi, a supporto delle difese antiossidanti. Allo stesso tempo, il glucosio marcato contribuiva in misura maggiore al ciclo, compensando la glutamina deviata. Una forma mutante di GGCT priva della normale attività enzimatica non poteva guidare questi cambiamenti né favorire la proliferazione, dimostrando che la funzione catalitica di GGCT è cruciale. È importante che fornire piruvato in eccesso o modificare l’ingresso nel ciclo energetico ripristinasse i livelli energetici cellulari ma non riducesse le specie reattive dell’ossigeno, indicando che GGCT controlla principalmente l’equilibrio redox attraverso il glutatione, non mediante semplici variazioni dell’apporto energetico.
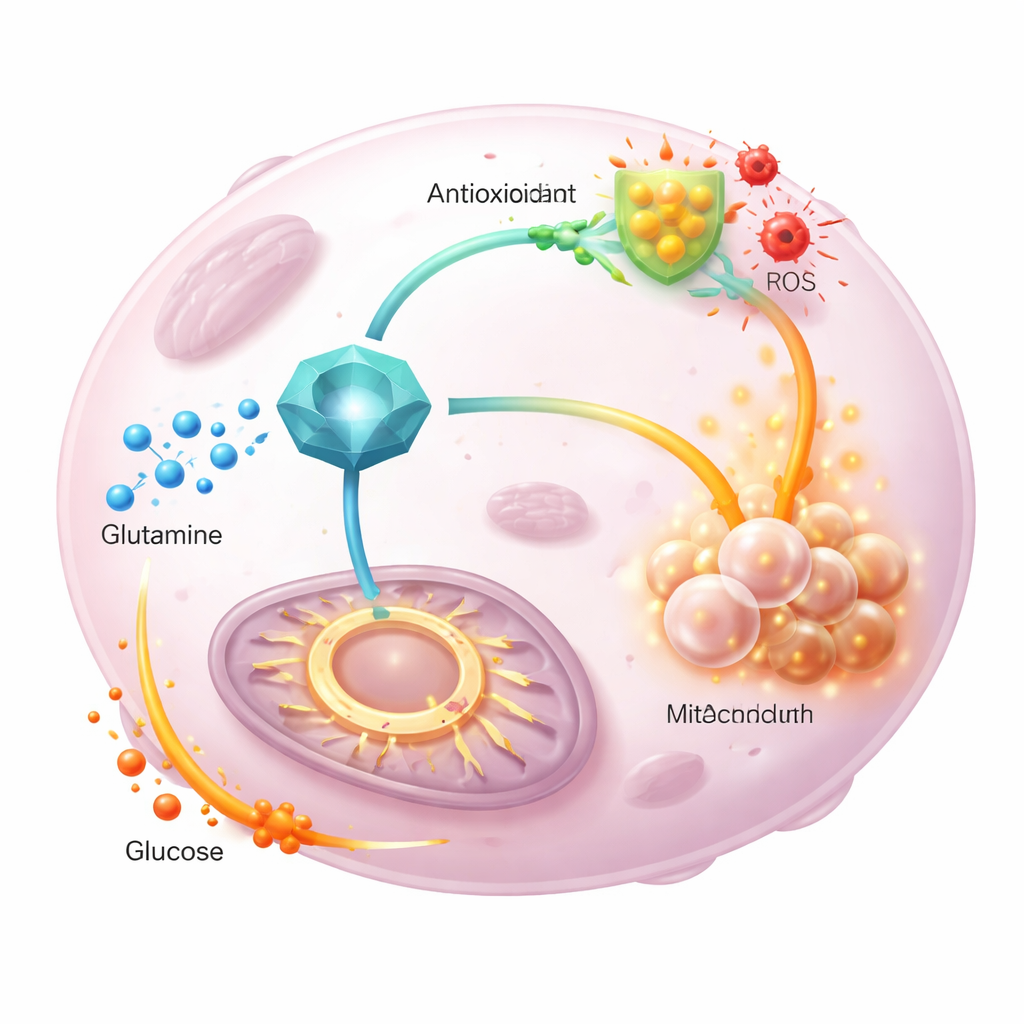
Cosa significa per le terapie future
Nel complesso, i risultati collocano GGCT come un coordinatore centrale che permette ai tumori di dividere i compiti della glutamina: indirizza più di questo nutriente verso la produzione di antiossidanti mentre attira il glucosio nel ciclo energetico per mantenere attiva la divisione cellulare. Nei modelli animali, l’abbattimento di GGCT rallentava la crescita tumorale, riduceva il glutatione e aumentava lo stress ossidativo, e questi effetti potevano essere parzialmente invertiti con un farmaco antiossidante. Per un lettore non specialista, il messaggio è che alcuni tumori sopravvivono usando GGCT come un quadro elettrico metabolico; farmaci che disattivano questo interruttore potrebbero indebolire contemporaneamente le difese del tumore contro il danno ossidativo e disturbare la sua flessibilità nell’uso dei nutrienti, rendendo più efficaci i trattamenti standard.
Citazione: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Parole chiave: metabolismo del cancro, glutamina, glutatione, stress ossidativo, enzima GGCT