Clear Sky Science · it
AATF sostiene la proliferazione delle cellule di glioblastoma mantenendo la respirazione mitocondriale tramite un meccanismo dipendente da NRF-1
Perché conta l’uso di energia nei tumori cerebrali
Il glioblastoma è la forma più aggressiva di tumore cerebrale nell’adulto e, nonostante chirurgia, radioterapia e chemioterapia, la maggior parte dei pazienti sopravvive poco più di un anno. Questo studio pone una domanda apparentemente semplice ma di ampie implicazioni: come alimentano la loro crescita incessante le cellule di glioblastoma e si può interrompere questa fonte di carburante? Gli autori si concentrano su una proteina regolatoria poco nota chiamata AATF e mostrano che essa aiuta le cellule tumorali a mantenere i loro “produttori di energia” — i mitocondri — in piena attività. Comprendere questo sistema di supporto nascosto potrebbe aprire nuove strade per rallentare o fermare questi tumori mortali.
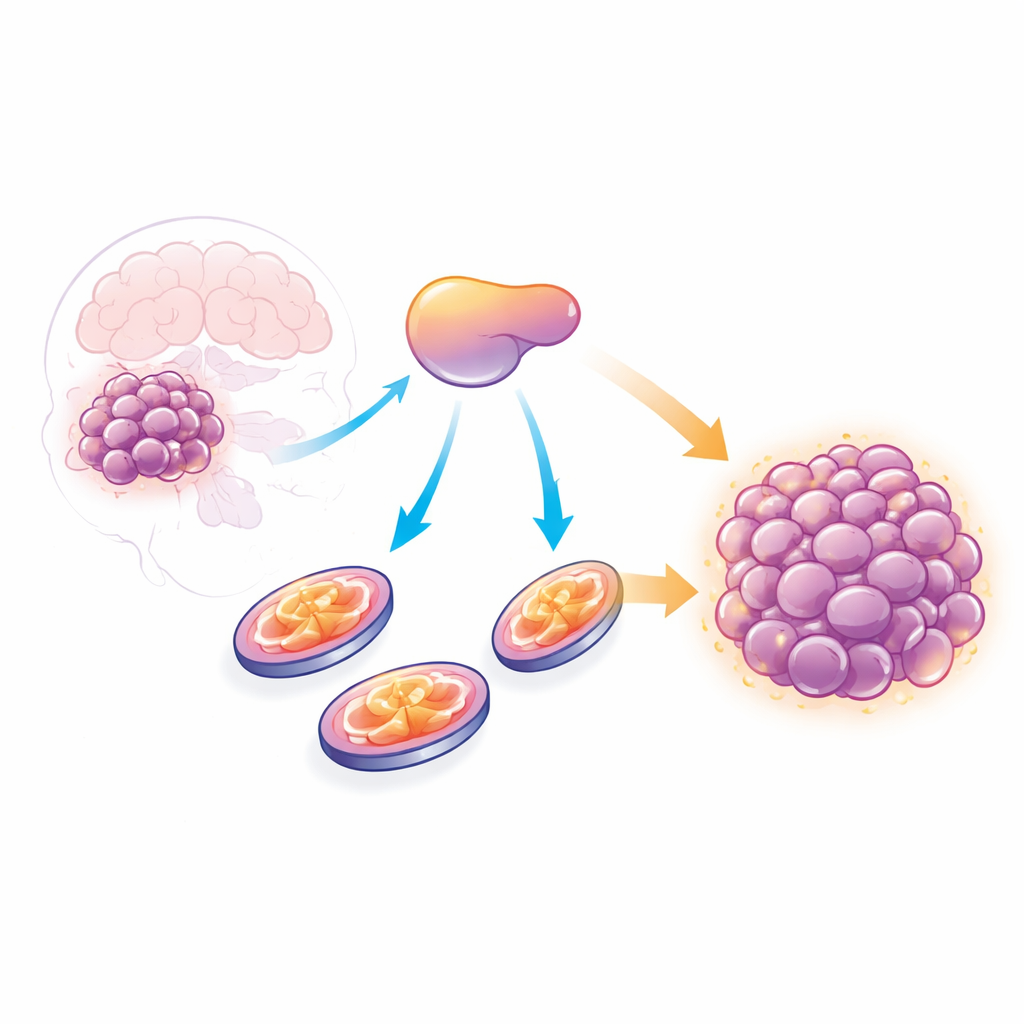
Un aiuto nascosto nella crescita tumorale
Le cellule tumorali spesso si affidano a una strategia di produzione di energia basata sul consumo di zucchero, la glicolisi, a lungo considerata la loro via energetica distintiva. Tuttavia lavori recenti hanno rivelato che molti tumori, incluso il glioblastoma, dipendono anche in modo marcato dai mitocondri, che producono energia tramite la fosforilazione ossidativa (OXPHOS). Analizzando ampi dataset di pazienti, i ricercatori hanno scoperto che i livelli di AATF sono più alti nei tessuti di glioblastoma rispetto al cervello normale e aumentano con il grado tumorale. I pazienti i cui tumori esprimevano più AATF tendevano ad avere una sopravvivenza più breve, suggerendo che questa proteina sia legata a una malattia più aggressiva.
Spegnere AATF rallenta le cellule cancerose
Per verificare se AATF sia solo un marcatore o un vero motore della crescita, il gruppo ha ridotto i suoi livelli in diverse linee cellulari di glioblastoma usando strumenti a RNA e l’interferenza CRISPR. Le cellule prive di AATF si moltiplicavano molto più lentamente, si accumulavano nella fase di riposo del ciclo cellulare e formavano molte meno colonie nel lungo periodo. È importante che questo rallentamento non fosse accompagnato da un’estesa morte cellulare o senescenza, il che significa che le cellule erano vive ma bloccate. Quando cellule deprivate di AATF sono state impiantate in topi, i tumori risultanti erano molto più piccoli e presentavano meno cellule in divisione, confermando che AATF è necessario per una crescita tumorale robusta nei tessuti viventi.
Riprogrammare la rete energetica del tumore
Poiché AATF è noto per influenzare l’attività genica, gli autori hanno esaminato come la sua perdita rimodelli il programma genetico della cellula. Il sequenziamento dell’RNA ha rivelato che centinaia di geni modificano la loro attività quando AATF è silenziato. Tra i geni più costantemente ridotti vi erano quelli che codificano componenti chiave della macchina OXPHOS mitocondriale. Le misure proteiche hanno confermato che molte parti dei complessi produttori di energia all’interno dei mitocondri risultavano ridotte. Quando i ricercatori hanno misurato direttamente il consumo di ossigeno e la produzione di energia, le cellule private di AATF mostravano una respirazione inferiore e livelli di ATP ridotti. Allo stesso tempo i loro mitocondri producevano più specie reattive dell’ossigeno, assumevano una morfologia frammentata a forma di anello associata a disfunzione e aumentavano l’espressione di geni che favoriscono la fissione mitocondriale, tutti segnali di una rete energetica sotto stress e compromessa.
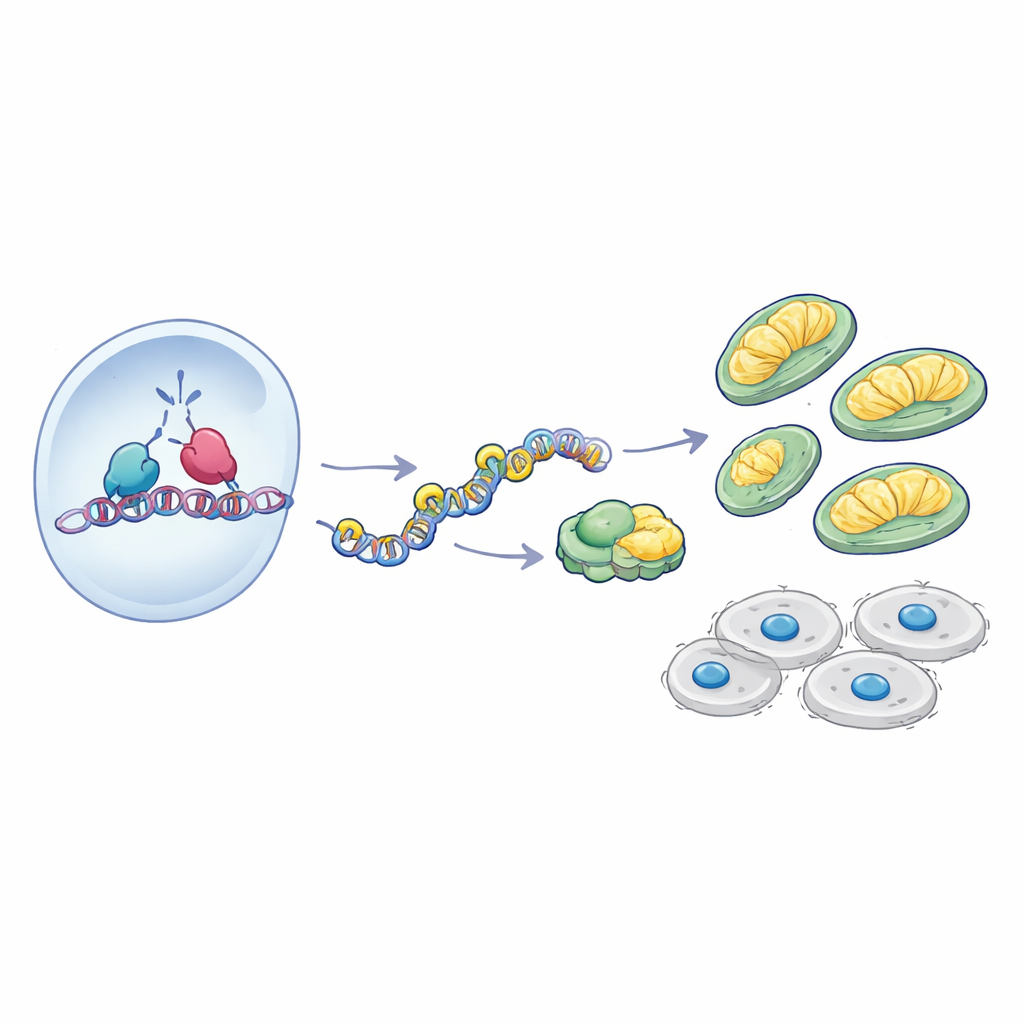
Una collaborazione a livello del DNA
Come esercita AATF un controllo così marcato sui geni mitocondriali? Lo studio si è concentrato su NRF-1, un fattore di trascrizione già noto come regolatore principale della biogenesi mitocondriale e dell’OXPHOS. I dati dei pazienti mostravano che i livelli di AATF e NRF-1 aumentano e diminuiscono insieme nel glioblastoma, e gli esperimenti sulle linee cellulari hanno rivelato che le due proteine interagiscono fisicamente. Con la cromatina immunoprecipitazione, gli autori hanno dimostrato che AATF è presente nelle regioni promotrici di diversi geni OXPHOS proprio dove si lega NRF-1. Quando NRF-1 è stato ridotto, il legame di AATF a questi promotori è diminuito nettamente, indicando che NRF-1 aiuta a reclutare AATF sul DNA. Inoltre, nelle cellule prive di AATF, NRF-1 poteva ancora legare il DNA, ma il reclutamento dell’enzima trascrizionale RNA polimerasi II risultava compromesso e la cromatina circostante diventava più compatta, con meno marcatori istonici attivanti e più marcatori repressivi. In sostanza, senza AATF, NRF-1 si trova sugli interruttori, ma le luci non si accendono.
Cosa significa per i trattamenti futuri
Per un non specialista, il messaggio è che le cellule di glioblastoma usano una partnership specializzata tra AATF e NRF-1 per mantenere i loro motori mitocondriali a pieno regime, fornendo l’energia necessaria per la rapida divisione e la resistenza alle terapie. AATF agisce come copilota sui geni mitocondriali, plasmando l’ambiente locale del DNA affinché NRF-1 possa guidare una forte espressione dei componenti OXPHOS. Rimuovere AATF inceppa questo sistema: i mitocondri vacillano, si accumulano sottoprodotti dannosi e le cellule tumorali perdono il loro vantaggio proliferativo sia in coltura sia nei topi. Sebbene attualmente non esistano farmaci che blocchino direttamente AATF, questo lavoro lo identifica come un target promettente nel glioblastoma e suggerisce che interrompere l’asse AATF–NRF-1–mitocondri potrebbe indebolire l’approvvigionamento energetico del tumore e migliorare l’efficacia delle terapie esistenti.
Citazione: Sorino, C., Di Giovenale, S., Falcone, I. et al. AATF supports proliferation of glioblastoma cells by sustaining mitochondrial respiration through an NRF-1-dependent mechanism. Cell Death Dis 17, 349 (2026). https://doi.org/10.1038/s41419-026-08617-0
Parole chiave: glioblastoma, respirazione mitocondriale, fosforilazione ossidativa, regolazione trascrizionale, metabolismo del cancro