Clear Sky Science · it
La transdifferenziazione adipogenica reprogramma le cellule PDAC ad alto EMT in uno stato post-mitotico simile agli adipociti e limita le metastasi
Trasformare cellule tumorali aggressive in innocuo tessuto adiposo
Il cancro del pancreas è uno dei tumori più letali, in gran parte perché si diffonde precocemente e resiste ai trattamenti standard. Questo studio esplora un’idea radicalmente diversa: invece di cercare di avvelenare o privare di nutrienti le cellule tumorali, cosa succederebbe se potessimo indurre le cellule pancreatiche più pericolose a trasformarsi in cellule simili al grasso che non si dividono più né migrano nel corpo? Il lavoro descrive come i ricercatori abbiano spinto cellule di carcinoma pancreatico altamente aggressive verso uno stato stabile simile agli adipociti, rallentando la crescita tumorale e riducendo la diffusione nei topi, suggerendo una nuova via per controllare questa malattia devastante.
Perché il cancro del pancreas è così difficile da fermare
Il carcinoma duttale del pancreas, la forma principale di cancro pancreatic0, ha una prognosi molto sfavorevole: solo circa uno su otto pazienti è vivo a cinque anni dalla diagnosi. Parte del problema è che molte cellule tumorali in questo cancro si trovano in uno stato di continua trasformazione chiamato EMT, che le rende più mobili, invasive e resistenti ai farmaci. I tentativi di bloccare i numerosi segnali che guidano questo stato hanno dato benefici limitati. Allo stesso tempo, il pancreas e i suoi tumori mostrano una sorprendente tendenza ad accumulare cellule adipose, sollevando la domanda se questa flessibilità nascosta dell’identità cellulare possa essere sfruttata. Gli autori hanno ipotizzato che se le cellule tumorali pancreatiche ricche di EMT sono già predisposte al cambiamento, forse possono essere reindirizzate verso un’identità tranquilla simile al grasso anziché una invasiva.
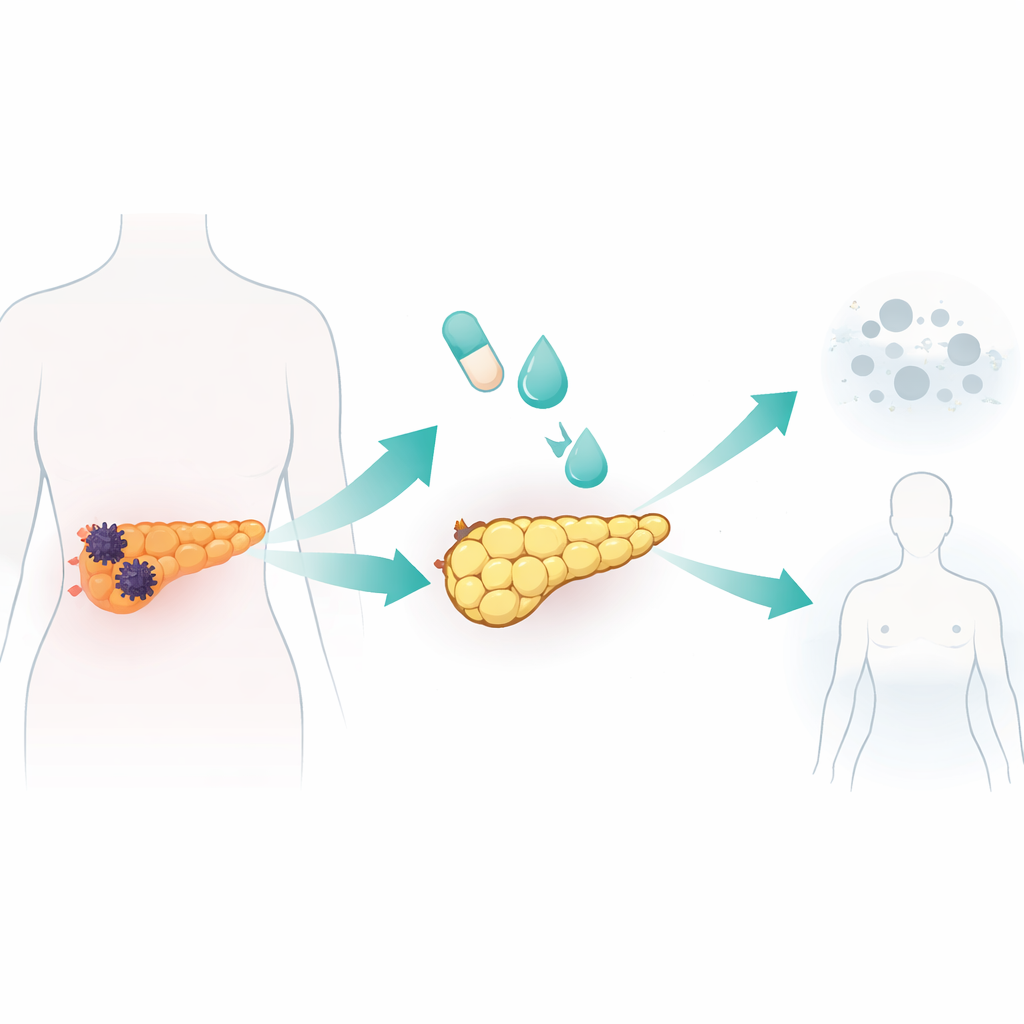
Riprogrammare le cellule tumorali in cellule simili agli adipociti in laboratorio
Il team ha testato un cocktail standard per la formazione di adipociti, impiegato in precedenti studi di biologia del tessuto adiposo e nel cancro al seno, su sette linee cellulari umane di carcinoma pancreatico e su una linea cellulare pancreatica normale. La miscela combinava insulina e uno steroide con rosiglitazone, un farmaco che attiva un regolatore maestro dell’adipogenesi, più una proteina di segnalazione chiamata BMP2 per sbloccare la plasticità cellulare. Una linea tumorale, chiamata AsPC-1, è risultata particolarmente reattiva. In dieci giorni queste cellule sono diventate più grandi e tondeggianti e si sono riempite di goccioline lipidiche, segni distintivi degli adipociti. Hanno attivato geni e proteine tipiche degli adipociti maturi e hanno mostrato un metabolismo lipidico robusto, incluso il rilascio di adiponectina e la capacità di mobilizzare i grassi immagazzinati su stimolo. Crucialmente, queste cellule convertite hanno cessato di proliferare, si sono bloccate in una fase precoce del ciclo cellulare e hanno migrato e invaso molto meno rispetto alle cellule tumorali non trattate.
Spegnere il programma tumorale in profondità nella cellula
Per capire cosa accadesse a livello molecolare, i ricercatori hanno analizzato il packaging del DNA e l’attività genica delle cellule convertite. Hanno riscontrato un ampio indurimento della cromatina, il complesso DNA–proteine che controlla l’accesso ai geni, insieme a una diminuzione globale dell’espressione genica, entrambe caratteristiche di cellule non proliferanti. I geni che supportano l’EMT, l’invasione e le metastasi, incluse le enzimi che degradano la matrice e i regolatori chiave dell’EMT, sono stati fortemente repressi, mentre i geni correlati al tessuto adiposo sono stati potenziati. Il profilo genico complessivo si è spostato da un’identità mesenchimale e altamente mobile a una che assomigliava strettamente agli adipociti maturi. I segnali legati alla crescita cellulare e alla risposta a un importante fattore EMT, il TGF-beta, sono stati attenuati, mentre le vie correlate alla gestione dei lipidi e all’adesione cellulare sono state potenziate. Questi cambiamenti suggeriscono che le cellule non sono state semplicemente rallentate, ma sostanzialmente riconfigurate.
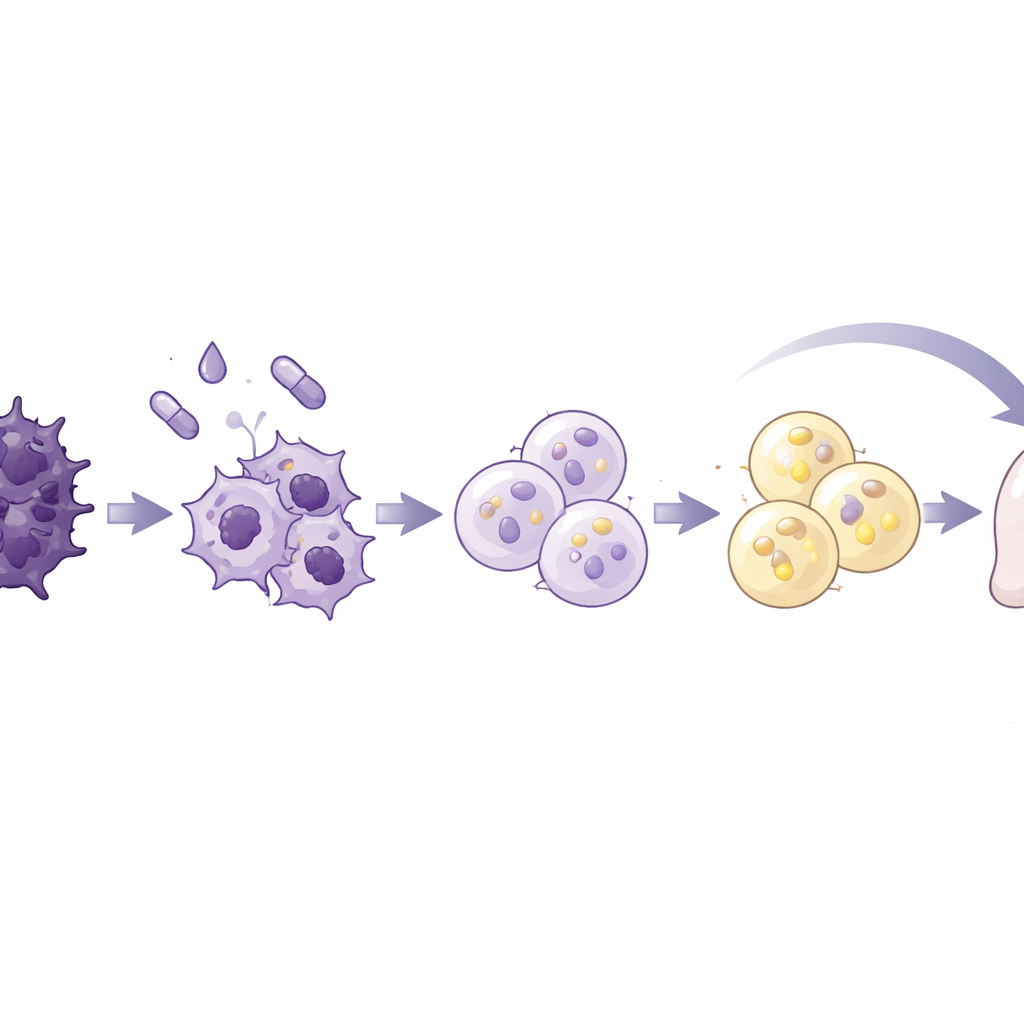
Mettere alla prova la strategia nei topi
I ricercatori si sono chiesti se questa conversione forzata verso uno stato simile al grasso potesse aiutare a controllare i tumori in animali vivi. Hanno impiantato cellule umane di carcinoma pancreatico nel pancreas o nella milza di topi per modellare tumori primari e metastasi epatiche. I topi trattati con rosiglitazone e BMP2 hanno sviluppato tumori pancreatici più piccoli e hanno mostrato goccioline lipidiche più abbondanti e marcatori di cellule adipose all’interno dei tumori, insieme a livelli più bassi di geni associati a EMT e invasione. Nel modello di metastasi, il trattamento non ha modificato il seme iniziale dei tumori, ma col tempo ha rallentato l’espansione del carico tumorale nel fegato rispetto agli animali non trattati. È importante che il tessuto pancreatico normale adiacente non abbia mostrato una convertibilità evidente in cellule adipose, e lo stato simile al grasso nei tumori è persisito per almeno un mese dopo l’interruzione dei farmaci, suggerendo un certo grado di durabilità e specificità.
Cosa potrebbe significare per la cura del cancro in futuro
Questo studio sostiene un concetto provocatorio: per i tumori pancreatici altamente plastici e ricchi di EMT, potrebbe essere possibile «convertire invece di uccidere», reindirizzando le cellule tumorali pericolose e migranti verso cellule stabili, non dividenti e simili agli adipociti che sono meno in grado di diffondersi. Pur essendo lavori a uno stadio iniziale su cellule e modelli murini, e non tutti i tumori pancreatici rispondono allo stesso modo, apre una nuova via terapeutica che agisce cambiando l’identità cellulare invece di limitarsi a bloccare i segnali di crescita. In futuro, tali approcci di transdifferenziazione potrebbero essere combinati con farmaci mirati o immunoterapie per mantenere il cancro del pancreas in uno stato più calmo e gestibile e ridurre il rischio di metastasi letali.
Citazione: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Parole chiave: cancro al pancreas, plasticità cellulare, transdifferenziazione, transizione epitelio-mesenchimale, cellule simili ad adipociti