Clear Sky Science · it
L’inibizione della chinasi correlata a Vaccinia 2 crea una vulnerabilità del metabolismo del glutatione nel cancro pancreatico
Perché è importante per il cancro pancreatico
Il cancro pancreatico è tra i tumori più letali, in parte perché i trattamenti standard spesso non funzionano. Questo studio mette in luce una debolezza nascosta in alcuni tumori pancreatici: la dipendenza da uno “scudo” cellulare contro i prodotti tossici dell’ossigeno. Capire quando questo scudo è fragile, e come un gene tumorale chiamato VRK2 lo rafforza, apre la strada a modi per avvelenare selettivamente le cellule tumorali risparmiando i tessuti sani.
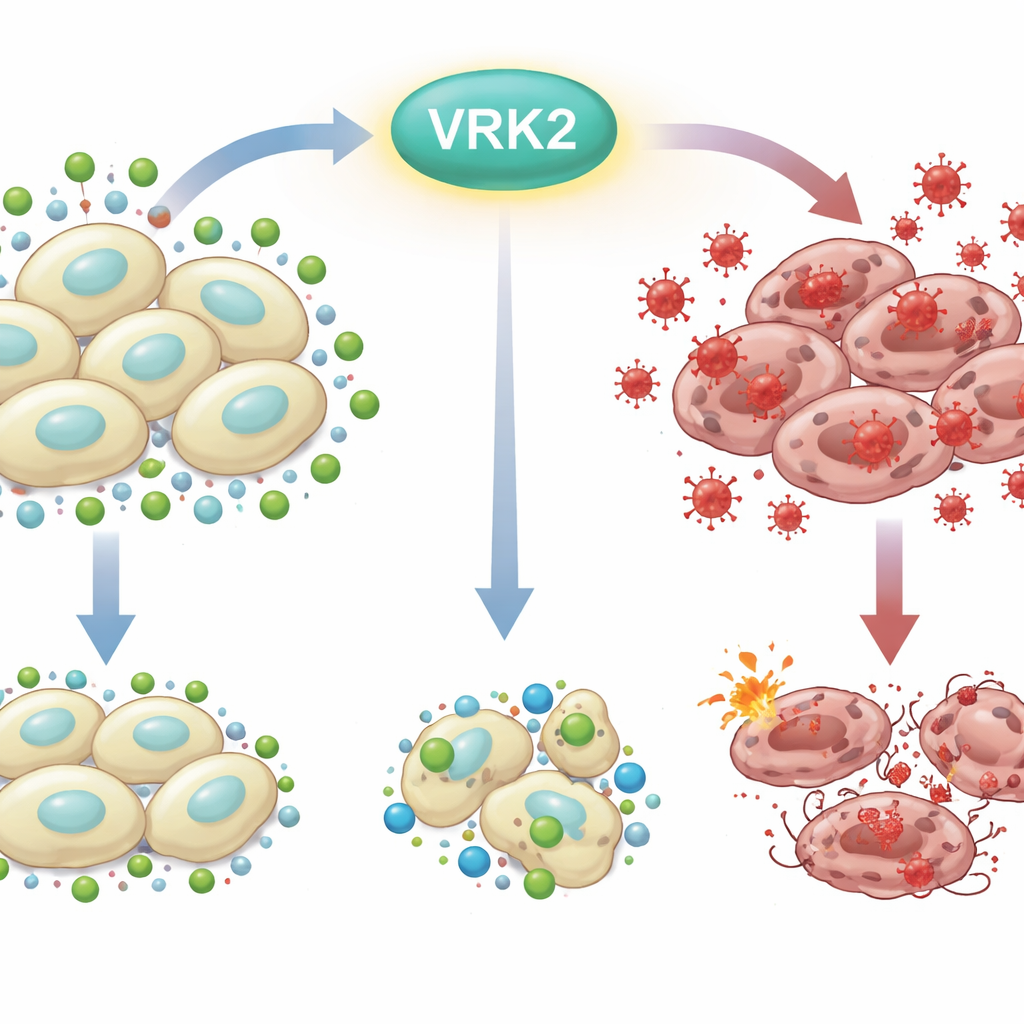
Il problema della ruggine interna
Ogni cellula combatte costantemente una «ruggine dall’interno» causata da specie reattive dell’ossigeno—forme altamente reattive dell’ossigeno che possono danneggiare DNA, lipidi e proteine. Per sopravvivere, le cellule si servono di difese chimiche, con il glutatione che funge da uno degli scudi più importanti. Le cellule del cancro pancreatico, che vivono in condizioni avverse e proliferano rapidamente, fanno ampio ricorso a stratagemmi metabolici per mantenere adeguati livelli di glutatione. Disrupting questo equilibrio tra ossidanti dannosi e antiossidanti protettivi può spingere le cellule tumorali oltre la soglia verso la morte cellulare.
Scoprire un punto debole nascosto
I ricercatori hanno cominciato disattivando VRK2, un gene promotore del cancro precedentemente associato a esiti peggiori nel cancro pancreatico, e poi hanno testato 281 composti che colpiscono il metabolismo. Hanno scoperto che le cellule prive di VRK2 erano sorprendentemente sensibili ai farmaci che bloccano la produzione di glutatione. In queste cellule carenti di VRK2 i livelli di glutatione calavano mentre le specie reattive dell’ossigeno aumentavano, causando la morte cellulare. Fornire antiossidanti supplementari o molecole simili al glutatione le salvava, confermando che la vulnerabilità chiave risiedeva nella loro ridotta capacità di detossificare lo stress ossidativo.
Come VRK2 aiuta le cellule tumorali a proteggersi
Successivamente il team si è chiesto perché VRK2 modifichi il metabolismo del glutatione. Si sono concentrati su una proteina trasportatrice chiamata SLC7A11, che si trova nella membrana esterna della cellula e porta all’interno la cistina, un mattone necessario per sintetizzare il glutatione. Con sorpresa, VRK2 non alterava la quantità complessiva di SLC7A11 prodotta dalla cellula; controllava invece se quel trasportatore raggiungeva con successo la superficie cellulare. Nelle cellule sane con VRK2 attivo, SLC7A11 viaggia dal reticolo endoplasmatico al Golgi e poi alla membrana. VRK2 potenzia questo trafficking modificando chimicamente una proteina di smistamento del carico chiamata Sec24C, che aiuta a caricare SLC7A11 nei vescicole di trasporto. Quando VRK2 è assente o bloccata, SLC7A11 rimane intrappolata all’interno della cellula, meno trasportatori raggiungono la superficie e lo scudo del glutatione si indebolisce.
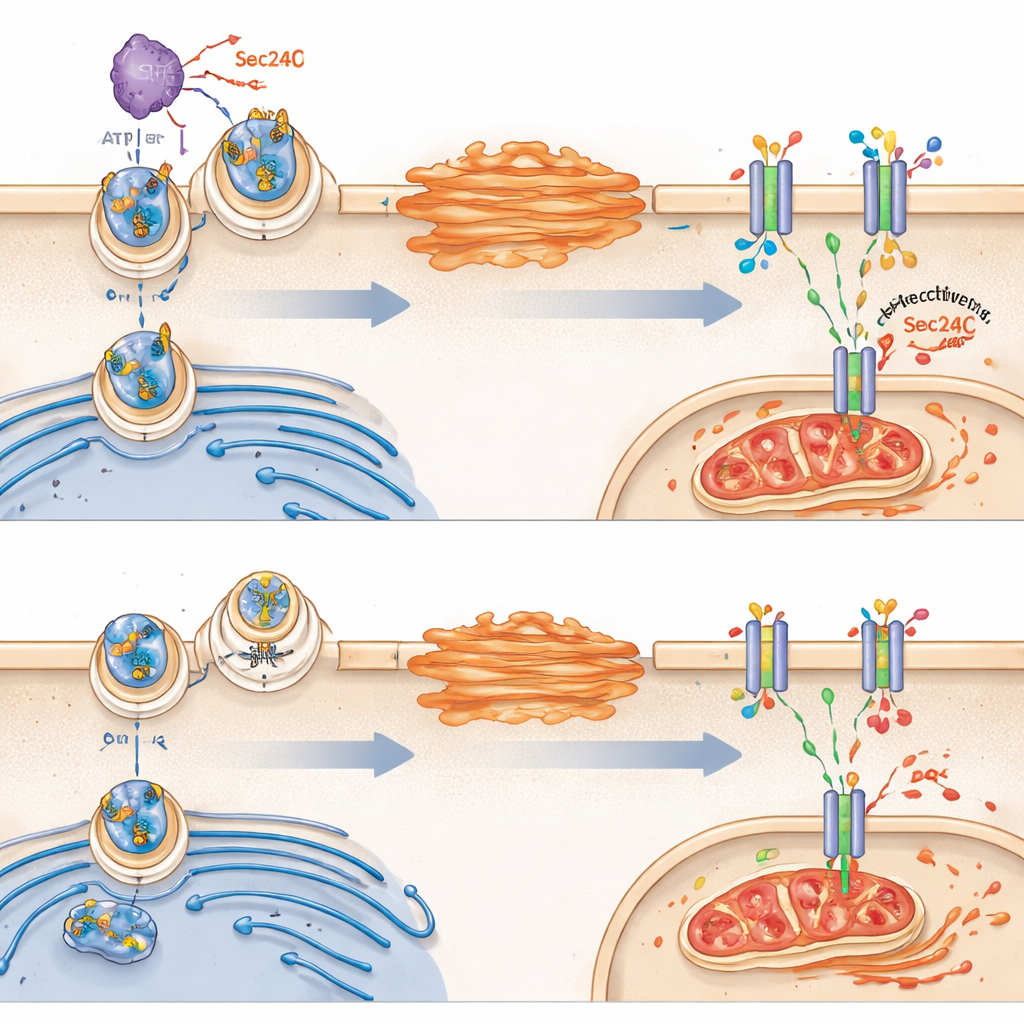
Da scudo rotto a ferroptosi
Senza sufficiente SLC7A11 di membrana, le cellule prive di VRK2 fanno fatica a importare cistina e a mantenere il glutatione. Questo le rende particolarmente vulnerabili a una forma di morte cellulare dipendente dal ferro chiamata ferroptosi, caratterizzata da ossidazione incontrollata dei lipidi di membrana e danno mitocondriale. Lo studio ha mostrato che i farmaci che interrompono la sintesi del glutatione scatenavano segni di ferroptosi nelle cellule carenti di VRK2, compresi mitocondri deformati e accumulo di prodotti di ossidazione lipidica. Bloccare la ferroptosi, ma non altri tipi di morte cellulare, proteggeva queste cellule, sottolineando che il loro tallone d’Achille è l’incapacità di contenere il danno ossidativo.
Orientare le scelte terapeutiche personalizzate
Infine, i ricercatori hanno testato i risultati in modelli animali e in cellule derivate di recente da pazienti. I tumori con bassi livelli di VRK2 si riducevano quando trattati con un farmaco che prende di mira il glutatione, mentre i tumori con alta espressione di VRK2 resistevano in gran parte. Tuttavia, quando ai tumori con VRK2 alto veniva somministrato anche un composto inibitore di VRK2, ritrovavano sensibilità all’inibizione del glutatione. Ciò suggerisce che i livelli di VRK2 possono dividere i pazienti in gruppi: quelli i cui tumori sono naturalmente vulnerabili alla terapia mirata al glutatione e quelli che potrebbero beneficiare di una strategia in due tempi che prima disabiliti VRK2 e poi attacchi il metabolismo del glutatione.
Cosa significa per i pazienti
In parole semplici, questo lavoro mostra che alcuni tumori pancreatici sopravvivono usando VRK2 per mantenere forte il loro scudo antiossidante. Togliere VRK2 assottiglia lo scudo; togliere il glutatione oltre a ciò fa crollare le cellule tumorali sotto lo stress ossidativo. Misurare VRK2 nei tumori potrebbe quindi aiutare i medici a decidere chi è più probabile che benefici di farmaci che interrompono il metabolismo del glutatione e chi potrebbe prima necessitare di un intervento mirato a VRK2. Pur richiedendo ulteriori test clinici, lo studio traccia un percorso chiaro verso terapie più personalizzate e basate sul metabolismo per un tumore che ha un urgente bisogno di opzioni migliori.
Citazione: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Parole chiave: cancro pancreatico, metabolismo del glutatione, VRK2, ferroptosi, SLC7A11