Clear Sky Science · it
Repressione di EGFR dal nuovo biguanide 4C potenzia la sensibilità del cancro ovarico agli inibitori PARP attraverso la down-regulation di BRCA2 e Rad51
Perché questa ricerca è importante
Per molte persone diagnosticate con cancro ovarico, i farmaci mirati attuali funzionano solo per una piccola minoranza i cui tumori presentano difetti genetici specifici. Questo studio esplora un modo per estendere i benefici di una classe importante di medicinali, gli inibitori PARP, a un gruppo molto più ampio di pazienti i cui tumori non hanno quelle mutazioni. Accoppiando un nuovo composto sperimentale con farmaci esistenti, i ricercatori mostrano una strategia per spingere le cellule tumorali in un vicolo cieco letale preservando i tessuti sani.
Un ostacolo nel trattamento attuale del cancro ovarico
Il cancro ovarico viene spesso scoperto in fase avanzata ed è ancora uno dei tumori più letali che colpiscono le donne. Gli inibitori PARP, come l’olaparib, possono essere straordinariamente efficaci, ma principalmente nei pazienti i cui tumori presentano già difetti in una via di riparazione del DNA legata ai geni BRCA1 e BRCA2. La maggior parte dei tumori, tuttavia, mantiene intatta la macchina della riparazione e può correggere i danni al DNA causati da questi farmaci, permettendo alle cellule tumorali di sopravvivere. Una parte chiave di questo apparato di riparazione coinvolge due proteine, BRCA2 e Rad51, che aiutano a ricomporre i filamenti di DNA rotti tramite un processo chiamato ricombinazione omologa. Trovare modi per indebolire selettivamente questa via di riparazione nelle cellule tumorali potrebbe rendere gli inibitori PARP utili per molti più pazienti.
Il ruolo di un noto interruttore di crescita
Il gruppo si è concentrato su una molecola ben nota collegata al cancro, il recettore del fattore di crescita epidermico (EGFR), che si trova sulla superficie di molte cellule tumorali e ne guida la crescita. Hanno scoperto che EGFR fa più che inviare segnali di crescita: nelle cellule di cancro ovarico con geni BRCA normali, livelli elevati di EGFR erano associati a scarsa sopravvivenza dei pazienti e resistenza agli inibitori PARP. Quando EGFR veniva ridotto o spento in colture cellulari e nei topi, i tumori diventavano molto più vulnerabili all’olaparib. I ricercatori hanno dimostrato che EGFR favorisce il trasporto di BRCA2 e Rad51 nel nucleo cellulare dopo danno al DNA, dove possono riparare le rotture e attenuare l’effetto del trattamento. Limitarsi a bloccare l’attività enzimatica di EGFR non era sufficiente; era necessario ridurre la quantità totale della proteina EGFR per compromettere in modo significativo questa via di riparazione.
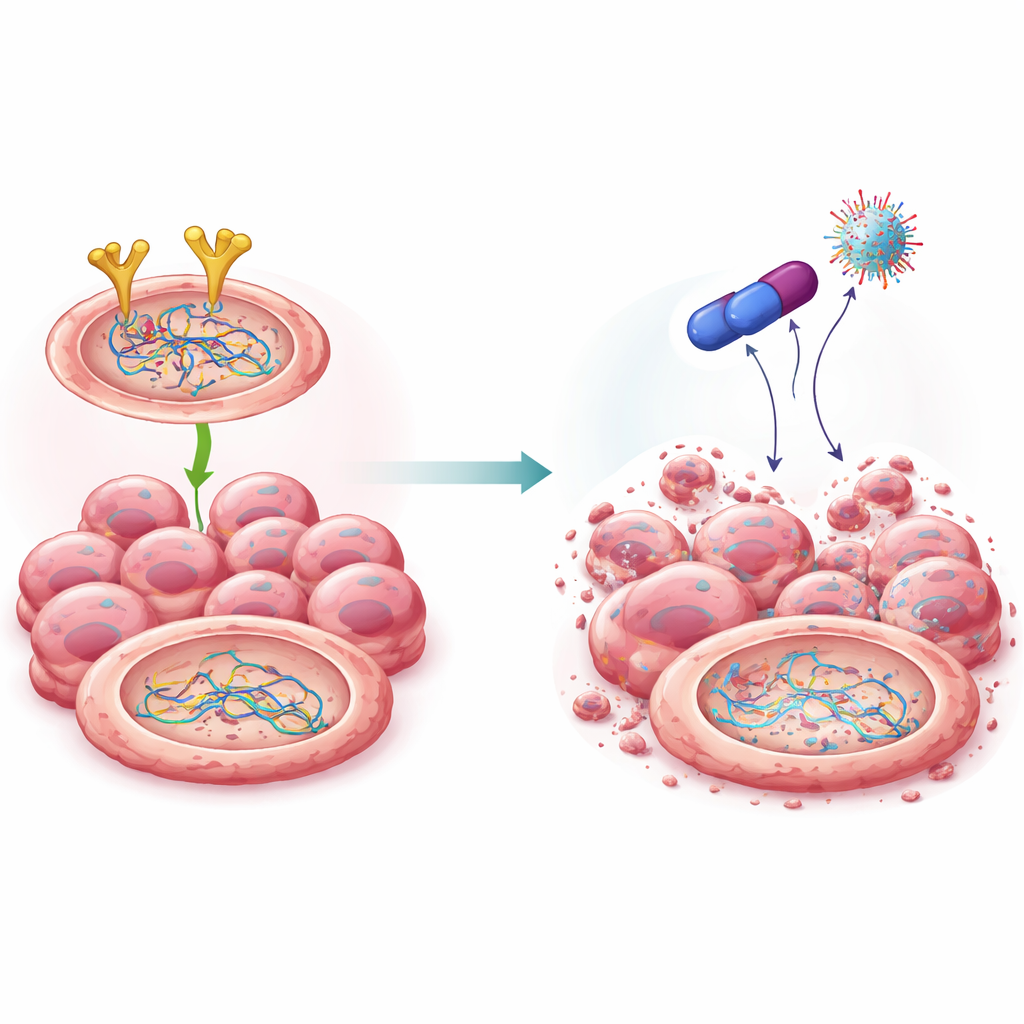
Un nuovo composto che disarma la squadra di riparazione
Sulla scia di lavori precedenti su una famiglia di farmaci nota come biguanidi, gli scienziati hanno sintetizzato diversi parenti chimici e identificato una molecola emergente, chiamata 4C. Questo composto era fortemente tossico per le cellule di cancro ovarico ma relativamente blando sulle cellule normali. Modellizzazione computazionale e test di laboratorio hanno indicato che 4C si lega direttamente a EGFR e ne promuove la degradazione nel sistema cellulare deputato allo smaltimento delle proteine. A differenza di alcuni farmaci EGFR esistenti, 4C riduceva la quantità complessiva di EGFR invece di limitarsi a silenziare la sua attività. Con la diminuzione dei livelli di EGFR, anche la stabilità di BRCA2 e Rad51 calava: venivano etichettate per lo smaltimento, degradate e non erano più in grado di sostenere una riparazione efficiente del DNA. Importante, questa potatura avveniva a livello proteico senza alterare i geni sottostanti.
Bloccare una via di salvataggio all’interno della cellula
Lo studio ha svelato una catena di eventi più dettagliata che collega il danno al DNA alla sopravvivenza tumorale. Dopo che gli inibitori PARP danneggiano il DNA, un’altra proteina sensore chiamata ATM invia un messaggio dal nucleo al corpo cellulare. In risposta, EGFR si associa con BRCA2 e Rad51 e ne facilita il trasferimento nel nucleo, dove riparano il danno. I ricercatori hanno scoperto che una terza proteina, c-Cbl, agisce normalmente come una sorta di etichettatrice per lo smaltimento di BRCA2 e Rad51. EGFR compete con c-Cbl per l’accesso a queste proteine di riparazione, proteggendole dall’essere marcate per la degradazione. Quando 4C riduce i livelli di EGFR, c-Cbl può legarsi più facilmente a BRCA2 e Rad51, portando alla loro etichettatura, degradazione e perdita. Con meno proteine di riparazione nel nucleo, le lesioni del DNA si accumulano e le cellule tumorali diventano molto più sensibili agli inibitori PARP.
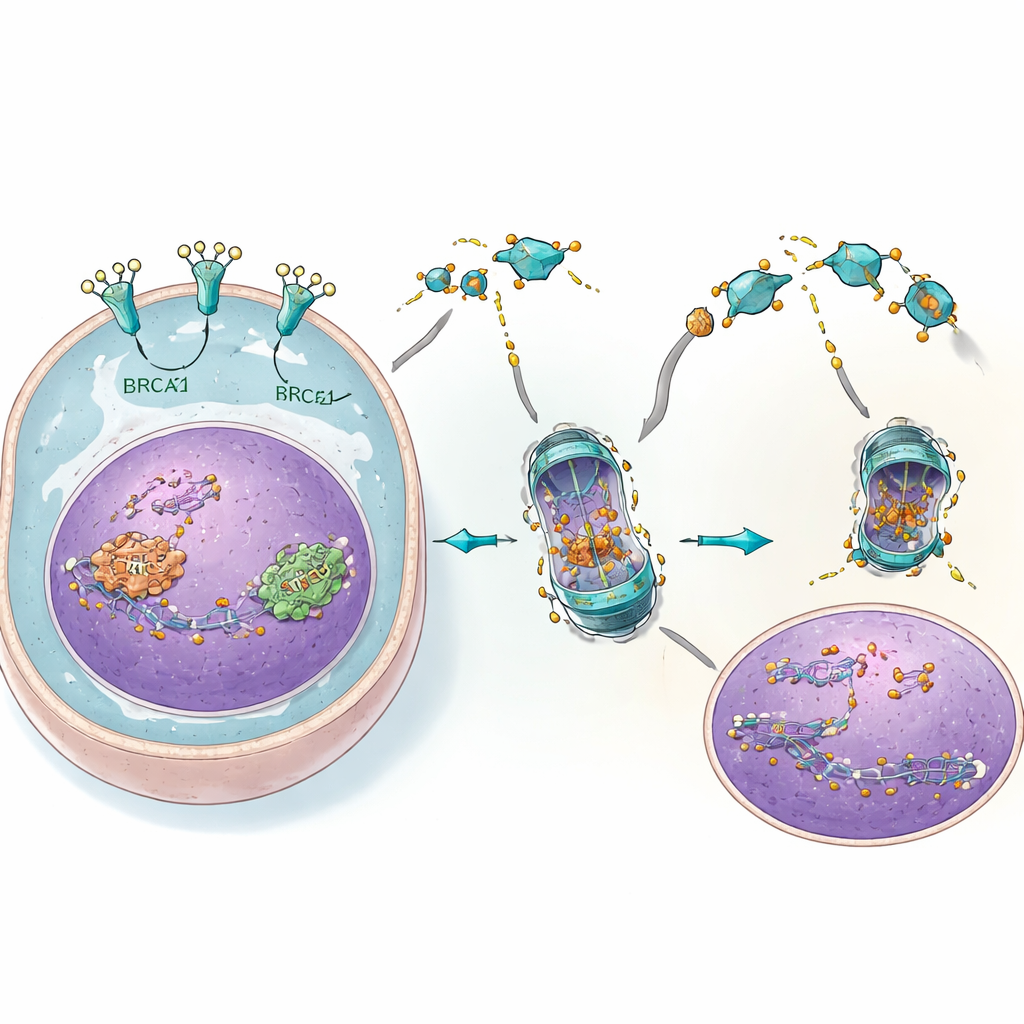
Dalle cellule agli animali: un’accoppiata potente
Sia nelle cellule in coltura sia nei modelli murini, la combinazione di 4C con inibitori PARP ha prodotto un potente colpo combinato. I tumori con geni BRCA normali che resistevano a ciascun farmaco singolarmente si sono ridotti drasticamente o hanno smesso di crescere quando esposti ad entrambi insieme. I marker di danno al DNA aumentavano nettamente, coerentemente con l’idea che la capacità di riparazione fosse stata sopraffatta. Allo stesso tempo, le cellule normali e organi chiave come fegato e reni mostravano poche evidenze di danno, probabilmente perché presentano livelli di EGFR molto più bassi e dipendono meno da questa specifica scorciatoia di riparazione. I benefici della combinazione si estendevano anche alla riduzione della diffusione delle cellule di cancro ovarico nell’organismo.
Cosa potrebbe significare per i pazienti
Questo lavoro propone un modo per trasformare un punto di forza della cellula tumorale in una vulnerabilità. Mirando a EGFR con il nuovo composto 4C, i ricercatori privano della protezione che BRCA2 e Rad51 forniscono, facendo sì che tumori con riparazione del DNA altrimenti normale si comportino più come tumori con mutazioni BRCA nella loro risposta agli inibitori PARP. Questa vulnerabilità indotta, nota come “letalità sintetica”, potrebbe ampliare l’efficacia dei farmaci esistenti a molte più donne con cancro ovarico, mantenendo gestibili gli effetti collaterali. Sebbene 4C sia ancora sperimentale e richieda ampi test in modelli più avanzati e in studi clinici, lo studio offre un quadro chiaro di come smantellare aiutanti specifici della riparazione nelle cellule tumorali potrebbe migliorare gli esiti terapeutici.
Citazione: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Parole chiave: cancro ovarico, inibitori PARP, EGFR, riparazione del DNA, terapia mirata