Clear Sky Science · it
La perdita di PRKACB favorisce la metastasi del carcinoma gastrico di tipo diffuso tramite l'attivazione del segnale RhoA
Perché questo studio è importante per il cancro dello stomaco
Il carcinoma gastrico di tipo diffuso è una forma particolarmente aggressiva di tumore gastrico che spesso si diffonde ampiamente nella cavità addominale, rendendolo difficile da trattare e spesso letale. Questo studio indaga perché questi tumori siano così inclini alla diffusione, rivelando un meccanismo molecolare di freno che normalmente limita la migrazione delle cellule tumorali—e mostrando cosa succede quando quel freno viene meno. Capire questo interruttore di controllo nascosto potrebbe aprire nuove strade per prevedere quali pazienti sono a maggior rischio e per sviluppare farmaci che rallentino o arrestino la diffusione pericolosa.
Una forma pericolosa di cancro gastrico
Non tutti i tumori gastrici si comportano allo stesso modo. I tumori di tipo intestinale tendono a formare masse più strutturate, mentre il carcinoma gastrico di tipo diffuso (DGC) è costituito da cellule sparse che si staccano facilmente dal tumore primario. I pazienti con DGC hanno un rischio di morte maggiore rispetto a quelli con la forma intestinale, in parte perché i loro tumori seminano più facilmente nuove lesioni nella cavità addominale. Studi genetici precedenti avevano già collegato il DGC a variazioni ricorrenti in un gene chiamato RHOA, che influenza come le cellule si muovono e cambiano forma. Ma rimaneva poco chiaro come tali variazioni si connettessero alle reti di segnalazione più ampie che determinano se le cellule tumorali restano al loro posto o migrano.
Trovare un freno mancante nei campioni tumorali
I ricercatori si sono concentrati su una proteina chiamata PRKACB, una subunità catalitica della nota enzima protein-chinasi A, che regola molti comportamenti cellulari aggiungendo gruppi fosfato ad altre proteine. Un’indagine proteomica precedente aveva suggerito che i livelli di PRKACB erano insolitamente bassi nei DGC aggressivi. Per verificarlo, il team ha esaminato campioni tumorali di 376 pazienti, confrontando i carcinomi di tipo diffuso e di tipo intestinale e i tessuti non cancerosi circostanti. Hanno riscontrato che i livelli di PRKACB erano marcatamente ridotti nei tumori di tipo diffuso, soprattutto negli stadi avanzati, ma non nei tumori di tipo intestinale. I pazienti i cui tumori presentavano scarsi livelli di PRKACB avevano una sopravvivenza complessiva significativamente peggiore, anche tenendo conto di altri fattori clinici, suggerendo che PRKACB funzioni come oncosoppressore in questo contesto.
Come il basso PRKACB alimenta la fuga cellulare
Per capire cosa faccia PRKACB all’interno delle cellule tumorali, il team ha usato linee cellulari in coltura che riproducono il carcinoma gastrico di tipo diffuso. Quando hanno ridotto artificialmente PRKACB, le cellule sono diventate più mobili e invasive nei test di laboratorio, attraversando più facilmente barriere e formando proiezioni simili a dita chiamate pseudopodi che aiutano le cellule a strisciare. Queste cellule hanno anche cambiato stato, passando da un profilo più ordinato ed epiteliale verso uno più lasso e di tipo mesenchimale associato alla metastasi, perdendo la molecola di adesione E‑cadherina che normalmente mantiene le cellule unite. Al contrario, aumentare i livelli di PRKACB rendeva le cellule meno migratorie e meno invasive. È importante sottolineare che questi cambiamenti non alteravano la velocità di proliferazione cellulare, indicando un ruolo specifico di PRKACB nella diffusione, non nella crescita.
Un approfondimento sull’interruttore di segnalazione RhoA
I ricercatori hanno quindi indagato come PRKACB eserciti questo effetto anti-metastatico. Utilizzando metodi di interazione proteina–proteina e modellazione strutturale, hanno mostrato che PRKACB si lega direttamente a RhoA, un interruttore molecolare che alterna forme inattive e attive per governare forma e movimento cellulare. PRKACB aggiunge un gruppo fosfato in una posizione specifica su RhoA (serina 188), che inattiva RhoA e attenua le vie a valle ROCK e FAK che guidano il riorganizzazione del citoscheletro e la motilità cellulare. Quando PRKACB veniva silenziato, RhoA risultava meno fosforilato, più attivo, e la segnalazione ROCK/FAK si intensificava, portando a un movimento cellulare più aggressivo. In modelli murini in cui tumori simili a quelli umani venivano impiantati nella parete gastrica, la diminuzione di PRKACB causava più noduli metastatici e più grandi nell’addome e un’insorgenza più precoce della diffusione visibile, ancora una volta senza cambiare la velocità di crescita delle metastasi già stabilite.
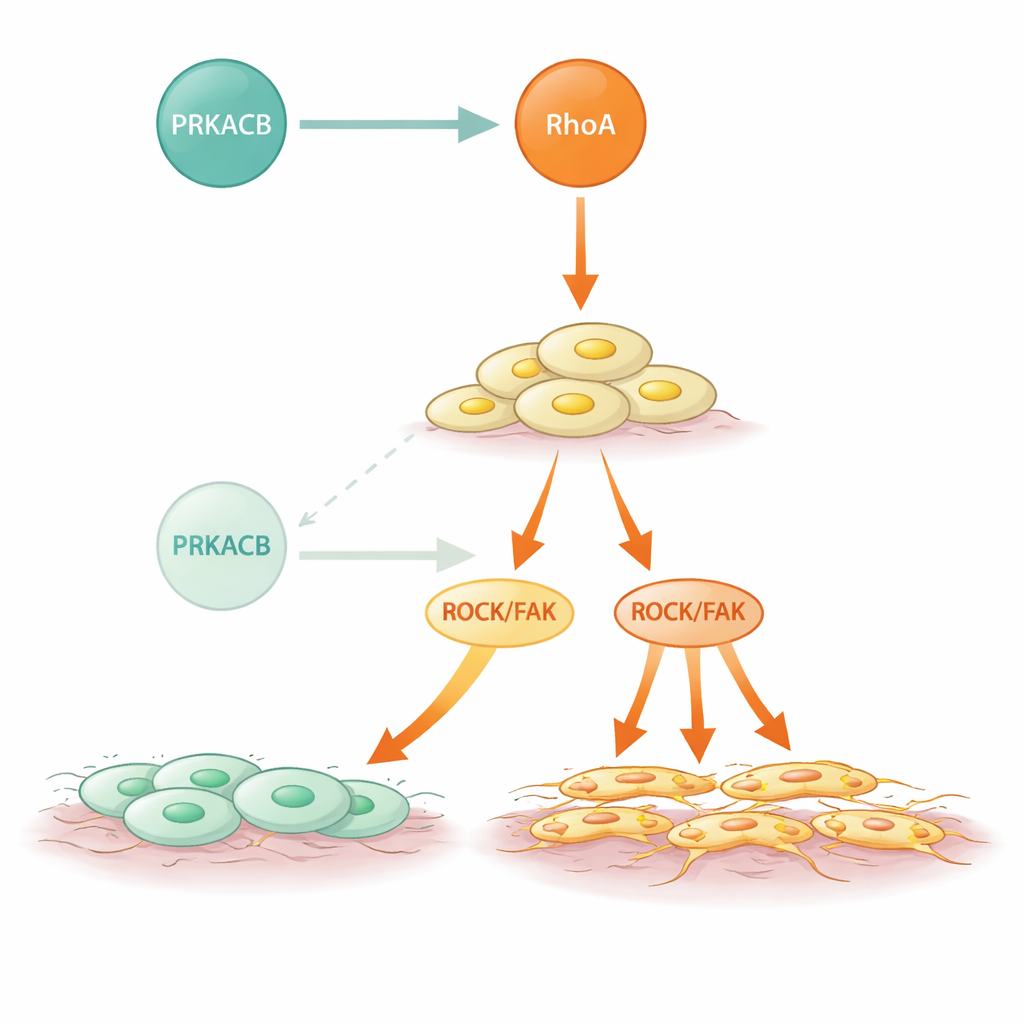
Segnalazione mutata e una possibile via d’intervento
I carcinomi gastrici di tipo diffuso spesso presentano mutazioni di RHOA, e questo studio mostra come alcune di quelle variazioni aggravino il problema. Diverse mutazioni ricorrenti associate al DGC in RhoA indebolivano o abolivano il suo legame con PRKACB, ma non compromettevano la capacità di RhoA di attivare i suoi effettori a valle. Di conseguenza, queste forme mutanti eludevano la fosforilazione restrittiva da parte di PRKACB e mostravano un’attività ROCK aumentata e un comportamento invasivo più marcato. Colpisce che, quando i ricercatori hanno trattato cellule e topi con un composto inibitore di RhoA, l’aumento di metastasi causato dalla bassa PRKACB è stato in gran parte invertito. Questo suggerisce che, anche nei tumori in cui il freno naturale è debole o assente, mirare direttamente la via RhoA iperattiva potrebbe ridurre la diffusione.
Cosa significa per i pazienti e le terapie future
In termini semplici, questo lavoro identifica PRKACB come una componente chiave di un circuito interno “anti-migrazione” nel carcinoma gastrico di tipo diffuso. Quando i livelli di PRKACB calano, o quando RhoA è mutato in modo che PRKACB non possa legarsi e modificarlo, la segnalazione RhoA si surriscalda e le cellule tumorali diventano più abili a staccarsi e colonizzare la cavità addominale. Misurare lo stato di PRKACB e RhoA nei tumori potrebbe aiutare i medici a valutare la probabilità che il cancro di un paziente metastatizzi e chi potrebbe trarre maggior beneficio da farmaci che inibiscono la via RhoA–ROCK–FAK. Sebbene tali trattamenti richiederanno ulteriori sviluppi e test clinici, lo studio traccia una chiara rotta molecolare da un freno mancante alla diffusione mortale—e indica nuove modalità per rallentare quel percorso.
Citazione: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Parole chiave: carcinoma gastrico di tipo diffuso, metastasi, PRKACB, segnalazione RhoA, via ROCK FAK