Clear Sky Science · it
O-GlcNAcilazione di YAP1 promuove il danno da ischemia‑riperfusione nei trapianti polmonari tramite legame al fattore di trascrizione HIF1α e attivazione di autophagia e mitofagia
Perché questo conta per i pazienti sottoposti a trapianto polmonare
Il trapianto polmonare può offrire una seconda possibilità di vita alle persone con malattie polmonari gravi, ma il polmone appena trapiantato spesso subisce un’ondata di danno quando il flusso sanguigno viene interrotto e poi ripristinato. Il cosiddetto danno da ischemia‑riperfusione può lasciare i pazienti con polmoni fragili, ricoveri prolungati in terapia intensiva e esiti a lungo termine peggiori. Lo studio alla base di questo articolo svela una catena molecolare nascosta nelle cellule polmonari che contribuisce a guidare questo danno precoce, indicando nuovi bersagli farmacologici che un giorno potrebbero rendere i trapianti polmonari più sicuri e con maggior successo.
Una reazione a catena innescata dalla perdita di ossigeno
Durante un trapianto, il polmone donatore è temporaneamente privato di sangue e ossigeno, per poi essere di nuovo esposto quando viene collegato alla circolazione del ricevente. I ricercatori hanno modellato questo arresto‑ripresa dell’apporto di ossigeno in colture di cellule polmonari e dell’endotelio vascolare in laboratorio e in un sistema di trapianto polmonare nel ratto. Hanno osservato che questo stress attivava fortemente un sistema di controllo della crescita e della sopravvivenza intracellulare noto come via Hippo–YAP. Quando attivata, la proteina YAP1 si sposta nel nucleo e si associa ad altri fattori per attivare o disattivare numerosi geni. In questo studio, l’ipossia seguita da riossigenazione ha aumentato notevolmente l’attività di YAP1 e dei suoi geni partner, e questo aumento era strettamente legato alla morte cellulare e al rilascio di molecole infiammatorie che possono infiammare e indebolire il polmone trapiantato.
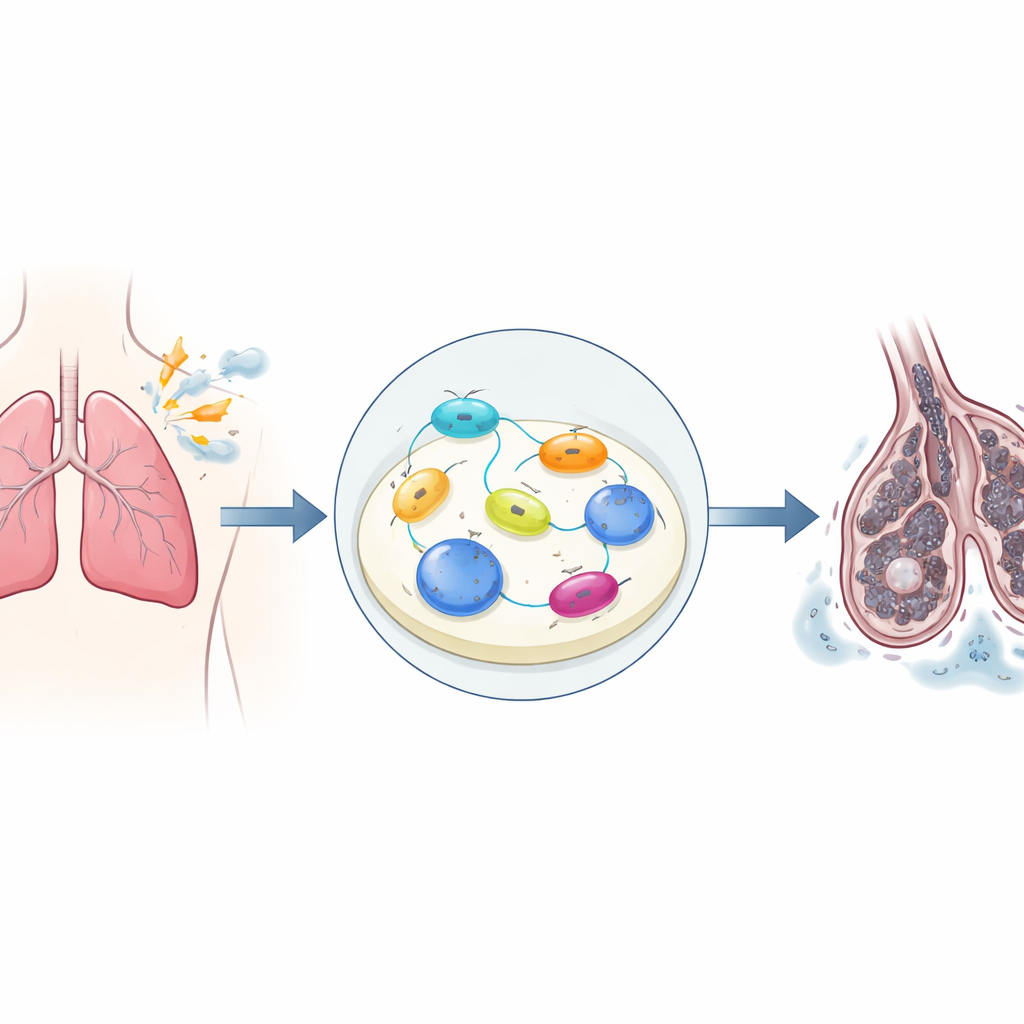
Il “self‑cleaning” che diventa eccessivo
Le cellule si affidano a un sistema interno di “autopulizia” noto come autofagia per degradare e riciclare componenti usurati, e a una versione più mirata, la mitofagia, per eliminare i mitocondri danneggiati, i piccoli impianti energetici della cellula. In quantità moderate, questi processi aiutano le cellule a far fronte allo stress. Qui invece il team ha rilevato che dopo il taglio e il ripristino dell’ossigeno sia autofagia che mitofagia erano fortemente aumentate nelle cellule polmonari e nei polmoni trapiantati. Al microscopio si osservava un maggior numero di vescicole di riciclo e segni di mitocondri avvolti e digeriti. Contemporaneamente, gli animali mostravano edema e danno strutturale nel tessuto polmonare, insieme a un aumento delle cellule che andavano incontro a morte programmata. Questo suggerisce che, nel contesto del trapianto, il meccanismo di autopulizia viene spinto in sovra‑attivazione e inizia a contribuire al danno anziché proteggerlo.
Un’etichetta zuccherina che modifica il comportamento delle proteine
I ricercatori si sono poi chiesti perché YAP1 diventasse così dannoso in queste condizioni. Si sono concentrati su una piccola etichetta a base di zucchero chiamata O‑GlcNAc che può essere aggiunta a molte proteine e ne modifica il comportamento. Questa etichetta è applicata da un enzima chiamato OGT. Hanno scoperto che la privazione e il ripristino dell’ossigeno aumentavano sia l’O‑GlcNAc globale nelle cellule sia, in modo più specifico, l’O‑GlcNAc su YAP1. Quando YAP1 portava questa modificazione zuccherina, si legava più saldamente a un altro importante sensore dell’ossigeno, HIF1α, che normalmente aiuta le cellule ad adattarsi alla carenza di ossigeno attivando geni protettivi. Attraverso test biochimici, il gruppo ha mostrato che YAP1 modificato attirava HIF1α su tratti di DNA che controllano geni coinvolti nell’autofagia e nella mitofagia, potenziandone l’attività e amplificando ulteriormente le risposte di riciclo e di stress della cellula.
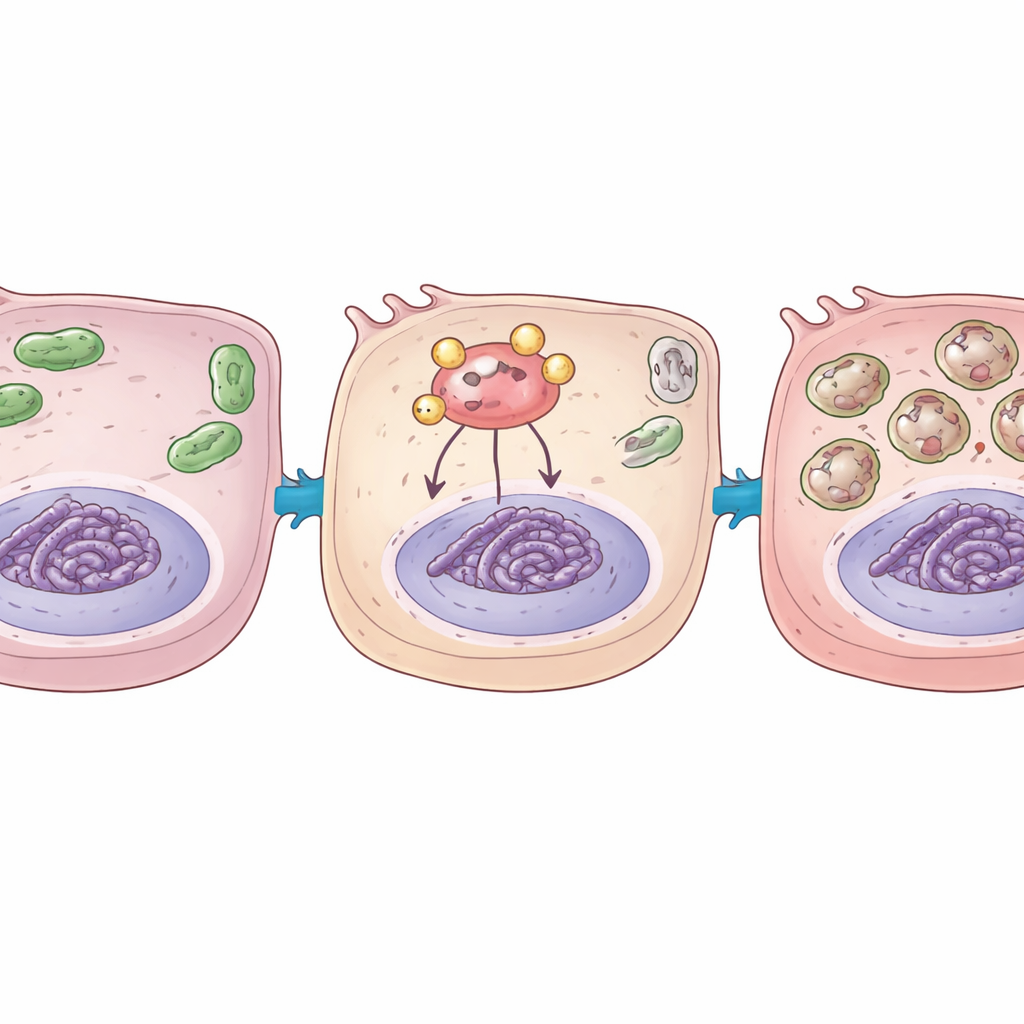
Spegnere il ciclo dannoso
Per verificare se questa via potesse essere domata, i ricercatori hanno usato strumenti genetici per ridurre l’espressione di YAP1 o di OGT, l’enzima che aggiunge l’etichetta zuccherina. Nei modelli cellulari, la riduzione di YAP1 ha attenuato l’attivazione della via di stress, ridotto l’eccessiva autofagia e mitofagia e diminuito la morte cellulare dopo il ripristino dell’ossigeno. Nei polmoni trapiantati di ratto, l’abbattimento di YAP1 o di OGT ha ridotto l’edema tissutale, abbassato i marcatori di autodigestione e di degrado mitocondriale e diminuito il numero di cellule in morte programmata. È importante notare che il blocco di OGT ha anche ridotto l’etichettatura zuccherina di YAP1 e la sua capacità di reclutare HIF1α sui geni correlati all’autofagia, indebolendo direttamente il ciclo dannoso scoperto dal gruppo.
Cosa significa per i trapianti futuri
Nel complesso, lo studio mostra che una piccola modifica chimica sulla proteina YAP1 può trasformare una normale rete di risposta allo stress in un motore di danno polmonare dopo il trapianto. Facendo sì che YAP1 si leghi con maggiore forza al sensore di ossigeno HIF1α e innalzi l’autodigestione cellulare oltre livelli salutari, questa etichetta favorisce edema, danno strutturale e perdita cellulare nel polmone nuovo. I risultati suggeriscono che farmaci volti ad attenuare l’attività di YAP1, a bloccarne l’etichettatura zuccherina da parte di OGT o a modulare con cautela autofagia e mitofagia potrebbero offrire nuove strategie per proteggere i polmoni trapiantati dal danno precoce, migliorando sia la sopravvivenza sia la qualità di vita dei riceventi.
Citazione: Dai, S., Wan, X., Xia, L. et al. O-GlcNAcylation of YAP1 promotes lung transplant ischemia-reperfusion injury via binding to HIF1α transcription factor and activating autophagy and mitophagy. Cell Death Dis 17, 311 (2026). https://doi.org/10.1038/s41419-026-08548-w
Parole chiave: trapianto polmonare, danno da ischemia‑riperfusone, YAP1, autofagia, mitofagia