Clear Sky Science · it
L’asse RNA non codificante lungo ADEI/miR-93-3p/STAT3 promuove la progressione e l’evasione immunitaria del linfoma diffuso a grandi cellule B positivo per virus di Epstein–Barr regolando il checkpoint PD-1/PD-L1
Perché questo conta per le nostre difese immunitarie
Alcuni linfomi legati al comune virus di Epstein–Barr (EBV) sono particolarmente difficili da trattare e spesso eludono le difese immunitarie dell’organismo. Questo studio svela un sistema di comunicazione nascosto all’interno di questi tumori: piccole bolle chiamate esosomi che trasportano una lunga molecola di RNA che aiuta i tumori a crescere e a nascondersi dalle cellule immunitarie. Comprendere questa conversazione occulta potrebbe aprire nuove vie per diagnosticare e trattare questi ostinati tumori del sangue.
Un virus che sbilancia l’equilibrio
Il linfoma diffuso a grandi cellule B (DLBCL) è il linfoma aggressivo più comune. Quando le cellule tumorali sono infettate da EBV, i pazienti tendono a rispondere peggio alla chemioterapia-immunoterapia standard. I ricercatori hanno prima confrontato in laboratorio cellule linfomatose EBV-positive e EBV-negative. Hanno scoperto che l’infezione da EBV rendeva le cellule linfomatose più rapide nella divisione, più produttive nel formare colonie e capaci di dare origine a tumori più grandi nei topi. Le cellule EBV-positive mostravano anche una maggiore presenza sulla superficie di una molecola chiamata PD-L1, che interagisce con PD-1 sulle cellule immunitarie per spegnere il loro attacco. Quando il gruppo ha messo in contatto le cellule linfomatose con i linfociti CD8 citotossici, i tumori EBV-positive riducevano il numero e la potenza di queste cellule T, un effetto che poteva essere invertito con anticorpi che bloccano il freno PD-1/PD-L1.
Un lungo RNA che aiuta i tumori a crescere e a nascondersi
Per capire come EBV rimodella il comportamento tumorale, il gruppo ha esaminato gli RNA non codificanti lunghi—tratti di RNA che non codificano proteine ma possono regolare molti processi cellulari. Analizzando il contenuto di RNA degli esosomi rilasciati da cellule DLBCL EBV-positive e EBV-negative, hanno identificato un RNA precedentemente non caratterizzato, che hanno chiamato lncADEI, fortemente aumentato nelle cellule EBV-positive e nei loro esosomi. Forzando le cellule linfomatose a produrre più lncADEI, le cellule proliferavano più rapidamente, formavano più colonie e resistevano alla morte cellulare programmata. Ridurre lncADEI aveva l’effetto opposto, rallentando la crescita e aumentando la morte cellulare sia in colture che in modelli tumorali murini.
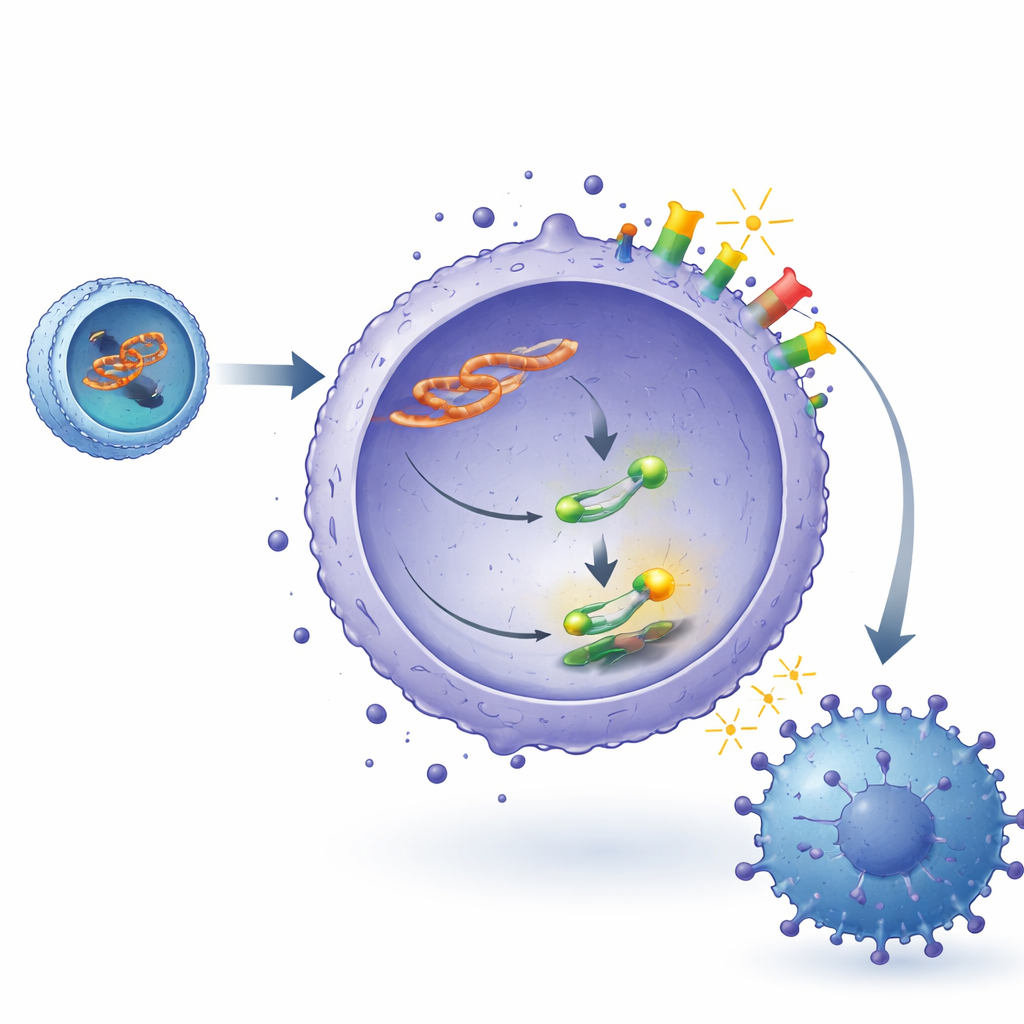
Come lncADEI riprogramma l’evasione immunitaria
I ricercatori hanno poi tracciato come lncADEI si collega al checkpoint immunitario PD-1/PD-L1. All’interno delle cellule linfomatose, lncADEI si localizza prevalentemente nel citoplasma, dove agisce come una spugna per un piccolo RNA regolatorio chiamato miR-93-3p. In condizioni normali, miR-93-3p contribuisce a tenere sotto controllo una proteina di segnalazione chiave, STAT3, legandosi al suo messaggio e limitandone la produzione. Quando lncADEI sequestra miR-93-3p, viene prodotta e attivata più STAT3. STAT3, a sua volta, si lega direttamente alla regione di controllo del gene PD-L1 nelle cellule linfomatose e aumenta la produzione di PD-L1. Questa catena—lncADEI che blocca miR-93-3p, libera STAT3 e aumenta PD-L1—si traduce in livelli più alti di PD-L1 sulle cellule tumorali, segnali di spegnimento più forti verso i linfociti CD8 e una ridotta attività delle cellule T.
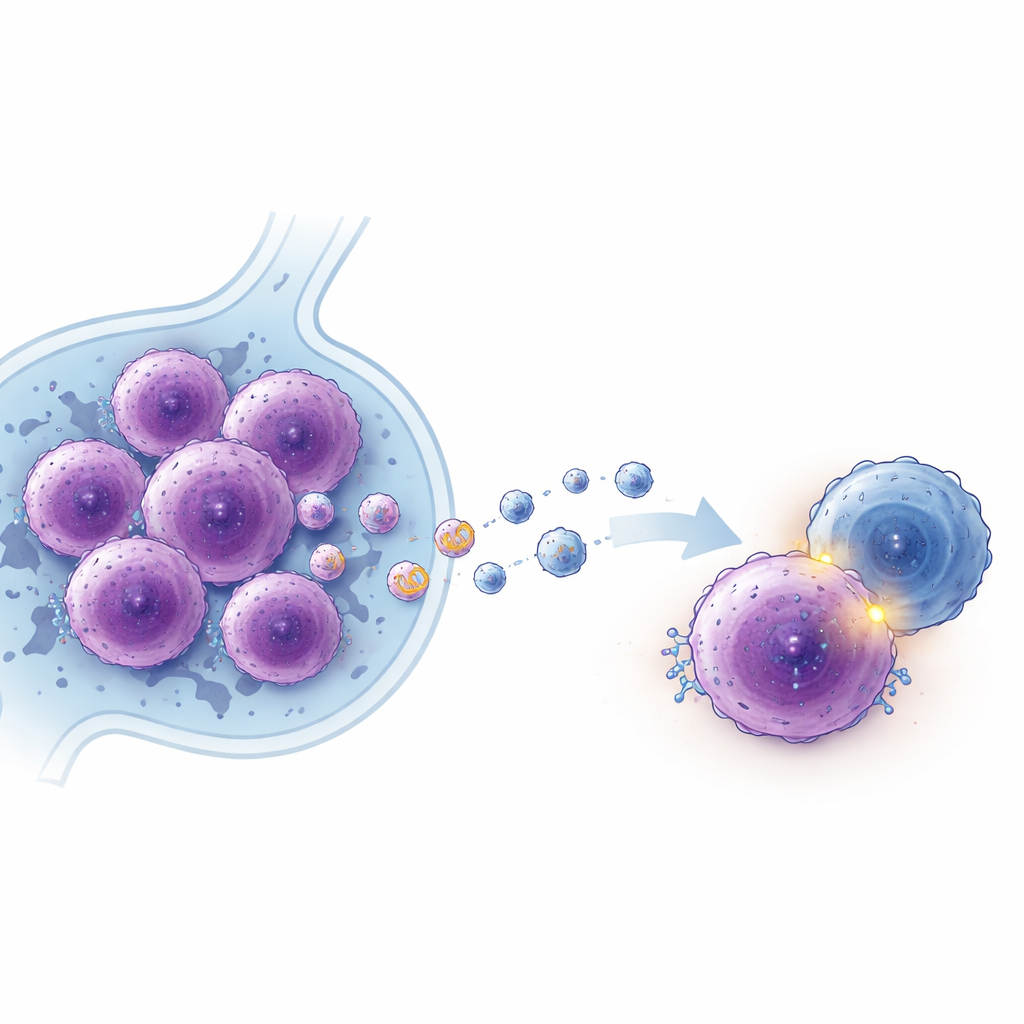
La “posta” esosomiale che diffonde istruzioni dannose
Le cellule linfomatose EBV-positive non si tengono lncADEI per sé. Secernono molti più esosomi rispetto alle cellule EBV-negative, e questi esosomi sono ricchi di lncADEI. Quando cellule linfomatose EBV-negative venivano esposte a esosomi provenienti da cellule EBV-positive, li incorporavano, i loro livelli interni di lncADEI aumentavano e cominciavano a comportarsi in modo più aggressivo—dividendosi più rapidamente e formando più colonie. In colture miste che includevano cellule T, esosomi arricchiti in lncADEI riducevano il numero e la capacità citotossica dei linfociti CD8 e aumentavano PD-1 su queste cellule immunitarie, indebolendo ulteriormente la risposta immunitaria. Ciò suggerisce che i tumori EBV-positive possono “istruire” le cellule tumorali vicine e rimodellare l’ambiente circostante attraverso esosomi ricchi di lncADEI.
Indizi dai campioni di sangue dei pazienti
Per collegare questi riscontri di laboratorio alla malattia reale, il gruppo ha misurato lncADEI negli esosomi plasmatici di 47 pazienti con DLBCL. I pazienti con tumori EBV-positive avevano livelli significativamente più elevati di lncADEI esosomiale rispetto ai pazienti EBV-negative. Elevati livelli di lncADEI nel sangue erano inoltre associati a stadio di malattia più avanzato, a sottotipo tumorale più aggressivo, a punteggi di rischio standard più alti e a marcatori aumentati di danno tissutale. Questi schemi suggeriscono che lncADEI esosomiale nel sangue potrebbe servire come indicatore minimamente invasivo di linfoma guidato da EBV e della sua gravità.
Cosa significa questo per le cure future
In termini pratici, questo lavoro rivela un trucco in tre step usato dai linfomi legati a EBV: sovraprodurre un lungo RNA (lncADEI), imballarlo in bolle viaggianti e usarlo sia all’interno del tumore sia nelle cellule vicine per aumentare un noto freno immunitario, PD-L1. Il risultato è una crescita tumorale più rapida e un attacco delle cellule T attenuato. Poiché ogni passaggio di questa catena—lo stesso lncADEI, la sua interazione con miR-93-3p e STAT3, e il rilascio di esosomi ricchi di lncADEI—offre un potenziale punto di intervento o di misurazione, lo studio indica nuove strategie per migliorare l’immunoterapia e monitorare i linfomi associati a EBV tramite un semplice esame del sangue.
Citazione: Zheng, W., Lai, G., Liao, Z. et al. Long noncoding RNA ADEI/miR-93-3p/STAT3 axis promotes Epstein–Barr virus-positive diffuse large B-cell lymphoma progression and immune evasion through regulating the PD-1/PD-L1 checkpoint. Cell Death Dis 17, 280 (2026). https://doi.org/10.1038/s41419-026-08532-4
Parole chiave: linfoma da virus di Epstein–Barr, checkpoint immunitario, RNA non codificante lungo, esosomi, segnalazione STAT3