Clear Sky Science · it
La miosina nucleare 1 collega l’architettura genomica al rimodellamento del tessuto adiposo, all’infiammazione metabolica e all’obesità nei topi
Perché lo scheletro della cellula conta per il grasso corporeo
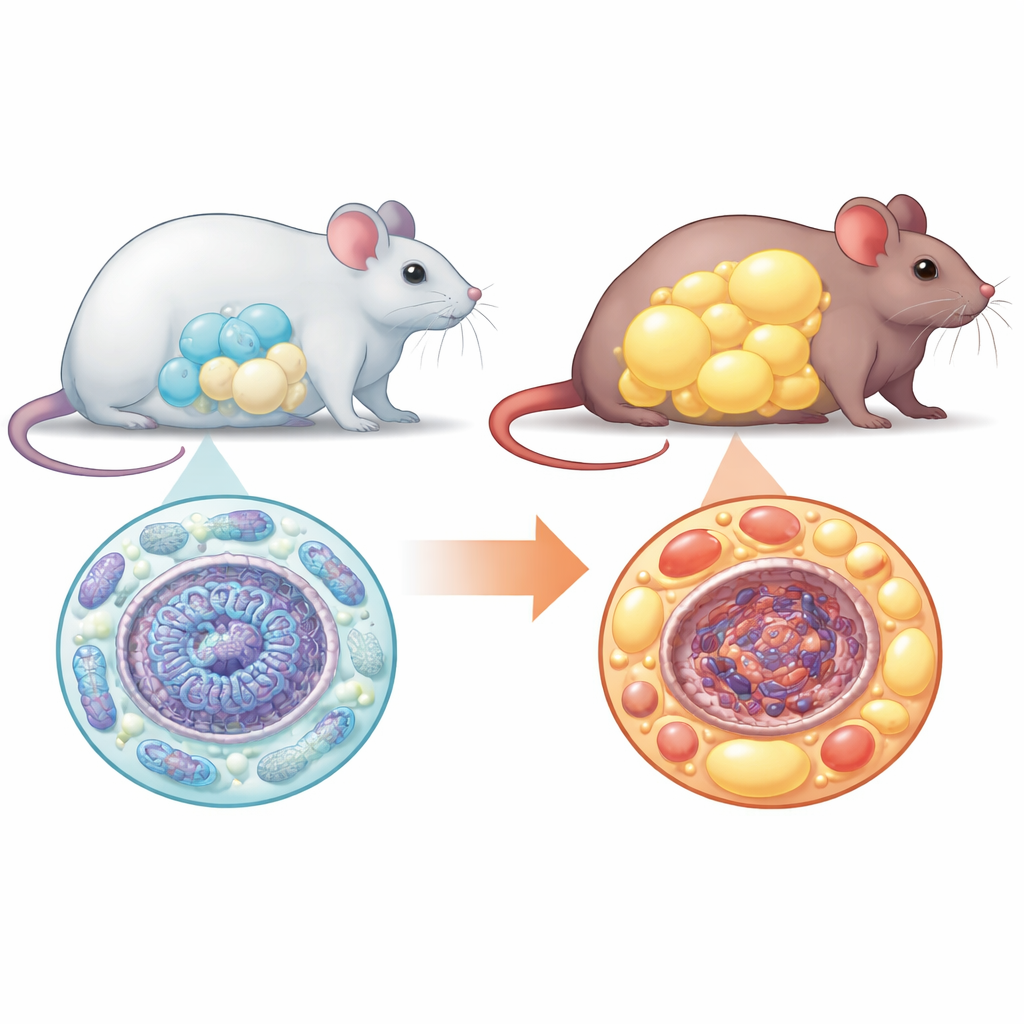
L’obesità viene spesso attribuita a ciò che mangiamo e a quanto ci muoviamo, ma in profondità nelle nostre cellule anche il modo in cui il DNA è impacchettato e letto può inclinare la bilancia. Questo studio rivela che una piccola proteina motrice, la miosina nucleare 1 (NM1), che contribuisce a organizzare il DNA nel nucleo cellulare, gioca un ruolo sorprendente nel modo in cui le cellule adipose si formano, immagazzinano energia e innescano l’infiammazione. Studiando topi privi di questa proteina, i ricercatori hanno scoperto un collegamento diretto tra l’architettura fisica del nostro patrimonio genetico e lo sviluppo di grasso viscerale patologico e problemi metabolici.
Dalle cellule staminali alle cellule adipose
Le cellule adipose si sviluppano da precursori versatili chiamati cellule staminali mesenchimali. Normalmente questi precursori si moltiplicano, cambiano il loro uso energetico e maturano in molte piccole cellule adipose ben funzionanti che immagazzinano in sicurezza le calorie in eccesso. Il gruppo ha scoperto che senza NM1 questo processo ordinato si rompe. Coltivando in laboratorio cellule staminali provenienti da topi normali e privi di NM1 e indolandole a differenziarsi in adipociti, molto meno cellule completavano la transizione in assenza di NM1. Le cellule che maturavano erano visibilmente più grandi del normale, piene di lipidi ma prive delle caratteristiche geniche e proteiche tipiche di adipociti sani. Questo schema — meno cellule ma ciascuna ingrandita — è un segno distintivo di tessuto adiposo malsano.
Come l’impacchettamento dei geni modella il comportamento degli adipociti
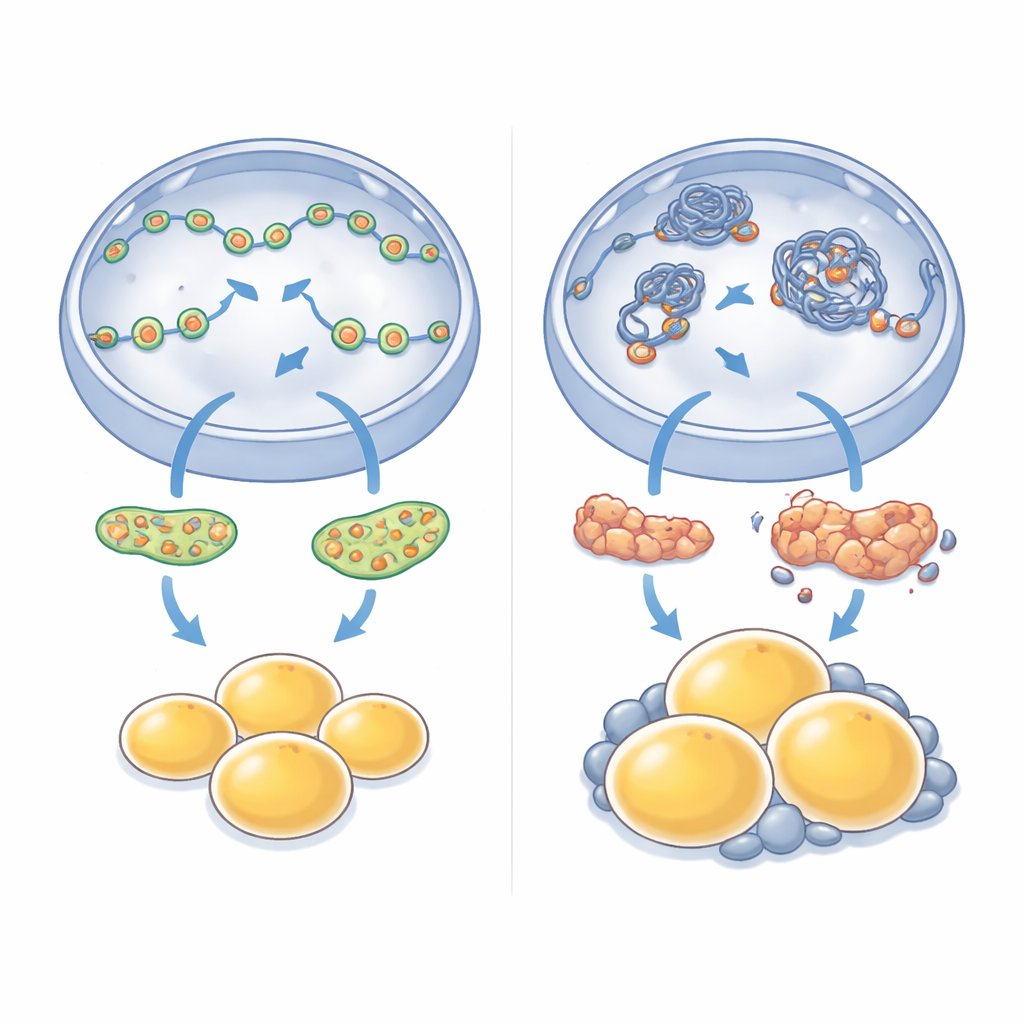
NM1 agisce nel nucleo, dove contribuisce a mantenere tratti di DNA accessibili affinché geni importanti possano essere attivati. Per capire come la sua perdita modifichi il comportamento cellulare, i ricercatori hanno sovrapposto mappe di regioni di DNA aperto con misure dell’attività genica in cellule con e senza NM1. Hanno osservato che molti geni necessari per la formazione degli adipociti, la gestione delle gocce lipidiche e la manutenzione dei mitocondri hanno perso sia accessibilità sia attività quando NM1 mancava. Allo stesso tempo, altri geni legati a percorsi di crescita e segnalazione sono diventati più aperti e più attivi. Ciò indica NM1 come un controllore del traffico: aiuta a mantenere un equilibrio tra regioni di DNA aperte e chiuse affinché le reti geniche appropriate guidino uno sviluppo adipocitario sano e il metabolismo.
Quando i cambiamenti locali diventano aumento di peso sistemico
Le conseguenze della perdita di questo singolo motore nucleare non sono rimaste confinate alle cellule in coltura. I topi privi di NM1 sono diventati gradualmente più pesanti dei loro consanguinei normali, pur non assumendo più cibo. Le scansioni e le analisi tissutali hanno mostrato un chiaro accumulo di grasso, specialmente intorno agli organi interni dell’addome, e le singole cellule adipose in queste aree erano sorprendentemente ingrandite. Misurando quali geni fossero attivati o soppressi in questo grasso viscerale, i ricercatori hanno trovato cambiamenti diffusi: vie coinvolte nell’uso dell’energia, nella segnalazione dell’insulina e nel rimodellamento tissutale erano riprogrammate. Geni associati alla crescita ed espansione degli adipociti risultavano spesso aumentati, mentre diversi regolatori centrali della formazione di adipociti sani erano attenuati, rispecchiando i difetti osservati nelle cellule staminali in coltura.
Grasso infiammato e motori energetici disturbati
Oltre alle dimensioni, il tessuto adiposo nei topi privi di NM1 mostrava segni di infiammazione e stress metabolico. Un’analisi approfondita dei percorsi ha evidenziato una forte attivazione di segnali immunitari guidati da molecole come l’interferone-gamma e il fattore di necrosi tumorale, noti per contribuire alla resistenza all’insulina e alle malattie metaboliche. Allo stesso tempo, i regolatori che favoriscono un tessuto adiposo calmo ed efficiente dal punto di vista energetico risultavano soppressi. Lo studio ha inoltre collegato la perdita di NM1 a mitocondri disturbati — i motori energetici della cellula. I geni che normalmente sovrintendono al controllo di qualità mitocondriale e allo switch tra produzione energetica efficiente e rapido metabolismo glicolitico erano disregolati, suggerendo che in assenza di NM1 gli adipociti adottano una strategia energetica meno efficiente e più soggetta a stress.
Segnali condivisi tra topi e umani
Per verificare se questo percorso nucleare potesse avere rilevanza nell’uomo, gli autori hanno esaminato grandi dataset genetici provenienti da grasso viscerale umano. Si sono concentrati su un omologo umano di NM1 chiamato MYO1C e hanno analizzato reti di varianti che modulano l’attività dei geni vicini. Hanno trovato che molti degli stessi temi osservati nei topi — controllo del citoscheletro, segnalazione immunitaria e regolazione metabolica — ricorrevano nelle reti genetiche umane centrate su MYO1C. Diversi geni alterati nel grasso dei topi privi di NM1 erano anche presenti in queste reti umane e sono stati associati al rimodellamento del tessuto adiposo e al metabolismo. Questa sovrapposizione tra specie suggerisce che meccanismi nucleari simili potrebbero influenzare il rischio di obesità anche negli esseri umani.
Cosa significa per obesità e salute metabolica
Nel complesso, il lavoro mostra che NM1 è molto più di un aiutante nucleare; è un hub centrale che lega l’organizzazione del DNA a come le cellule adipose crescono, immagazzinano energia e comunicano con il sistema immunitario. Quando NM1 manca, gli interruttori genici nei precursori adiposi vengono impostati in modo errato, i mitocondri funzionano male, le cellule adipose si ingrandiscono invece di moltiplicarsi e il grasso viscerale si infiamma — una combinazione che somiglia al tessuto adiposo malsano osservato in obesità e resistenza all’insulina. Per il lettore non specialista, il messaggio è che l’organizzazione fisica del DNA e dei suoi ausiliari all’interno del nucleo può predisporre i tessuti a un’espansione adiposa salutare o dannosa. Proteine come NM1 e il suo omologo umano MYO1C potrebbero un giorno diventare bersagli per terapie volte a rimodellare il tessuto adiposo dall’interno, offrendo una strada più precisa per affrontare le malattie legate all’obesità.
Citazione: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Parole chiave: adipogenesi, cromatina, mitocondri, grasso viscerale, infiammazione metabolica