Clear Sky Science · it
La trimetilazione della lisina 36 sull'istone H3 da parte di SETD2 modella un paesaggio epigenetico nelle cellule staminali intestinali per orchestrare il metabolismo lipidico e attenuare la senescenza cellulare
Perché le cellule staminali intestinali contano con l'avanzare dell'età
In profondità nel rivestimento del nostro intestino, piccole cellule staminali lavorano senza sosta per rinnovare il tessuto che ci aiuta a digerire il cibo e assorbire i nutrienti. Con l'età queste cellule staminali si esauriscono, rendendo l'intestino più vulnerabile alle malattie e più lento a guarire. Questo studio esplora come sottili marche chimiche sulle proteine che impacchettano il DNA contribuiscano a mantenere giovani le cellule staminali intestinali, come la loro perdita alteri la capacità delle cellule di bruciare i grassi e come farmaci mirati potrebbero un giorno rallentare questo declino.
Cellule invecchianti in un ambiente esigente
La superficie interna dell'intestino è uno dei tessuti che si rinnova più rapidamente nel corpo. Le cellule staminali annidate alla base di piccole cavità, dette cripte, si dividono per sostituire miliardi di cellule ogni pochi giorni. Questo lavoro costante richiede un apporto energetico costante, in gran parte derivato dalla degradazione dei grassi. Allo stesso tempo, queste cellule staminali sono regolate da un codice «epigenetico»: marche chimiche sugli istoni che contribuiscono a determinare quali geni sono attivi o silenziati. Gli autori si sono concentrati su una di queste marche, nota come trimetilazione di H3K36, creata da un enzima chiamato SETD2, e hanno chiesto se i cambiamenti in questa marca possano aiutare a spiegare perché le cellule staminali intestinali perdono vigore con l'età.
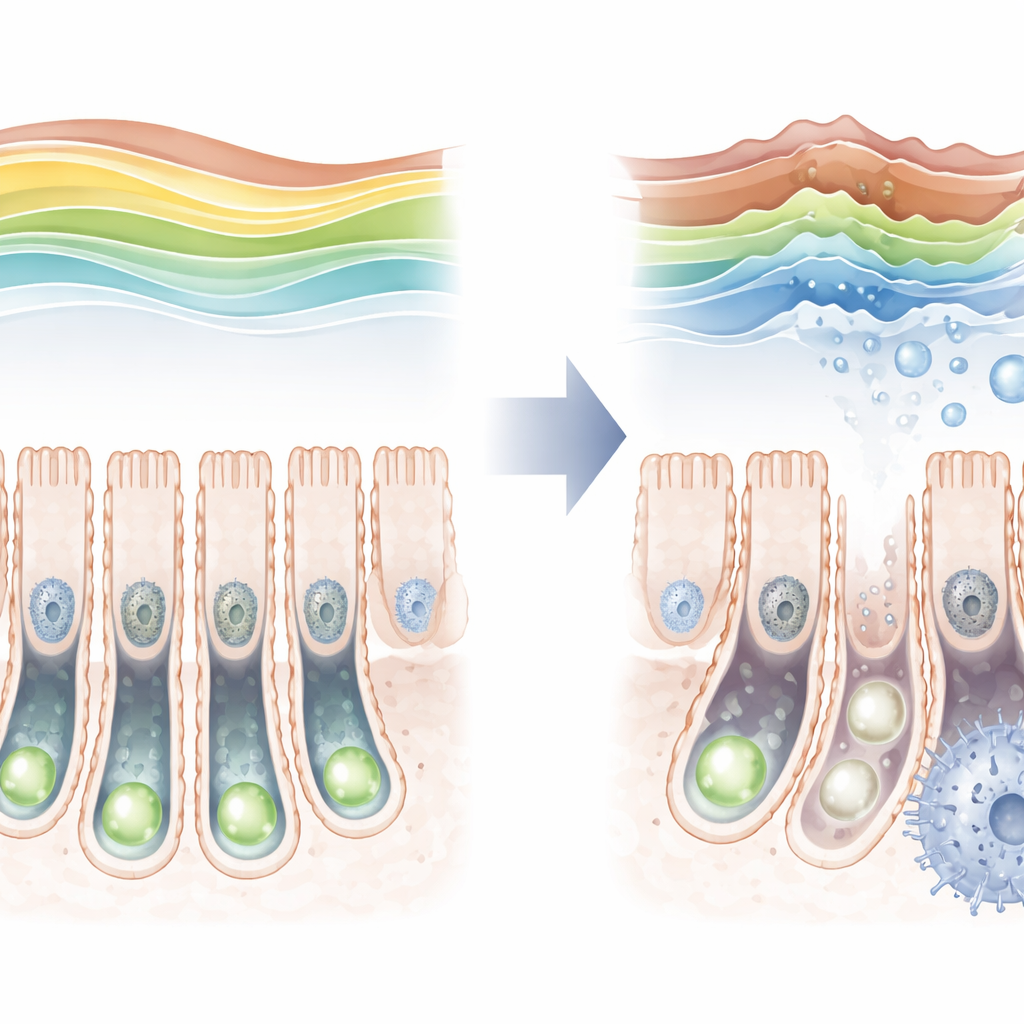
Una marca protettiva che svanisce con l'età
Esaminando gli intestini di topi lungo l'arco della vita, i ricercatori hanno scoperto che la trimetilazione di H3K36 non è statica. È relativamente bassa subito dopo la nascita, poi aumenta fino a un picco nei giovani adulti per poi diminuire negli individui anziani. Con il calo di questa marca negli animali più vecchi, i marcatori di invecchiamento cellulare aumentavano nelle cellule staminali, suggerendo un collegamento tra i due fenomeni. Per testare questo più direttamente, il gruppo ha ingegnerizzato topi in cui SETD2 poteva essere rimosso solo nelle cellule staminali intestinali. Quando l'enzima è stato cancellato, la marca protettiva è quasi scomparsa, le cellule staminali si sono divise meno frequentemente e hanno faticato a generare l'intera gamma di tipi cellulari intestinali specializzati.
Come i cambiamenti epigenetici sabotano la combustione dei grassi
La perdita di questa singola marca istonica ha innescato una cascata di cambiamenti all'interno delle cellule staminali. Le misure dell'attività genica hanno mostrato che molti geni coinvolti nel ciclo cellulare e nella duplicazione del DNA erano soppressi, mentre geni legati allo stress e all'invecchiamento erano sovraespressi. In modo notevole, il segnale più forte indicava un disturbo nella gestione dei lipidi: i geni che normalmente supportano l'ossidazione degli acidi grassi—la combustione controllata dei grassi per ottenere energia—erano attenuati e i lipidi cominciavano ad accumularsi nelle cripte. Il profilo metabolico ha confermato l'accumulo di acidi grassi a catena lunga, segno che i percorsi normali di processamento dei grassi stavano fallendo. Allo stesso tempo, il confezionamento fisico del DNA nel nucleo si è modificato, con molte regioni che sono diventate più esposte o più compatte, rimodellando quali geni la cellula poteva usare con facilità.
Rimodellatori della cromatina e la marcia verso la senescenza
Per capire come emergessero questi cambiamenti nel confezionamento del DNA, gli autori hanno mappato sia le regioni di cromatina aperta sia un insieme di altre marche istoniche lungo il genoma. Quando la trimetilazione di H3K36 veniva persa, ampi tratti di DNA guadagnavano marche «attive» e diventavano più accessibili, specialmente vicino a geni legati al metabolismo e all'invecchiamento. Un attore chiave in questa transizione è stato il complesso di rimodellamento della cromatina SWI/SNF, guidato da una subunità centrale chiamata SMARCA4. Nelle cellule staminali prive di SETD2, i livelli di SMARCA4 aumentavano e il complesso sembrava contribuire ad aprire regioni che attivano programmi di senescenza. Quando i ricercatori ridussero l'attività di SMARCA4 geneticamente o con un inibitore mirato, le cellule staminali recuperarono parte della loro capacità di formare mini-intesti sani in coltura e i marcatori di invecchiamento diminuirono—suggerendo che un rimodellamento eccessivo spinge queste cellule verso uno stato stanco e senescente.
Ririscaldare le vie energetiche per salvare le cellule staminali
Poiché il deficit nella combustione dei grassi è emerso come problema centrale, il gruppo ha testato se potenziare questa via potesse contrastare l'invecchiamento delle cellule staminali. Hanno usato un farmaco che attiva PPARα, un regolatore maestro dell'ossidazione degli acidi grassi. Negli organoidi cresciuti da cellule staminali prive di SETD2, questo trattamento ha aumentato la crescita, ripristinato le strutture a gemma caratteristiche di cellule staminali vigorose e ridotto l'accumulo di lipidi. Nei topi vivi, la stessa intervento ha parzialmente ricostituito il pool di cellule staminali, abbassato i marcatori di senescenza e normalizzato l'accumulo lipidico nelle cripte intestinali. Questi risultati collocano l'ossidazione degli acidi grassi come un collegamento cruciale tra il controllo epigenetico e la salute delle cellule staminali.
Cosa significa per un invecchiamento sano
Nel complesso, il lavoro mostra che una specifica marca istonica, depositata da SETD2, aiuta a mantenere un paesaggio epigenetico bilanciato nelle cellule staminali intestinali. Quando questa marca svanisce, la cromatina viene rimodellata in modo anomalo, le vie di combustione dei grassi deficitano, i lipidi si accumulano e le cellule scivolano nella senescenza, indebolendo il sistema di riparazione dell'intestino. Riducendo l'attività eccessiva della macchina di rimodellamento o ripristinando il metabolismo lipidico con farmaci mirati, potrebbe essere possibile preservare la funzione delle cellule staminali e la salute intestinale nelle età più avanzate. Sebbene questi risultati provengano da esperimenti sui topi, rispecchiano pattern osservati in disturbi intestinali umani, aprendo la prospettiva che terapie metaboliche calibrate possano un giorno aiutare a contrastare il declino legato all'età nelle nostre cellule staminali intestinali.
Citazione: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Parole chiave: cellule staminali intestinali, epigenetica, ossidazione degli acidi grassi, senescenza cellulare, SETD2