Clear Sky Science · it
Un RNA legato a Lamp2a secreto da ADSC previene il feedback ENO1–lattilazione–glicolisi e il comportamento maligno cellulare nel carcinoma mammario triplo negativo
Perché è importante per i pazienti
Il carcinoma mammario triplo negativo è una delle forme più aggressive di cancro al seno e manca dei bersagli ormonali o dei fattori di crescita che rendono altri sottotipi più trattabili. Questo studio svela come questi tumori riallaccino il loro uso energetico per sopravvivere in ambienti poveri di ossigeno e descrive un modo ingegnoso per attaccare quel circuito. Per il lettore offre uno scorcio di come la comprensione del metabolismo del cancro possa portare a nuove terapie altamente mirate, molto diverse dalla chemioterapia tradizionale.
Come si alimentano questi tumori
Molti tumori dipendono fortemente da una via veloce ma inefficiente di produzione di energia chiamata glicolisi, che trasforma lo zucchero nel sottoprodotto lattato. Analizzando campioni di pazienti, banche dati genetiche pubbliche e molte linee cellulari di carcinoma mammario, i ricercatori dimostrano che i tumori triplo negativi fanno ancora più affidamento sulla glicolisi rispetto ad altri tumori mammari. Un enzima chiave in questa via, ENO1, è presente a livelli particolarmente elevati in questi tumori ed è associato a una sopravvivenza peggiore. Quando i livelli di ENO1 sono stati ridotti in cellule triplo negative coltivate in laboratorio, le cellule si sono spostate dalla glicolisi verso una produzione energetica più normale nei mitocondri, sono cresciute più lentamente e hanno mostrato minore capacità di invadere o formare colonie.
Un circolo vizioso pericoloso dentro le cellule tumorali
Approfondendo, il gruppo ha scoperto che lo stesso lattato rafforza ENO1 e imprigiona le cellule tumorali in un circolo vizioso. Il lattato può modificare chimicamente le proteine in un processo chiamato lattilazione. Nelle cellule triplo negative, un eccesso di lattato aumentava la lattilazione di ENO1, che a sua volta potenziava l’attività e la stabilità dell’enzima, accelerando ulteriormente la glicolisi e producendo ancora più lattato. In condizioni di basso ossigeno — tipiche dei tumori solidi — questo circuito si rafforzava, aiutando le cellule tumorali a resistere alla morte cellulare e a continuare a proliferare. Bloccare l’attività di ENO1 con un inibitore molecolare di piccole dimensioni, o ridurre la produzione di lattato, indeboliva questo circuito, frenava la glicolisi e rallentava la crescita tumorale nei topi.
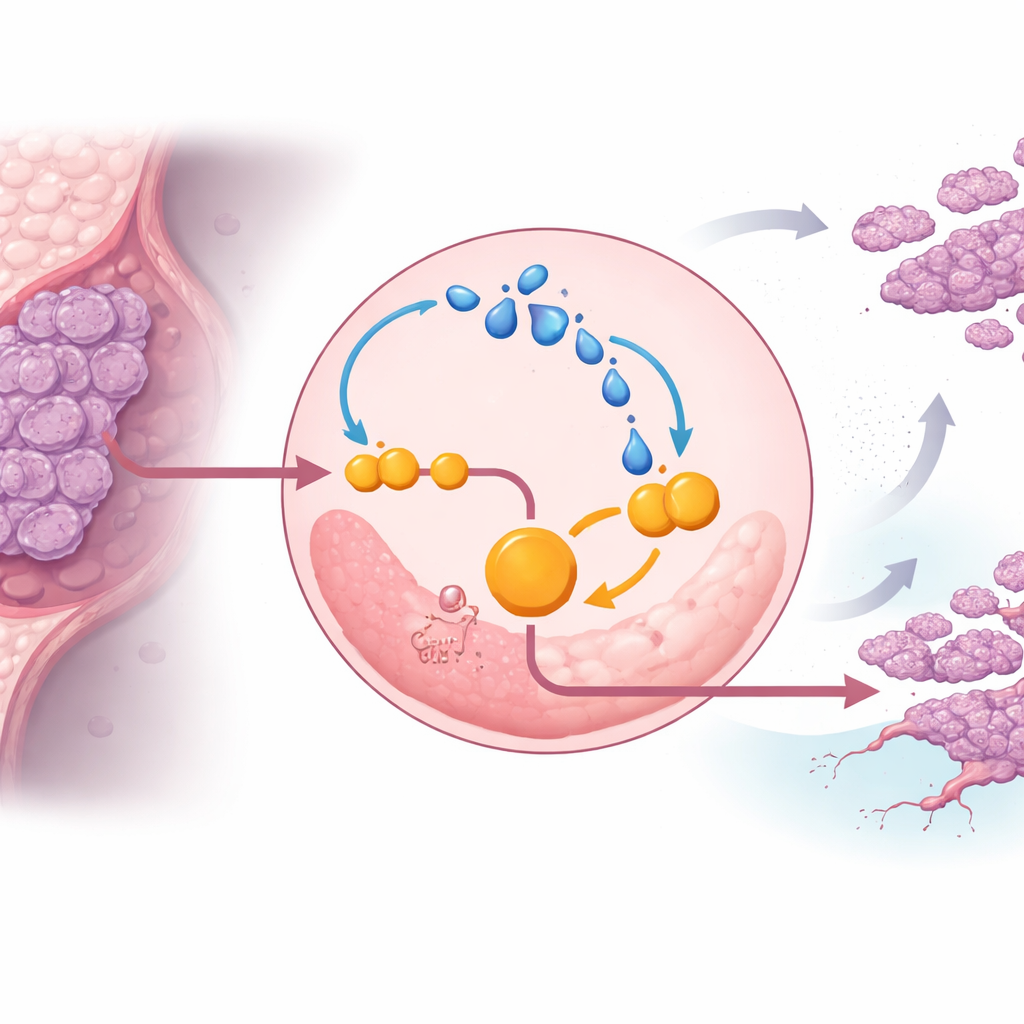
Il selettore molecolare che protegge ENO1
Lo studio ha identificato un punto di controllo specifico su ENO1 che rende possibile questo circuito. Una proteina nota come EP300 aggiunge etichette a base di lattato su diversi residui di lisina di ENO1, con un sito, denominato K262, che si è rivelato cruciale. Quando questo sito è stato mutato in modo da non poter più essere lattilato, ENO1 veniva rapidamente instradato verso i centri di riciclo della cellula, i lisosomi, e degradato. Senza questa etichetta protettiva, le cellule triplo negative perdevano gran parte della loro spinta glicolitica e della capacità di formare tumori e metastasi nei modelli animali. Ciò individua la lattilazione di ENO1 in K262 come un interruttore molecolare che protegge l’enzima dalla distruzione e sostiene il metabolismo alterato del tumore.
Un nuovo modo per segnare ENO1 per la distruzione
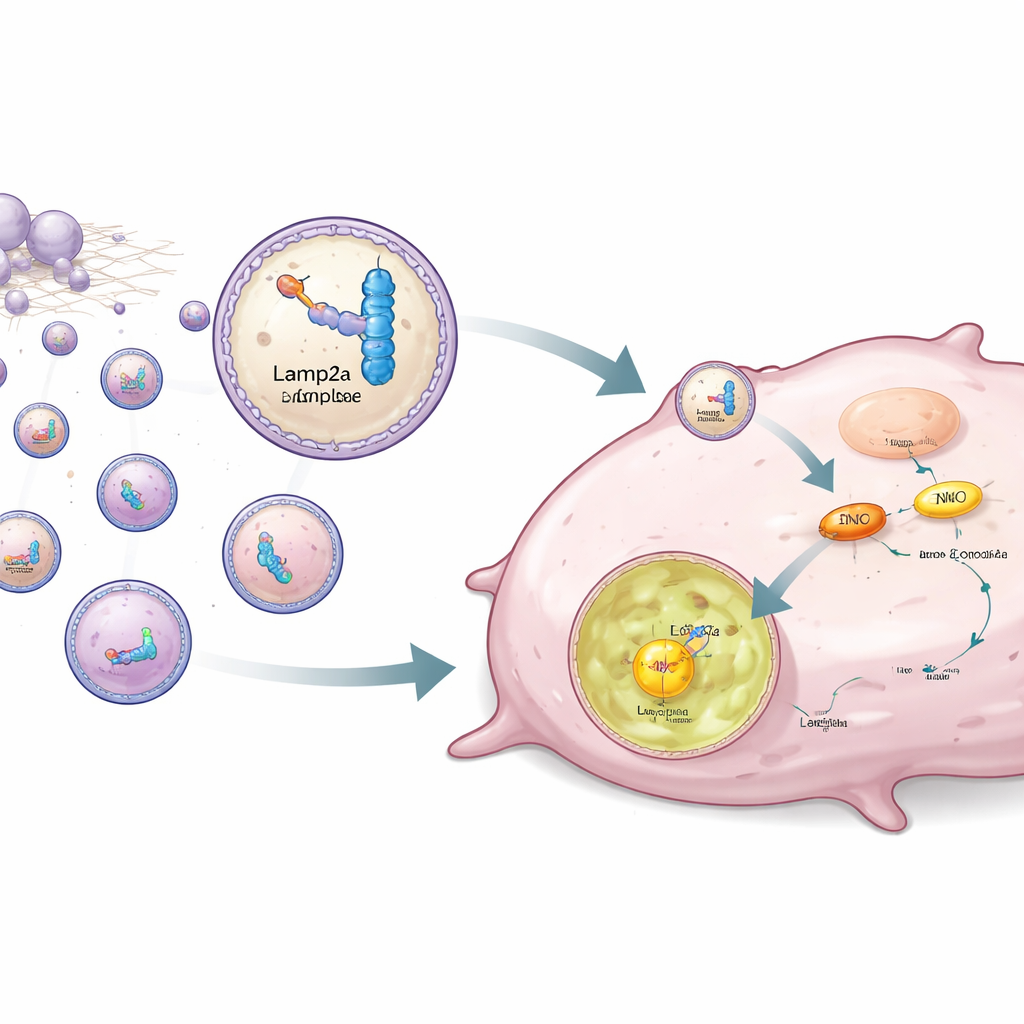
Piuttosto che limitarsi a bloccare ENO1, gli autori hanno ideato una strategia per rimuoverlo selettivamente dalle cellule tumorali. ENO1 funziona anche come proteina legante RNA, riconoscendo sequenze RNA corte e specifiche. Il gruppo ha progettato pezzi di RNA sintetici che si legano saldamente a ENO1 e poi li ha collegati a Lamp2a, una proteina di membrana lisosomiale coinvolta nella degradazione proteica mirata. Le cellule staminali derivate dal tessuto adiposo umano sono state modificate geneticamente per produrre questa coppia RNA–Lamp2a e per confezionarla in piccole vescicole chiamate esosomi. Quando questi esosomi ingegnerizzati sono stati aggiunti a cellule triplo negative, la porzione di RNA si è agganciata a ENO1, mentre la parte Lamp2a ha guidato l’intero complesso nei lisosomi, dove ENO1 è stato degradato anche se portava il marchio di lattilazione stabilizzante.
Testare l’approccio di degradazione mirata negli animali
Per avvicinare questa idea a una terapia pratica, i ricercatori hanno coltivato le cellule staminali modificate su uno scaffold biodegradabile e impiantato questo costrutto sotto la pelle dei topi, vicino ai tumori triplo negativi. Da questa posizione, le cellule staminali rilasciavano continuamente esosomi contenenti i complessi mirati contro ENO1. I tumori in questi animali mostravano livelli proteici di ENO1 nettamente più bassi, glicolisi ridotta, meno cellule in divisione e più segni di morte cellulare rispetto ai controlli. I tumori crescevano più lentamente e il loro comportamento maligno risultava chiaramente attenuato, dimostrando che indirizzare ENO1 verso i lisosomi può effettivamente privare il cancro della sua via energetica preferita.
Cosa potrebbe significare per i trattamenti futuri
Per un pubblico non specialista, il messaggio principale è che questo lavoro rivela sia una vulnerabilità sia un nuovo angolo terapeutico potenziale per il carcinoma mammario triplo negativo. La vulnerabilità è la dipendenza del tumore da un circuito energetico autorinforzante costruito attorno a ENO1 e al lattato, specialmente nelle regioni a basso ossigeno. L’angolo terapeutico è un sistema di degradazione proteica mirata che utilizza RNA su misura ed esosomi derivati da cellule staminali per trascinare ENO1 nel macchinario di smaltimento cellulare. Pur essendo ancora lontano dall’uso clinico, questo approccio illustra come una comprensione profonda degli stratagemmi metabolici del cancro possa ispirare terapie precise che mirano a disarmare, invece che semplicemente avvelenare, le cellule maligne.
Citazione: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Parole chiave: carcinoma mammario triplo negativo, metabolismo del cancro, segnalazione del lattato, degradazione proteica mirata, enzima ENO1