Clear Sky Science · it
La fosfatasi Shp1 regola la stabilità della proteina CXCR2 e l’invasività mediata da IL8 nel tumore al seno
Perché questa ricerca è importante per il tumore al seno
Il tumore al seno resta una delle principali cause di morte per cancro nelle donne, in gran parte perché alcuni tumori diventano invasivi e si diffondono ad organi distanti. Questo studio chiarisce come un segnale infiammatorio comune nei tumori, chiamato IL8, comunichi con le cellule del cancro al seno e come un “freno” molecolare chiamato Shp1 contribuisca a decidere se quelle cellule restano localizzate oppure diventano più aggressive. Comprendere questa lotta molecolare potrebbe aprire nuove strade per rallentare o bloccare la diffusione dei tumori difficili da trattare, in particolare della malattia triplo-negativa.
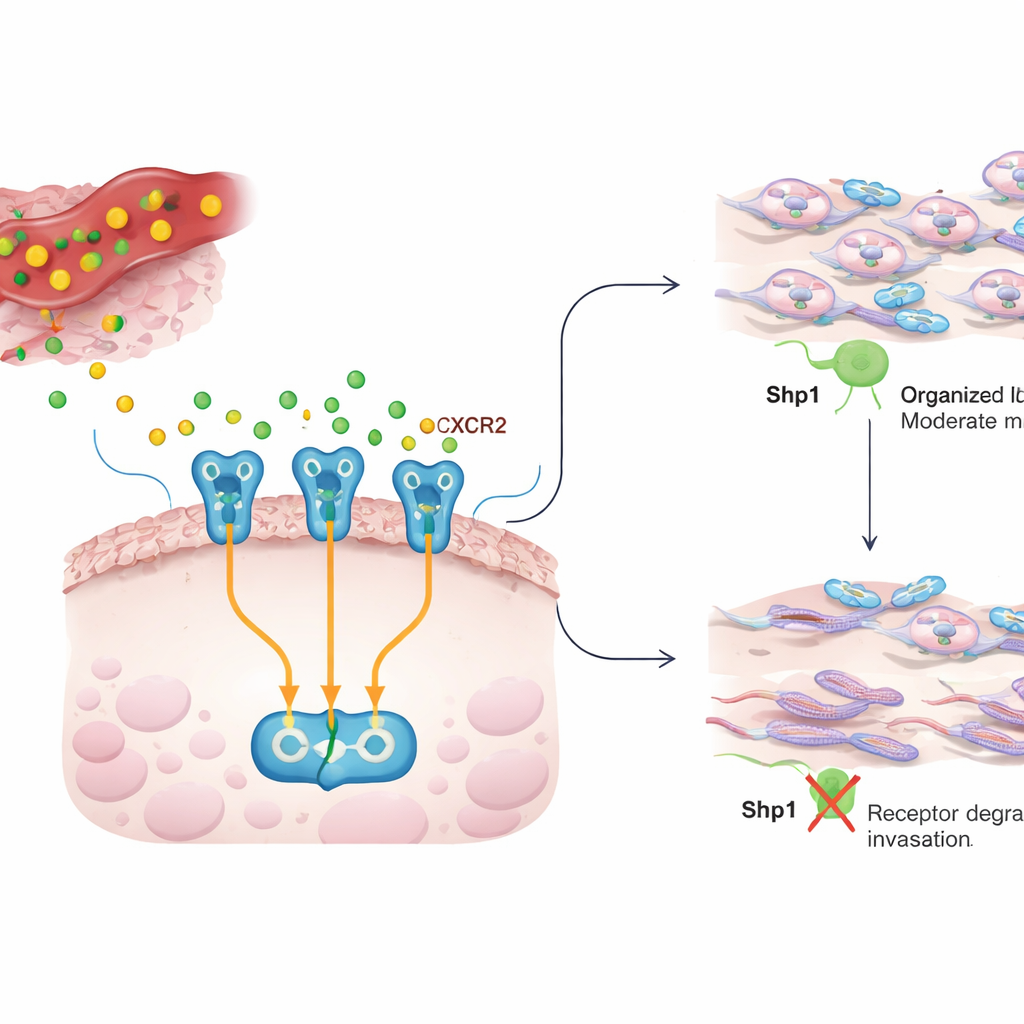
Una conversazione tra infiammazione e cellule tumorali
All’interno di un tumore, le cellule tumorali sono circondate da cellule immunitarie e di supporto che rilasciano messaggeri chimici, o citochine. IL8 è uno di questi messaggeri ed è spesso presente a livelli elevati in molti tumori, dove alimenta la crescita, la formazione di vasi sanguigni e la capacità delle cellule tumorali di muoversi e invadere. IL8 segnala attraverso un recettore sulla superficie delle cellule tumorali chiamato CXCR2. Quando IL8 si lega a CXCR2, attiva diversi circuiti intracellulari che riorganizzano lo scheletro cellulare, aiutando le cellule a spostarsi attraverso i tessuti e a diffondersi. Il lavoro attuale indaga come questa conversazione IL8–CXCR2 venga tenuta sotto controllo e se Shp1, un enzima solitamente considerato un freno soppressore di tumori sui segnali di crescita, influenzi anche questo comportamento invasivo.
Il ruolo nascosto di Shp1 nel movimento cellulare
I ricercatori hanno inizialmente rimosso o bloccato chimicamente Shp1 in una linea cellulare del tumore al seno di tipo luminale ampiamente utilizzata (MCF7) e hanno misurato quanto efficacemente le cellule potevano migrare e invadere attraverso un gel che simula il tessuto. In assenza di Shp1, le cellule tumorali richiudevano le ferite più velocemente e attraversavano il gel con un’efficienza due–tre volte maggiore, rivelando che Shp1 normalmente limita il movimento. Analizzando dati di pazienti, hanno inoltre riscontrato che donne i cui tumori esprimevano meno Shp1 avevano una sopravvivenza peggiore e un tempo alla recidiva più breve. Complessivamente, questi risultati suggeriscono che Shp1 limita il comportamento aggressivo delle cellule del tumore al seno e che la perdita di questo freno è associata a esiti peggiori.
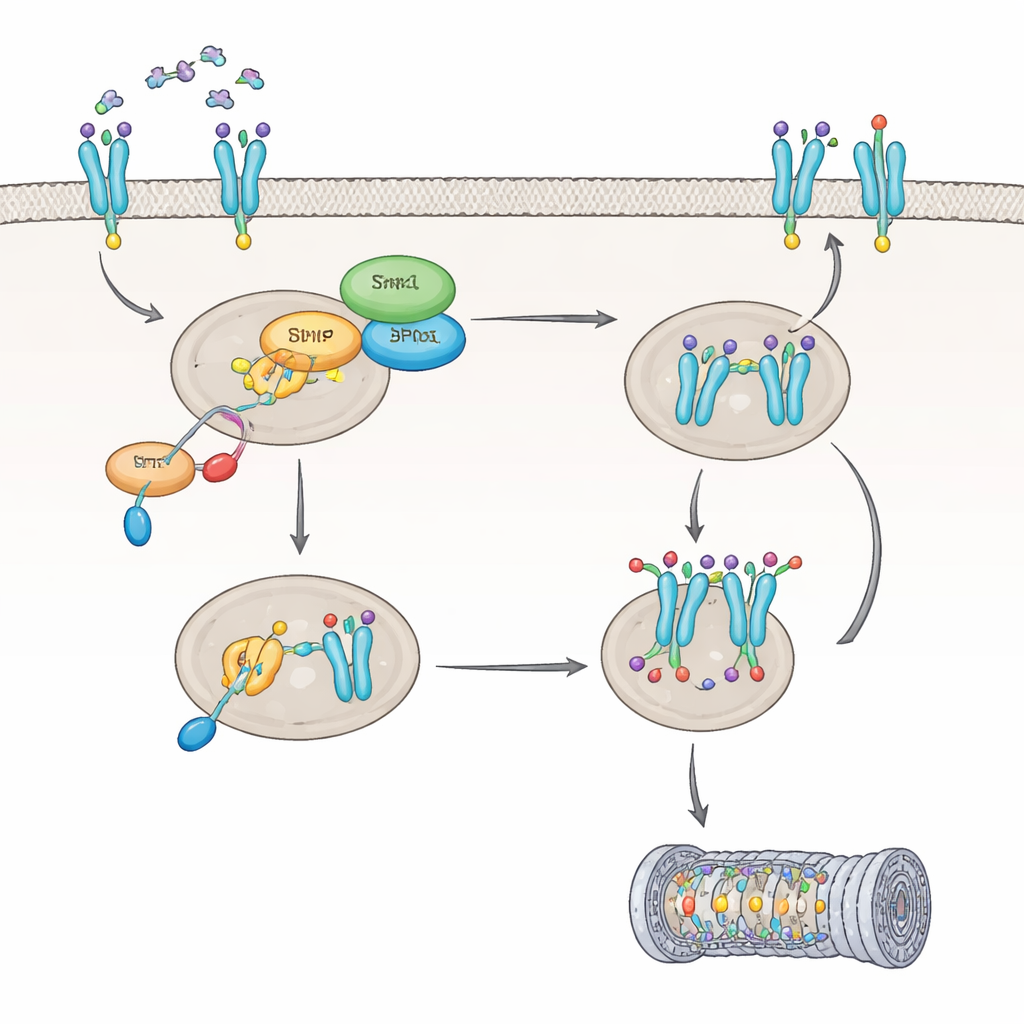
Come IL8 disattiva Shp1 e riprogramma un recettore chiave
Successivamente, il gruppo ha esplorato come IL8 influenzi lo stesso Shp1. Hanno scoperto che IL8 attiva una proteina chiamata PKC, che marca Shp1 in un sito specifico, riducendone l’attività enzimatica di circa il 60%. Quando Shp1 viene attenuato in questo modo, un altro enzima, PP2A, diventa meno attivo e il recettore CXCR2 rimane in uno stato altamente modificato che altera il suo destino all’interno della cellula. Invece di essere ripulito e riciclato alla superficie cellulare, CXCR2 viene etichettato per la distruzione, principalmente tramite la macchina cellulare che degrada le proteine, il proteasoma. Una modifica particolare su CXCR2, sull’amminoacido Ser347, si è dimostrata cruciale per l’attacco di questi tag di degradazione. Nelle cellule prive di Shp1, CXCR2 era più pesantemente etichettato e degradato più rapidamente, portando a un numero inferiore di recettori sulla superficie cellulare e a una risposta attenuata a IL8 nel tempo.
Tipi diversi di tumore al seno, circuiti diversi
Il tumore al seno non è una singola malattia; i tumori sono raggruppati in sottotipi luminali, HER2-positivi e triplo-negativi in base ai loro pattern recettoriali. I ricercatori hanno testato il circuito IL8–CXCR2–Shp1 in diverse linee cellulari rappresentative di ciascun sottotipo. Nelle cellule luminali e triplo-negative, IL8 attivava la cascata Shp1–PP2A–CXCR2, e il blocco di Shp1 aumentava sia l’invasività basale sia annullava l’effetto pro-invasivo tipico di IL8. Al contrario, le cellule HER2-positive rispondevano ancora a IL8, ma il blocco di Shp1 modificava poco il loro comportamento, suggerendo che in questi tumori Shp1 sia occupato da altri segnali, come HER2, e meno disponibile a regolare CXCR2. Analisi su larga scala dell’espressione genica hanno supportato questo quadro: le linee triplo-negative tendevano ad avere livelli inferiori di Shp1, segnalazioni GPCR alterate e livelli più alti di IL8, coerenti con un profilo più aggressivo guidato dall’infiammazione.
Cosa significa per i trattamenti futuri
A un non specialista, il messaggio centrale è che l’enzima Shp1 agisce come un controllore del traffico per il recettore di IL8, CXCR2, determinando se il recettore viene riutilizzato o distrutto e, a sua volta, quanto fortemente le cellule del tumore al seno possono rispondere agli stimoli infiammatori. Nei tumori luminali e triplo-negativi questo punto di controllo sembra particolarmente importante: quando i livelli di Shp1 sono bassi o la sua attività è bloccata, le cellule diventano più invasive e gli esiti dei pazienti peggiorano. Poiché Shp1 può essere potenziato o modulato da alcuni farmaci esistenti, mirare all’asse Shp1–CXCR2, possibilmente in combinazione con inibitori di IL8 o di CXCR2, potrebbe offrire una nuova strategia per limitare l’invasione e le metastasi nei sottotipi di tumore al seno più aggressivi.
Citazione: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Parole chiave: invasione del cancro al seno, segnalazione di IL8, recettore CXCR2, fosfatasi Shp1, carcinoma mammario triplo-negativo