Clear Sky Science · it
CRMP2 inibisce la formazione di metastasi compromettendo la stabilizzazione dell'mRNA di CXCL10 dipendente da ILF3 nel carcinoma mammario
Perché fermare la diffusione del cancro è importante
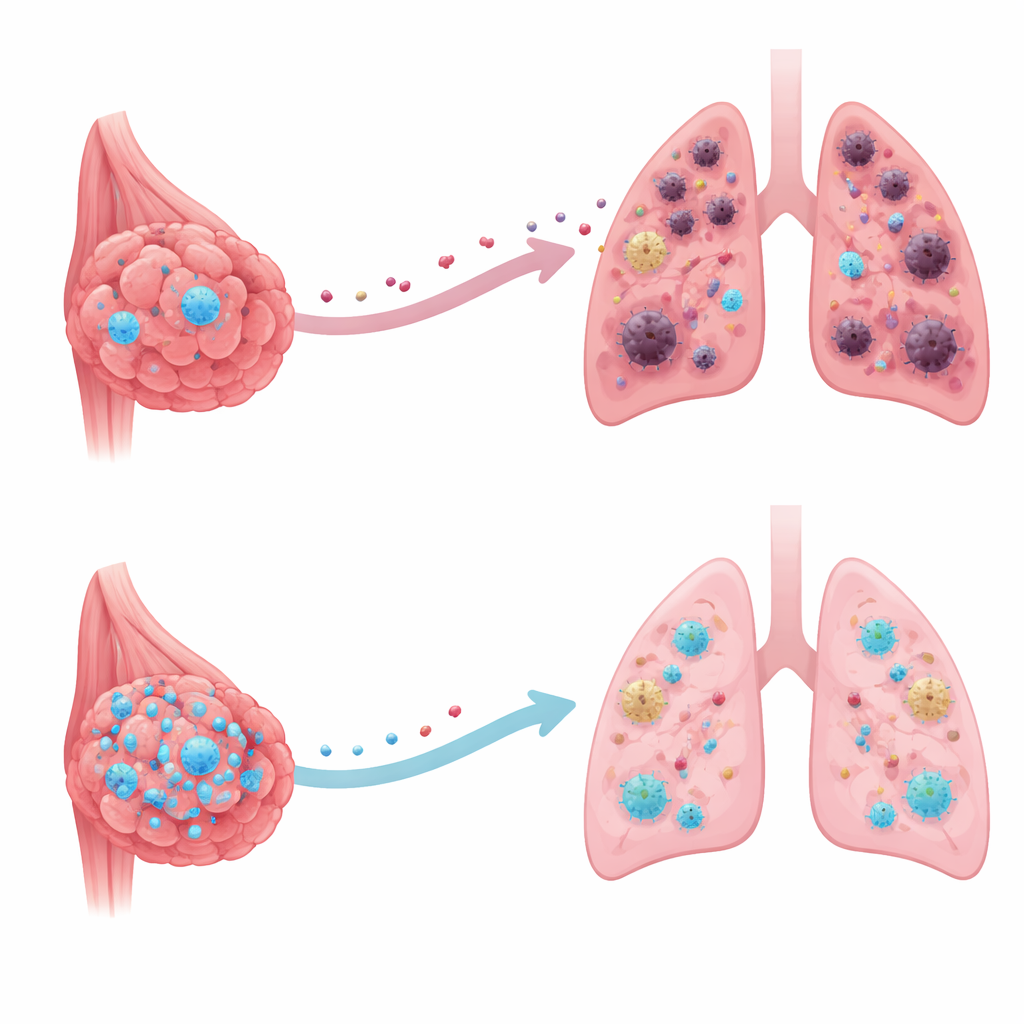
La maggior parte dei decessi per carcinoma mammario non è dovuta al tumore primario, ma al fatto che le cellule tumorali migrano verso organi vitali come i polmoni e lì formano nuove lesioni. Questo studio scopre una proteina protettiva intrinseca nelle cellule del carcinoma mammario che può rallentare o addirittura bloccare questa diffusione modificando il “tappeto d’accoglienza” che gli organi distanti preparano per le cellule tumorali vaganti. Comprendere questo interruttore di sicurezza nascosto potrebbe aprire la strada a nuovi trattamenti che impediscano alle cellule tumorali di radicarsi in altre parti del corpo.
Un difensore silenzioso all’interno delle cellule tumorali
I ricercatori si sono concentrati su una proteina chiamata CRMP2, nota soprattutto per il suo ruolo nel favorire la crescita dei neuroni e nel mantenere il loro scheletro interno. Analizzando grandi banche dati oncologiche pubbliche e campioni tumorali di pazienti, hanno osservato che i livelli di CRMP2 erano insolitamente bassi nei tumori mammari, in particolare nei tumori già metastatizzati. I pazienti i cui tumori mantenevano quantità maggiori di CRMP2 tendevano a vivere più a lungo e avevano una probabilità minore di sviluppare metastasi a distanza. Questo schema suggerisce che CRMP2 si comporti più come un freno che come un acceleratore nel carcinoma mammario, agendo come un difensore interno piuttosto che come un promotore della malattia.
Come i polmoni vengono preparati per l’invasione
Le cellule tumorali raramente arrivano in un organo distante all’improvviso. Molto prima del loro arrivo, il tumore primario rilascia molecole che rimodellano quell’organo in quella che gli scienziati chiamano una “nicchia pre‑metastatica” — un microambiente che favorisce la sopravvivenza tumorale. Usando un modello murino ben consolidato che imita da vicino il carcinoma mammario umano, il gruppo ha mostrato che quando le cellule tumorali mammarie venivano ingegnerizzate per produrre CRMP2 in eccesso, i tumori primari crescevano alla stessa velocità, ma i polmoni diventavano molto meno ospitali. I marcatori di infiammazione e di rimodellamento tissutale nei polmoni diminuivano e venivano reclutate meno cellule immunitarie che normalmente sopprimono le difese antitumorali. Di conseguenza, dopo la rimozione del tumore primario, si formavano molte meno nodularità metastatiche nei polmoni.
Una catena di segnalazione che provoca problemi
Indagando più a fondo, gli scienziati hanno chiesto quali segnali secreti dal tumore fossero responsabili della preparazione dei polmoni. Si sono concentrati su CXCL10, una piccola proteina messaggera (chemochina) nota per attrarre certe cellule immunitarie e per risvegliare cellule tumorali dormienti. Sia nelle cellule tumorali mammarie umane che murine coltivate in laboratorio, l’aumento di CRMP2 ha ridotto drasticamente la quantità di CXCL10 prodotta e secreta. Nei topi, i polmoni esposti a materiale tumorale ricco di CRMP2 mostravano livelli molto più bassi di CXCL10 e meno cellule immunitarie in ingresso che normalmente attenuano l’attività delle cellule T protettive. Quando i ricercatori bloccarono CXCL10 con un anticorpo, la colonizzazione polmonare da parte delle cellule tumorali diminuì; quando aggiunsero nuovamente CXCL10, l’effetto protettivo di CRMP2 venne annullato. Ciò ha collocato CXCL10 chiaramente a valle di CRMP2 come principale promotore di una nicchia favorevole alle metastasi.
Il mediatore nascosto che stabilizza segnali dannosi
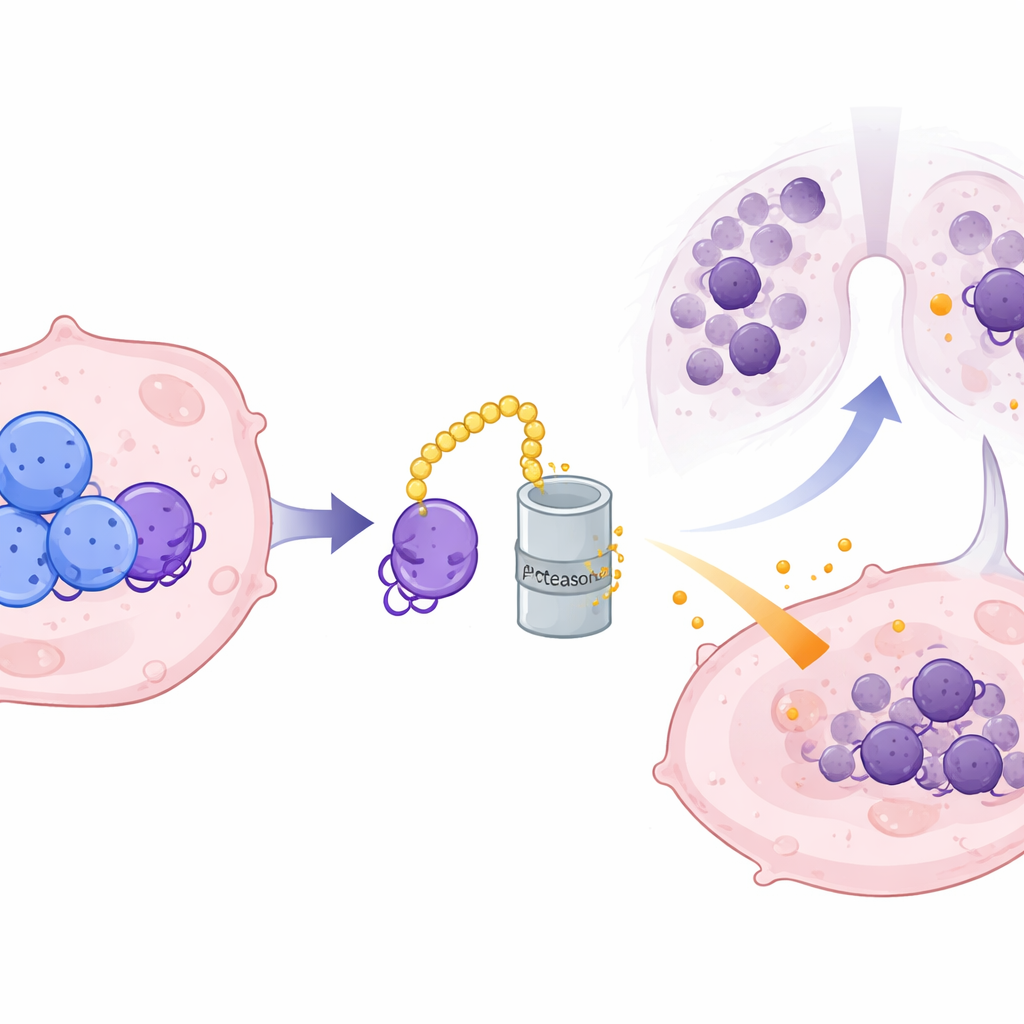
Poiché CRMP2 si trova all’interno delle cellule mentre CXCL10 è secreto, il gruppo sospettò l’esistenza di un mediatore molecolare. Identificarono ILF3, una proteina legante l’RNA, come partner diretto di CRMP2. ILF3 si lega all’RNA che codifica CXCL10 e normalmente lo protegge dalla degradazione, permettendo la produzione di maggiore proteina CXCL10. CRMP2 si lega a ILF3 in punti di contatto specifici e lo marca per la distruzione tramite il sistema di riciclo proteico della cellula, accorciandone la durata e interrompendone il legame con l’RNA di CXCL10. Quando i livelli di CRMP2 sono elevati, ILF3 viene degradato più rapidamente, l’RNA di CXCL10 diventa instabile e viene secreta meno chemochina infiammatoria. Il ripristino artificiale di ILF3 era in grado di sovrascrivere la soppressione di CXCL10 mediata da CRMP2, confermando il suo ruolo come anello cruciale in questa catena.
Trasformare un composto vegetale in un potenziale alleato
Per verificare se questa via potesse essere sfruttata terapeuticamente, i ricercatori hanno setacciato una libreria di composti naturali e hanno scoperto che il psorale — una molecola di origine vegetale usata da tempo nei trattamenti cutanei — si lega direttamente a CRMP2 e ne aumenta la stabilità. Negli esperimenti su cellule, il psorale aumentava i livelli di CRMP2, riduceva ILF3 e CXCL10 e diminuiva il comportamento invasivo delle cellule del carcinoma mammario senza danneggiarne la viabilità complessiva. In diversi modelli murini, il psorale non ridusse i tumori mammari primari, ma diminuì nettamente le metastasi polmonari e attenuò la formazione della nicchia pre‑metastatica, ancora una volta in modo dipendente da CRMP2. Sebbene il psorale stesso possa causare tossicità epatica e richiederà ottimizzazione, questi risultati dimostrano che piccole molecole possono potenziare il ruolo protettivo di CRMP2.
Cosa significa questo per i pazienti
Complessivamente, questo lavoro rivela un asse protettivo all’interno delle cellule del carcinoma mammario in cui CRMP2 destabilizza ILF3, che a sua volta riduce CXCL10 e impedisce ai polmoni di diventare terreno fertile per le metastasi. Piuttosto che attaccare direttamente le cellule tumorali, questa strategia mira a disarmare le nicchie distanti da cui dipendono, spostando l’equilibrio a favore delle difese dell’organismo. Pur rimanendo molto da fare prima che un approccio del genere arrivi in clinica, mirare alla via CRMP2–ILF3–CXCL10 — possibilmente con farmaci simili al psorale ma più sicuri — offre un nuovo e promettente angolo per impedire la diffusione del carcinoma mammario.
Citazione: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Parole chiave: metastasi nel carcinoma mammario, nicchia pre‑metastatica, segnalazione delle chemochine, proteine leganti l'RNA, terapici da prodotti naturali