Clear Sky Science · it
I fibroblasti associati al cancro favoriscono la resistenza a osimertinib nelle cellule del carcinoma polmonare non a piccole cellule tramite la modifica m7G di NET1 mediata da METTL1
Perché alcuni tumori polmonari smettono di rispondere a un farmaco “intelligente”
Farmaci mirati come osimertinib hanno trasformato il trattamento per molte persone con un comune tipo di cancro polmonare, offrendo una sopravvivenza più lunga con effetti collaterali inferiori rispetto alla chemioterapia tradizionale. Tuttavia per la maggior parte dei pazienti questi benefici sono temporanei: i tumori finiscono per trovare modi per eludere il farmaco. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: il tessuto di supporto del tumore — nello specifico cellule chiamate fibroblasti associati al cancro — sta silenziosamente aiutando le cellule tumorali a sfuggire agli effetti di osimertinib?
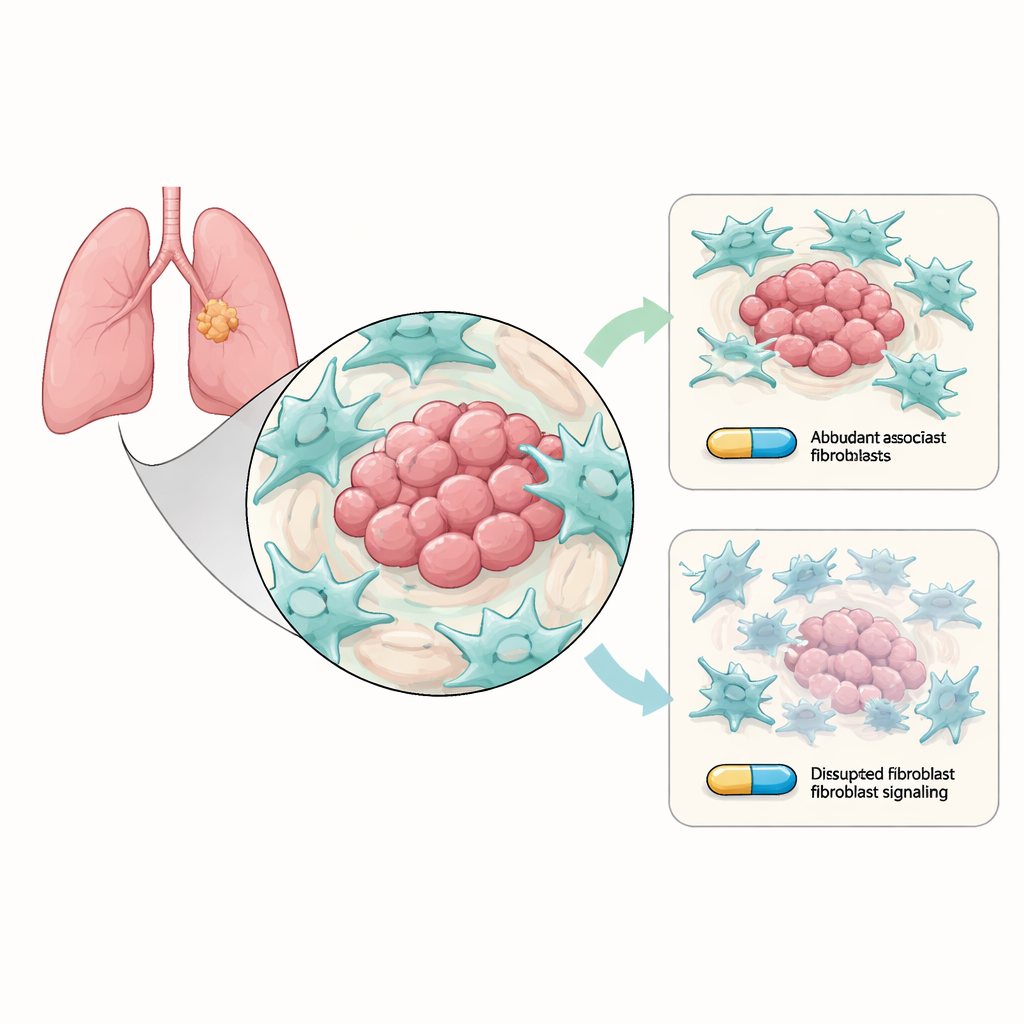
Cellule “aiutanti” che schermano segretamente il tumore
Il carcinoma polmonare non a piccole cellule cresce all’interno di un quartiere affollato di cellule non tumorali noto come microambiente tumorale. Tra gli abitanti più numerosi ci sono i fibroblasti associati al cancro (CAF), cellule del tessuto connettivo che rimodellano l’area attorno al tumore. I ricercatori hanno coltivato in laboratorio cellule tumorali polmonari portatrici delle comuni mutazioni EGFR sensibili a osimertinib insieme ai CAF. Hanno osservato che quando i CAF erano presenti, le cellule tumorali risultavano più difficili da eliminare con osimertinib: formavano più colonie, andavano incontro a meno morte cellulare e manifestavano tratti “stem-like” più marcati associati a sopravvivenza a lungo termine e recidiva. In altre parole, sebbene il farmaco colpisse ancora le cellule tumorali, i fibroblasti circostanti le aiutavano silenziosamente a resistere.
Un segno chimico sull’RNA che cambia le regole
Il gruppo ha quindi guardato oltre i geni stessi, verso i segni chimici che decorano l’RNA — le copie operative dell’informazione genetica all’interno delle cellule. Uno di questi segni, chiamato m7G, può influenzare la stabilità di una molecola di RNA e l’efficienza della sua traduzione in proteina. Tramite test biochimici e mappature su scala genomica, i ricercatori hanno mostrato che i CAF aumentano la marcatura m7G complessiva sugli RNA all’interno delle cellule tumorali polmonari. Questo incremento era guidato principalmente da un’enzima metiltransferasi chiamato METTL1, che deposita i segni m7G sugli mRNA. I livelli di METTL1 erano più alti nei tumori polmonari rispetto al tessuto normale circostante e risultavano associati a malattia più avanzata e a una sopravvivenza peggiore dei pazienti, suggerendo che questo enzima compie più che un semplice fine-tuning delle funzioni cellulari di routine.
Un segnale secreto e una catena molecolare vulnerabile
Come fanno i CAF ad aumentare METTL1 nelle cellule tumorali? Lo studio indica una proteina chiamata HMGB1, che i CAF rilasciano nel loro ambiente. Rispetto alle cellule tumorali, i CAF secernevano quantità molto maggiori di HMGB1. Quando i ricercatori aggiungevano HMGB1 alle cellule tumorali polmonari, aumentavano i livelli di METTL1 e le marcature m7G; quando bloccavano HMGB1 nel mezzo condizionato dai CAF, questo effetto diminuiva. Approfondendo ulteriormente, hanno identificato un bersaglio chiave dell’RNA di METTL1: NET1, un gene che favorisce la crescita e la migrazione cellulare. I CAF aumentavano sia il tagging m7G sia l’abbondanza dell’RNA e della proteina NET1, e METTL1 si legava fisicamente all’RNA di NET1 per stabilizzarlo. Meno METTL1 significava meno NET1 modificato, segnali di sopravvivenza delle cellule tumorali più deboli e maggiore sensibilità a osimertinib.
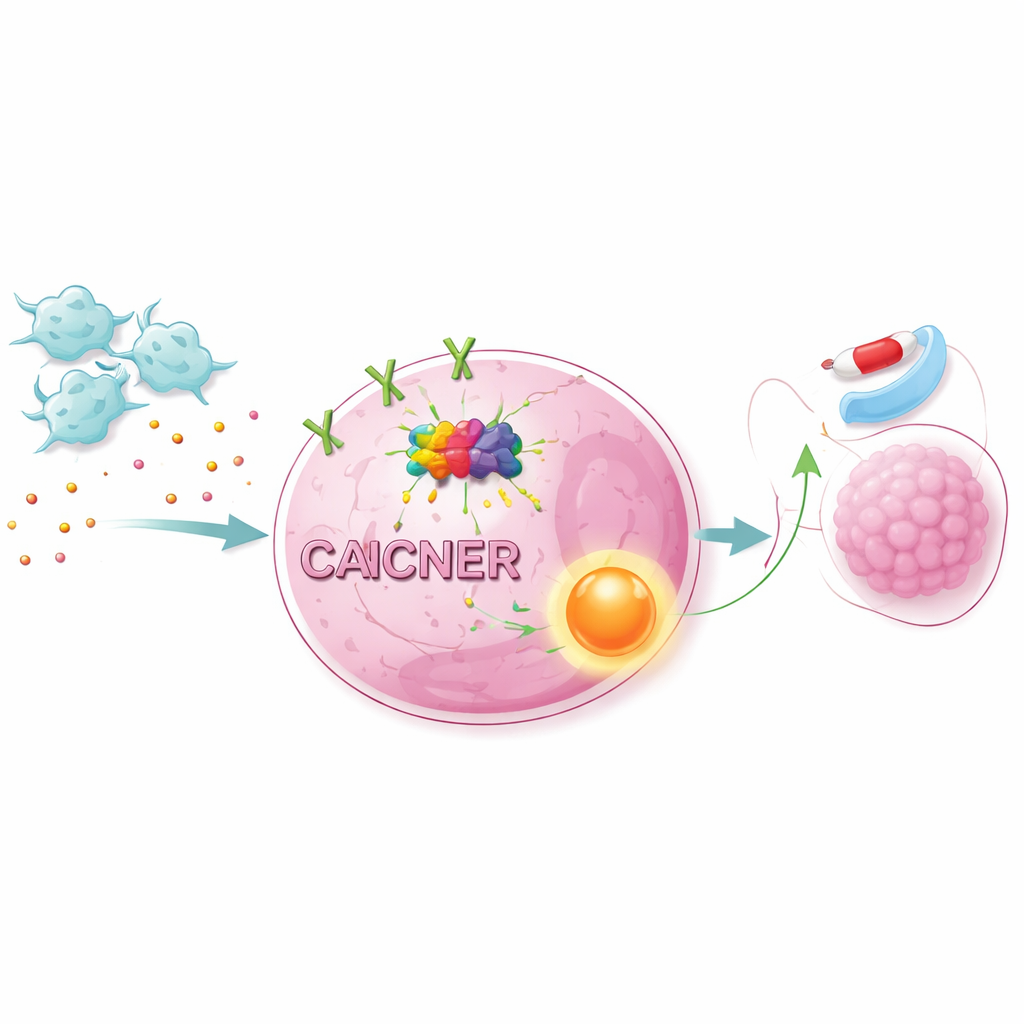
Attivazione di vie di sopravvivenza all’interno delle cellule tumorali
Il segnale NET1 rafforzato non agiva da solo. Combinando dati su larga scala dell’RNA con analisi delle vie di segnalazione, gli scienziati hanno mostrato che i CAF attivano una principale via di crescita e sopravvivenza cellulare nota come via AKT/NF-κB. Bloccare AKT o NF-κB con inibitori specifici rendeva le cellule tumorali polmonari più vulnerabili a osimertinib, anche in presenza di CAF. Modificare i livelli di NET1 dava effetti simili: ridurre NET1 indeboliva la protezione offerta dai CAF, mentre aumentare NET1 accresceva la resistenza. Nei topi impiantati con cellule tumorali polmonari umane, l’aggiunta di CAF faceva crescere i tumori più rapidamente e li rendeva meno responsivi a osimertinib. L’abbattimento di METTL1 nelle cellule tumorali riduceva i segni m7G, abbassava NET1 e l’attivazione delle vie, e diminuiva nettamente la crescita tumorale indotta dai CAF.
Cosa significa per il futuro del trattamento del cancro polmonare
Per le persone con carcinoma polmonare con mutazione EGFR, questo lavoro offre un nuovo modo di pensare al motivo per cui farmaci potenti come osimertinib falliscono nel tempo. Piuttosto che attribuire la colpa solo a nuove mutazioni nelle cellule tumorali, lo studio mette in luce una catena molecolare che inizia al di fuori della cellula tumorale — con i CAF che rilasciano HMGB1 — e prosegue attraverso METTL1, i segni m7G su NET1 e l’attivazione di vie di sopravvivenza che attenuano l’effetto del farmaco. Interrompere questa catena in uno qualsiasi dei suoi punti potrebbe, in linea di principio, ripristinare o prolungare la sensibilità al trattamento. Sebbene farmaci che prendano di mira direttamente METTL1, HMGB1 o specifici RNA segnati da m7G siano ancora in fase iniziale, lo studio suggerisce che combinare osimertinib con terapie rivolte alle cellule di supporto del tumore o ai loro segnali di modifica dell’RNA potrebbe aiutare a mantenere questo tipo di cancro polmonare sotto controllo più a lungo.
Citazione: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Parole chiave: resistenza a osimertinib, carcinoma polmonare non a piccole cellule, fibroblasti associati al cancro, metilazione dell'RNA, via METTL1 NET1