Clear Sky Science · it
miR-424(322)~503 compromette la progressione del cancro del colon guidata dalla carenza di PTEN
Perché questo studio è importante per il cancro del colon
Il cancro del colon resta uno dei tumori più comuni e mortali a livello mondiale, e molti pazienti progrediscono verso malattia avanzata nonostante chirurgia, chemioterapia e farmaci mirati. Questo studio esplora un piccolo insieme di “interruttori” genetici chiamati microRNA che possono rallentare o accelerare la crescita tumorale. Scoprendo come un specifico cluster di microRNA interagisce con un noto gene oncosoppressore, PTEN, il lavoro aiuta a spiegare perché alcuni tumori del colon diventano più aggressivi e indica nuovi modi per prevedere il rischio e progettare terapie.
Piccoli interruttori di RNA con grande impatto
I microRNA sono brevi molecole di RNA che non codificano per proteine ma modulano finemente l’uso di centinaia di geni in una cellula. Il cluster miR-424(322)~503, composto da due microRNA correlati, ha lasciato perplessi i ricercatori perché può comportarsi come freno o acceleratore in tumori diversi. Nel cancro del colon il suo ruolo non era chiaro. Gli autori si sono concentrati sui tumori guidati dalla perdita di PTEN, un gene che normalmente tiene sotto controllo i segnali di crescita ed è frequentemente alterato nei tumori del colon. Hanno posto una domanda semplice ma potente: cosa succede allo sviluppo del cancro del colon quando sia PTEN sia questo cluster di microRNA sono assenti?
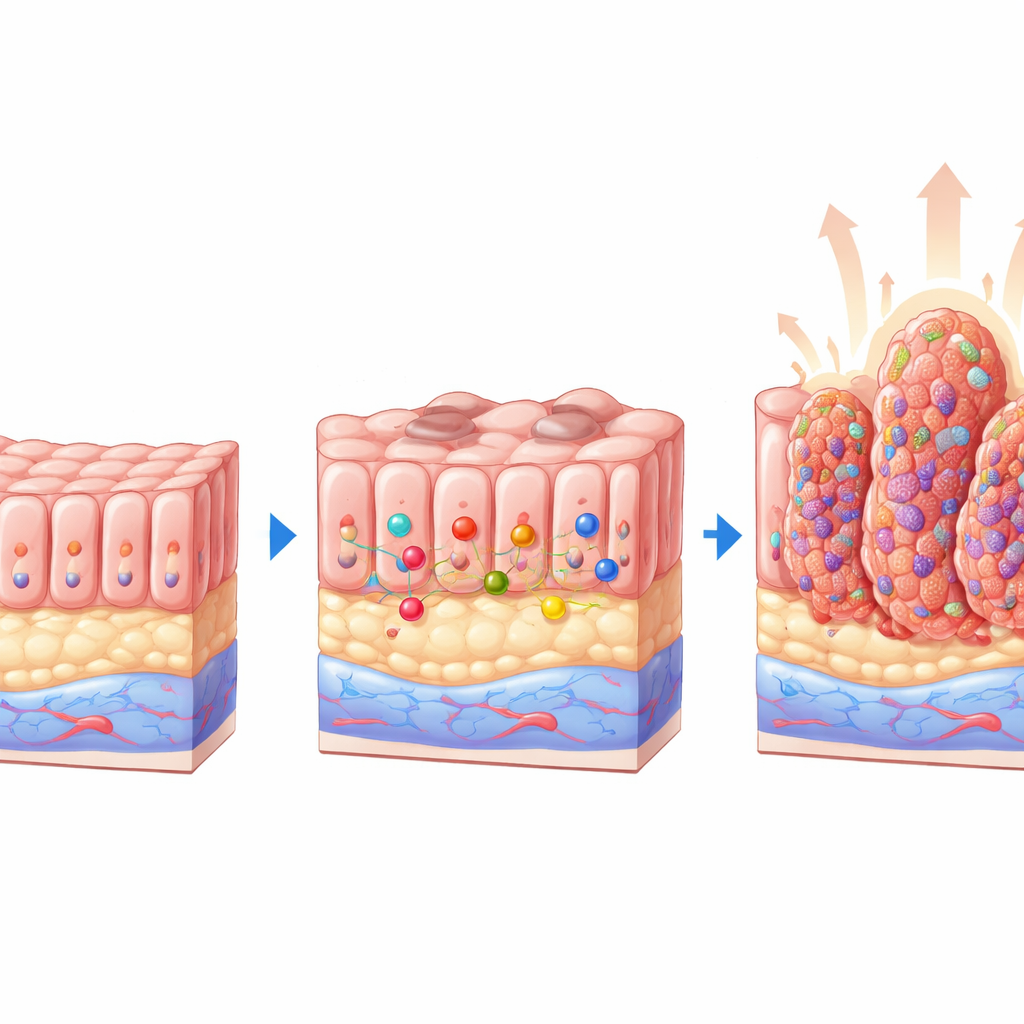
I modelli murini rivelano un ruolo protettivo
Per rispondere, il team ha usato topi geneticamente modificati in cui PTEN può essere disattivato nell’epitelio intestinale, e li ha incrociati con topi privi del cluster miR-424(322)~503. Sono così stati creati quattro gruppi: animali normali, topi privi solo dei microRNA, topi privi solo di PTEN e topi doppio knock-out privi di entrambi. Dopo aver indotto la perdita di PTEN, hanno esaminato attentamente i colons. Gli animali privi solo di PTEN hanno sviluppato molteplici piccoli polipi, molti con tessuto anomalo in fase iniziale. In netto contrasto, i topi privi sia di PTEN sia del cluster di microRNA avevano molte più lesioni, polipi più grandi e una maggiore proporzione di alterazioni avanzate, inclusa displasia di alto grado e adenocarcinoma manifesto. Il solo absere del cluster microRNA non ha causato malattia, mostrando che la sua perdita è particolarmente dannosa quando PTEN è già assente.
La via classica inalterata, spostamento verso nuovi colpevoli
Il cancro del colon è spesso guidato da una sovraattivazione della via Wnt/β-catenina, un percorso chiave che controlla le cellule staminali nell’intestino. Poiché questo cluster di microRNA può influenzare quella via nel tessuto mammario, gli autori hanno testato se lo stesso accadeva qui. Sorprendentemente, livelli e localizzazione della β-catenina e del suo corecettore LRP6 nel colon non sono cambiati quando il cluster microRNA è stato rimosso, nemmeno negli animali doppio knock-out. Invece, il profilo di espressione genica su larga scala ha puntato altrove: i tumori privi sia di PTEN sia dei microRNA mostravano forti firme di rimodellamento tissutale, risposta a ferite e transizione epitelio-mesenchimale, un programma legato a invasione e metastasi. Sono risultate particolarmente arricchite le vie di segnalazione guidate dalle chinasi MAP (ERK1/2 e p38) e dal fattore di crescita TGFβ.
Come i segnali di crescita sfuggono al controllo
Approfondendo, i ricercatori hanno esaminato le proteine nel tessuto colonico. Hanno riscontrato che mentre la perdita di PTEN da sola attivava la via PI3K/AKT, l’aggiunta della perdita del cluster microRNA produceva un’ulteriore impennata dell’attività MAPK: più JNK, p38, MKK4 attivati e soprattutto ERK1/2. Questi segnali altamente attivi coincidevano con livelli più elevati di ciclina D1, un driver chiave della divisione cellulare. Allo stesso tempo, componenti della via TGFβ che ne promuovono l’attività (SMAD3 e SMAD4) aumentavano, mentre un freno interno (SMAD7) diminuiva, e le cellule tumorali mostravano una maggiore colorazione nucleare di SMAD2/3, coerente con l’attivazione della via. Confrontando i geni tumorali murini con i bersagli predetti dei microRNA, il team ha identificato IGF1, un potente fattore di crescita che alimenta le cascate MAPK, come bersaglio diretto del cluster miR-424(322)~503. In assenza dei microRNA, IGF1 sfuggiva alla repressione, spingendo ancora più in alto la segnalazione MAPK. Analisi di dataset di tumori umani del colon rispecchiavano questi risultati: IGF1 era più alto nei tumori con basso miR-424 o miR-503, e la lunga RNA non codificante che ospita questi microRNA, MIR503HG, così come i microRNA stessi, risultavano alterati in modo coordinato nei tumori dei pazienti.
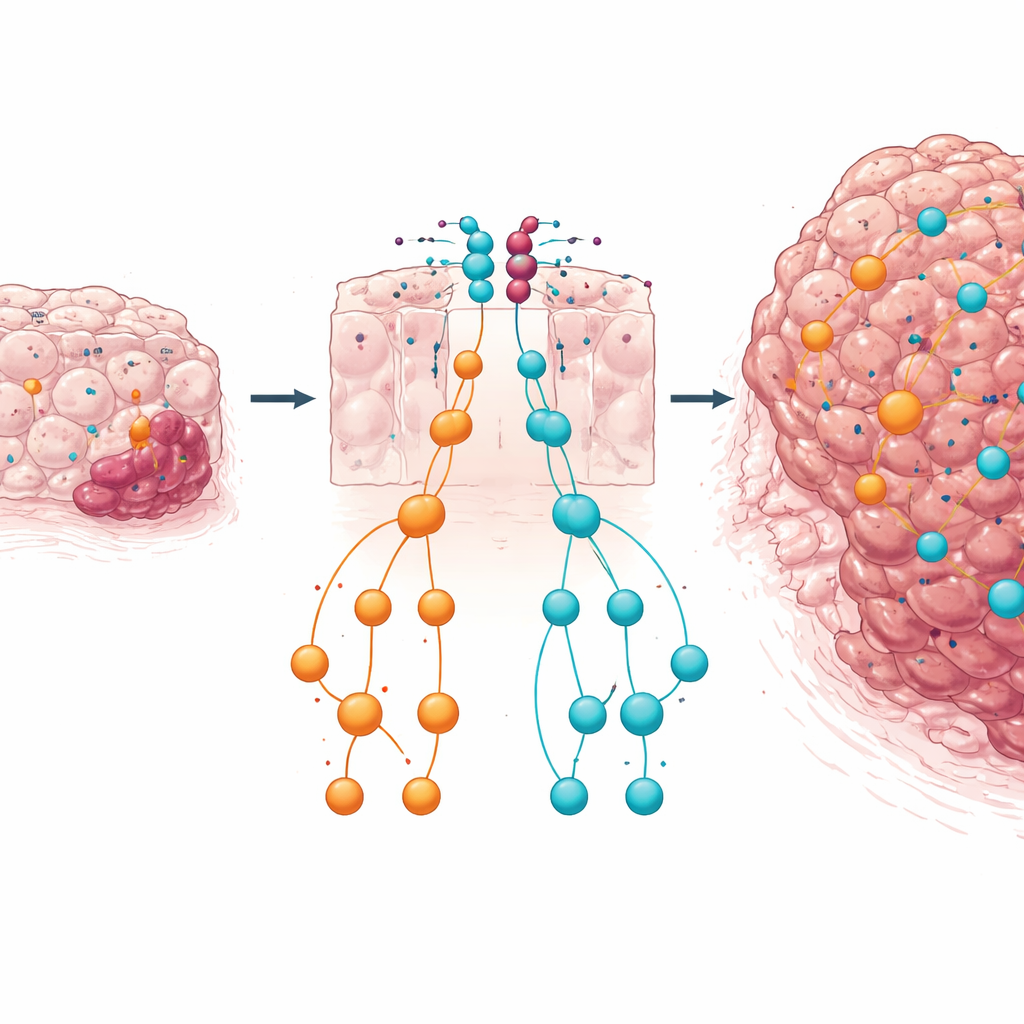
Una doppia rete di sicurezza e cosa significa per i pazienti
Nel complesso, i risultati suggeriscono che nel tessuto colonico carente di PTEN, il cluster miR-424(322)~503 funge da seconda rete di sicurezza. Quando PTEN è perso, questi microRNA vengono upregolati, in parte attraverso segnali come il TGFβ, e lavorano per contenere vie di crescita potenti come IGF1–MAPK e TGFβ–SMAD. Se questo freno microRNA viene rimosso, segnali di crescita e rimodellamento sfuggono al controllo, accelerando la transizione da polipi benigni a cancro invasivo. Per il lettore generico, il messaggio chiave è che non tutte le modifiche genetiche in un tumore spingono nella stessa direzione: alcune sono difese integrate. Comprendere come PTEN e questo cluster di microRNA cooperano per mantenere l’equilibrio della crescita cellulare potrebbe aiutare a identificare pazienti ad alto rischio e ispirare trattamenti combinati che mirino sia agli assi PI3K/AKT sia MAPK/TGFβ nel cancro colorettale.
Citazione: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Parole chiave: cancro colorettale, PTEN, microRNA, segnalazione MAPK, TGF-beta