Clear Sky Science · it
Segnalazione ROR1-PI3K/AKT guida la resistenza adattativa al blocco del ciclo cellulare nel cancro ovarico con mutazione TP53
Perché questa ricerca è importante per la salute delle donne
Il cancro ovarico è tra i tumori più letali nelle donne, in gran parte perché le neoplasie spesso sviluppano resistenza alla chemioterapia. Questo studio pone una domanda cruciale: quando farmaci potenti sono progettati per spingere le cellule tumorali verso un errore letale durante la divisione, come fanno queste cellule a sopravvivere e quell’«via di fuga» può diventare essa stessa un punto debole? Tracciando le cellule di cancro ovarico per settimane e mesi di trattamento, i ricercatori individuano un sistema di controllo centrale all’interno delle cellule che decide se continuare a dividersi o rallentare per riparare i danni — e rivelano un nuovo modo per attaccare tumori che hanno già imparato a resistere ai farmaci standard. 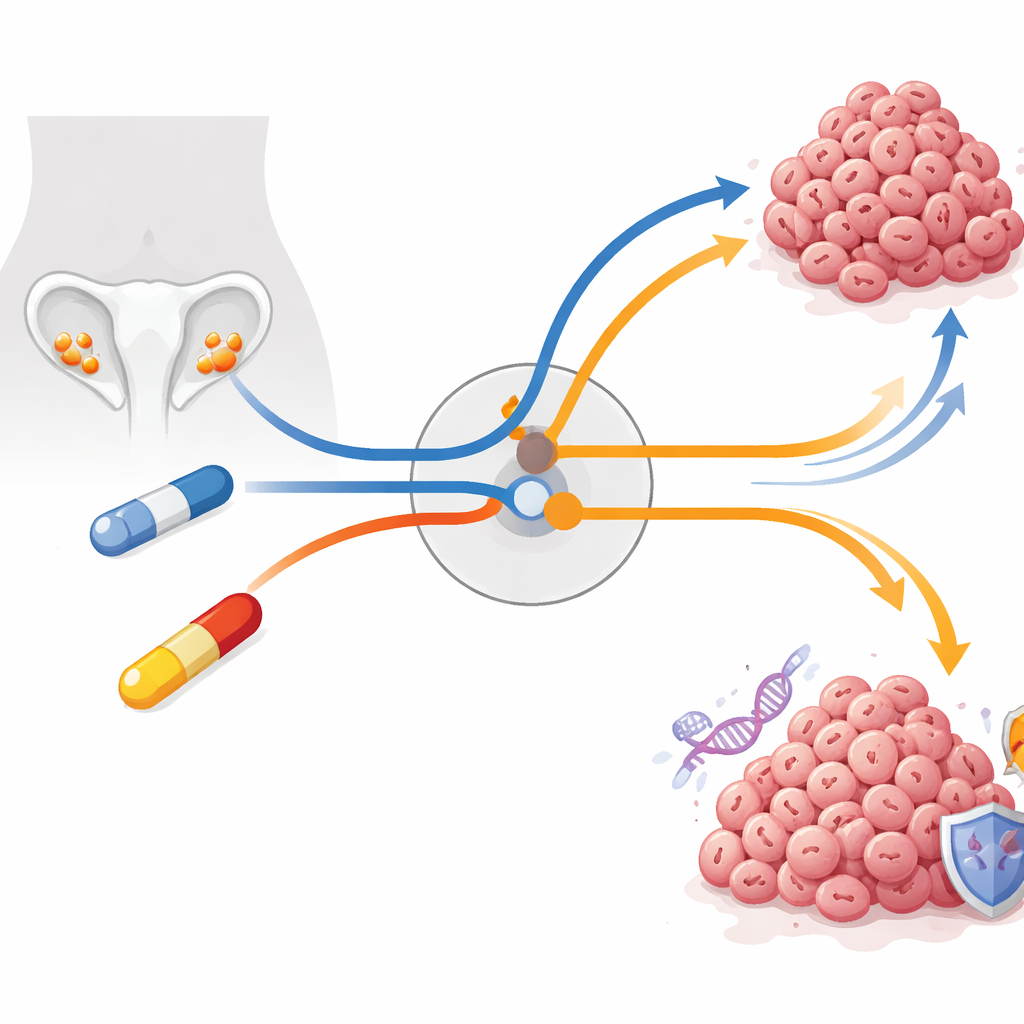
Due farmaci comuni, una via di fuga condivisa
Il gruppo si è concentrato sul carcinoma sieroso di alto grado dell’ovaio, la forma più aggressiva e comune della malattia, che quasi sempre presenta mutazioni nel gene TP53, il «guardiano del genoma». Poiché TP53 è compromesso, questi tumori dipendono in modo anomalo dai checkpoint successivi del ciclo cellulare. Due farmaci largamente usati o sperimentati in questo contesto sfruttano questa vulnerabilità: adavosertib, un inibitore sperimentale di WEE1 che spinge le cellule danneggiate a entrare prematuramente in divisione, e paclitaxel, un chemioterapico di riferimento che blocca lo scheletro interno necessario alla separazione dei cromosomi. In teoria, entrambi dovrebbero indurre nelle cellule tumorali una «catastrofe mitotica» — un fallimento della divisione fatale. Eppure, in clinica e in laboratorio, i tumori si adattano frequentemente. I ricercatori hanno creato modelli cellulari resistenti a lungo termine aumentando gradualmente le dosi di farmaco per mesi, imitazione più realistica di quanto accade nei pazienti rispetto a esperimenti brevi con dosi elevate.
Come le cellule tumorali si rimodellano per sopravvivere
Utilizzando imaging avanzato e la tecnica «Cell Painting» — che colora contemporaneamente molte strutture cellulari — gli scienziati hanno osservato che le cellule resistenti non somigliavano semplicemente alle loro precedenti controparti. Molte avevano nuclei multipli, scheletri interni riorganizzati e formavano aggregati più compatti e sferoidi 3D più piccoli e sparsi, segni distintivi di una parziale trasformazione nota come transizione epitelio–mesenchimale. Questi cambiamenti fisici suggerivano che le cellule avessero riorientato i loro meccanismi di movimento, divisione e interazione. Allo stesso tempo, un sequenziamento dell’RNA a singola cellula dettagliato ha rivelato che ogni farmaco e linea cellulare aveva sviluppato il proprio schema di geni e cromosomi alterati. Nonostante questa diversità genetica, è emerso un tema coerente: l’attività di una via di crescita e sopravvivenza centrata su PI3K e AKT aumentava nei modelli resistenti, spesso accompagnata da percorsi di segnalazione correlati come MAPK e NF-κB.
Un interruttore cellulare tra «scorciatoia rapida» e «riparazione lenta»
Approfondendo, i ricercatori hanno scoperto che questo sistema PI3K/AKT funziona come un interruttore che commuta le cellule tumorali tra due strategie di sopravvivenza. In una modalità «scorciatoia rapida», l’elevata attività PI3K/AKT disattiva la proteina freno FOXO3 e indebolisce i checkpoint del ciclo cellulare, permettendo alle cellule di continuare a dividersi e sfuggire agli effetti letali di adavosertib o paclitaxel. In una modalità opposta di «riparazione lenta», l’attività PI3K/AKT è più bassa, FOXO3 resta attiva nel nucleo e le cellule rallentano la replicazione, attivano programmi di riparazione del DNA e espellono i farmaci con maggiore efficienza. È notevole che l’esposizione breve iniziale ai farmaci inducesse un forte picco di attività PI3K/AKT in tutti i modelli; la resistenza a lungo termine si stabilizzava poi nello stato di scorciatoia rapida o di riparazione lenta a seconda del background genetico del cancro e delle vie di segnalazione pregresse. Ciò dimostra che lo stesso hub centrale può supportare vie di fuga molto diverse. 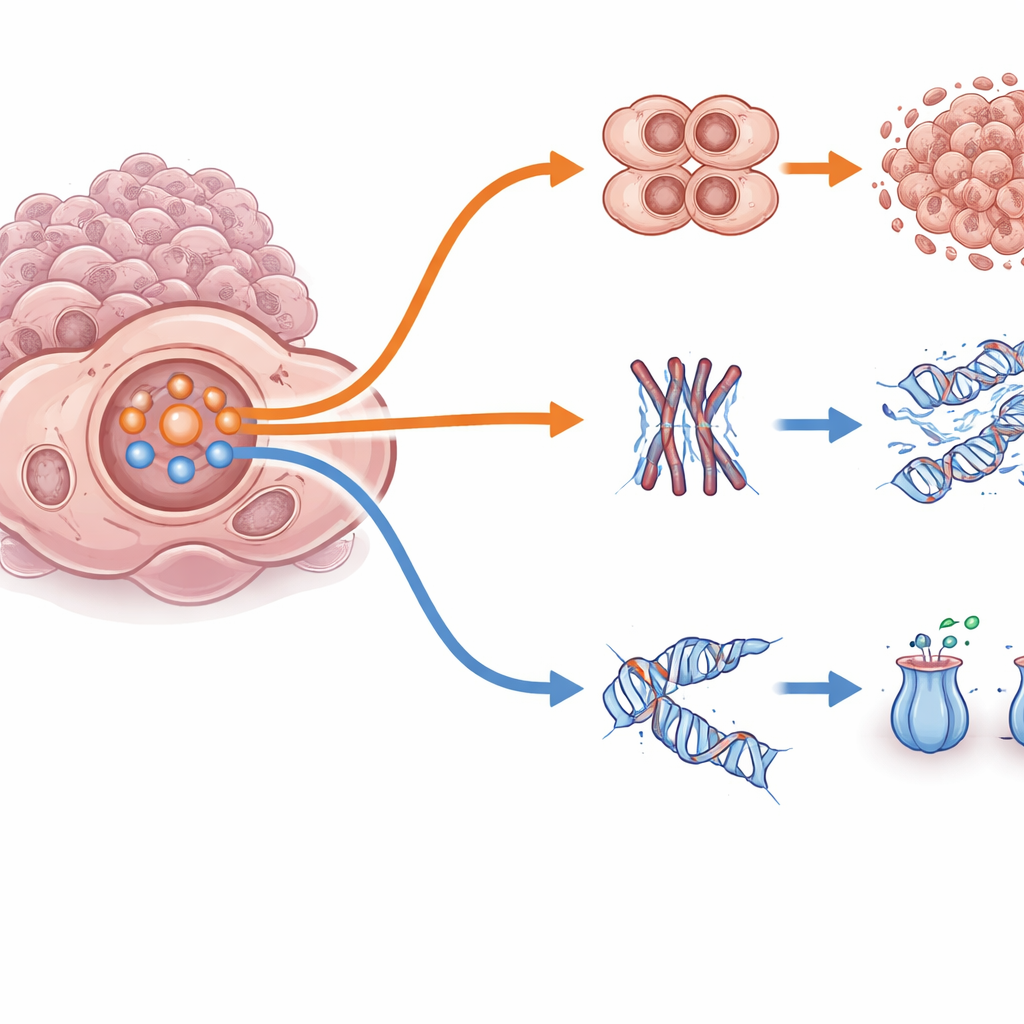
Trasformare un segnale di resistenza in un bersaglio terapeutico
Un elemento chiave a monte di questo hub è ROR1, una proteina recettoriale di norma rara nei tessuti adulti sani ma elevata in diversi tumori. In molti modelli di cancro ovarico resistenti, i livelli di ROR1 aumentavano insieme all’attività PI3K/AKT. Il gruppo ha dimostrato che modulare ROR1 verso l’alto o verso il basso poteva alterare la facilità con cui le cellule acquisivano resistenza ad adavosertib o paclitaxel, in modo dipendente dal contesto. Soprattutto, hanno testato zilovertamab-vedotin, un coniugato anticorpo–farmaco che si dirige verso ROR1 e rilascia un carico tossico. Sia nelle linee cellulari sia in organoidi 3D derivati da pazienti, i tumori con alto ROR1 e resistenti ad adavosertib risultavano particolarmente vulnerabili a questo agente, e la combinazione con adavosertib incrementava spesso l’uccisione cellulare. Alcuni modelli resistenti al paclitaxel erano meno sensibili, probabilmente perché avevano anche rafforzato la capacità di espellere i farmaci.
Cosa significa per il futuro del trattamento del cancro ovarico
Questo lavoro riformula la resistenza ai farmaci nel cancro ovarico con mutazione TP53 non come un evento casuale, ma come una risposta coordinata governata da un interruttore di segnalazione centrale. Identificando l’asse PI3K/AKT–FOXO3 e ROR1 come nodi chiave, lo studio indica strategie pratiche: associare farmaci che prendono di mira la mitosi come adavosertib e paclitaxel a terapie che bloccano l’hub di resistenza o sfruttano ROR1 sulle cellule resistenti. Poiché ROR1 è in gran parte assente nei tessuti sani, tali combinazioni potrebbero colpire selettivamente i tumori recidivanti e induriti dalla terapia, risparmiando le cellule normali. Sebbene questi risultati derivino da modelli di laboratorio e colture derivate da pazienti piuttosto che da trial clinici conclusi, offrono una road map chiara per progettare terapie più intelligenti e durature per le donne affette da carcinoma sieroso di alto grado dell’ovaio.
Citazione: Raivola, J., Rantanen, F., Dini, A. et al. ROR1-PI3K/AKT signaling drives adaptive resistance to cell cycle blockade in TP53 mutated ovarian cancer. Cell Death Dis 17, 276 (2026). https://doi.org/10.1038/s41419-026-08501-x
Parole chiave: cancro ovarico, resistenza ai farmaci, via PI3K AKT, terapia con anticorpi contro ROR1, inibitori del ciclo cellulare