Clear Sky Science · it
La soppressione dell’autofagia guidata da mTOR definisce una vulnerabilità metabolica nel cancro al seno HR+/HER2− resistente agli inibitori di CDK4/6
Perché è importante per le pazienti con cancro al seno
Molte donne con cancro al seno avanzato oggi vivono più a lungo grazie a farmaci chiamati inibitori di CDK4/6, che rallentano la velocità con cui le cellule tumorali si dividono. Purtroppo, la maggior parte dei tumori impara col tempo a sfuggire a questi medicinali. Questo studio pone una domanda incoraggiante: quando il cancro al seno diventa resistente agli inibitori di CDK4/6, acquisisce una nuova debolezza che i medici potrebbero sfruttare con farmaci metabolici già disponibili e relativamente semplici, come la metformina o il dicloroacetato (DCA)?
Quando i farmaci che bloccano il ciclo cellulare smettono di funzionare
I medici trattano spesso il tipo più comune di cancro al seno—tumori con recettori ormonali positivi e HER2 negativo—con terapia ormonale più inibitori di CDK4/6 come palbociclib o ribociclib. Questi farmaci prendono di mira proteine che spingono le cellule attraverso il ciclo di divisione. Col tempo, però, alcune cellule tumorali si adattano e diventano fortemente resistenti, continuando a crescere anche in presenza di dosi elevate di farmaco. I ricercatori hanno ricreato questo problema in laboratorio esponendo linee cellulari di carcinoma mammario (T47D e MCF7) a quantità di inibitori di CDK4/6 progressivamente crescenti. Hanno così ottenuto due tipi di sopravvissute: cellule parzialmente resistenti e un gruppo più piccolo di cloni altamente resistenti che non rispondevano più bene al trattamento.
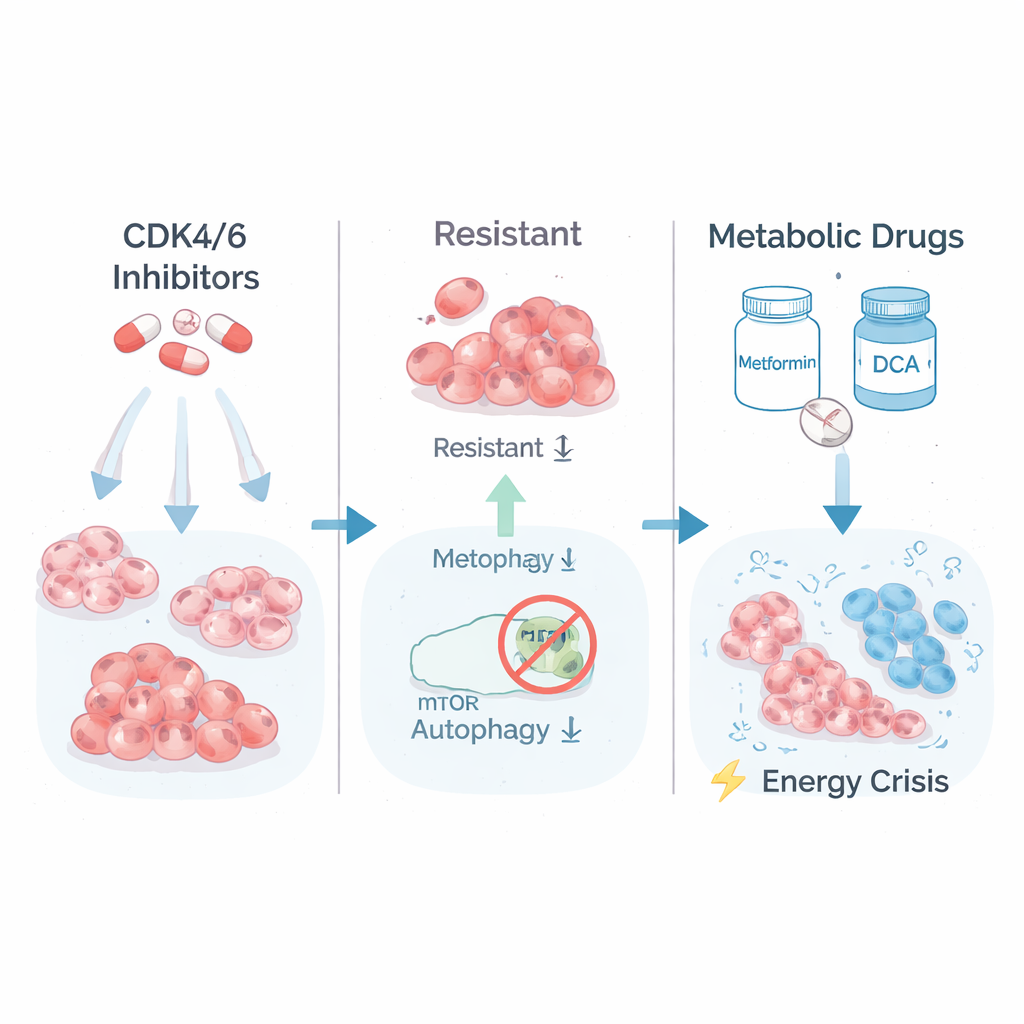
Una debolezza nascosta nell’uso dell’energia del tumore
Per capire cosa rendeva diverse le cellule altamente resistenti, il gruppo ha esaminato quali geni erano attivati o silenziati. Hanno scoperto che le cellule più resistenti avevano potenziato le vie coinvolte nella combustione dello zucchero (glicolisi) e la segnalazione di crescita controllata da un complesso proteico chiamato mTORC1. In altre parole, queste cellule vivevano a tutto gas, consumando carburante a ritmi elevati per continuare a crescere. Gli scienziati hanno quindi testato se questo metabolismo «alta marcia» potesse essere usato contro le cellule. Hanno trattato le cellule resistenti e quelle parentali con metformina, un comune farmaco per il diabete che stressa le centrali energetiche cellulari, e con DCA, che costringe le cellule a processare il carburante in modo più efficiente. Colpisce che i cloni più resistenti al farmaco sono risultati i più vulnerabili: la loro crescita a lungo termine in coltura crollava sotto il trattamento metabolico, mentre le cellule parentali e quelle solo parzialmente resistenti erano molto meno influenzate.
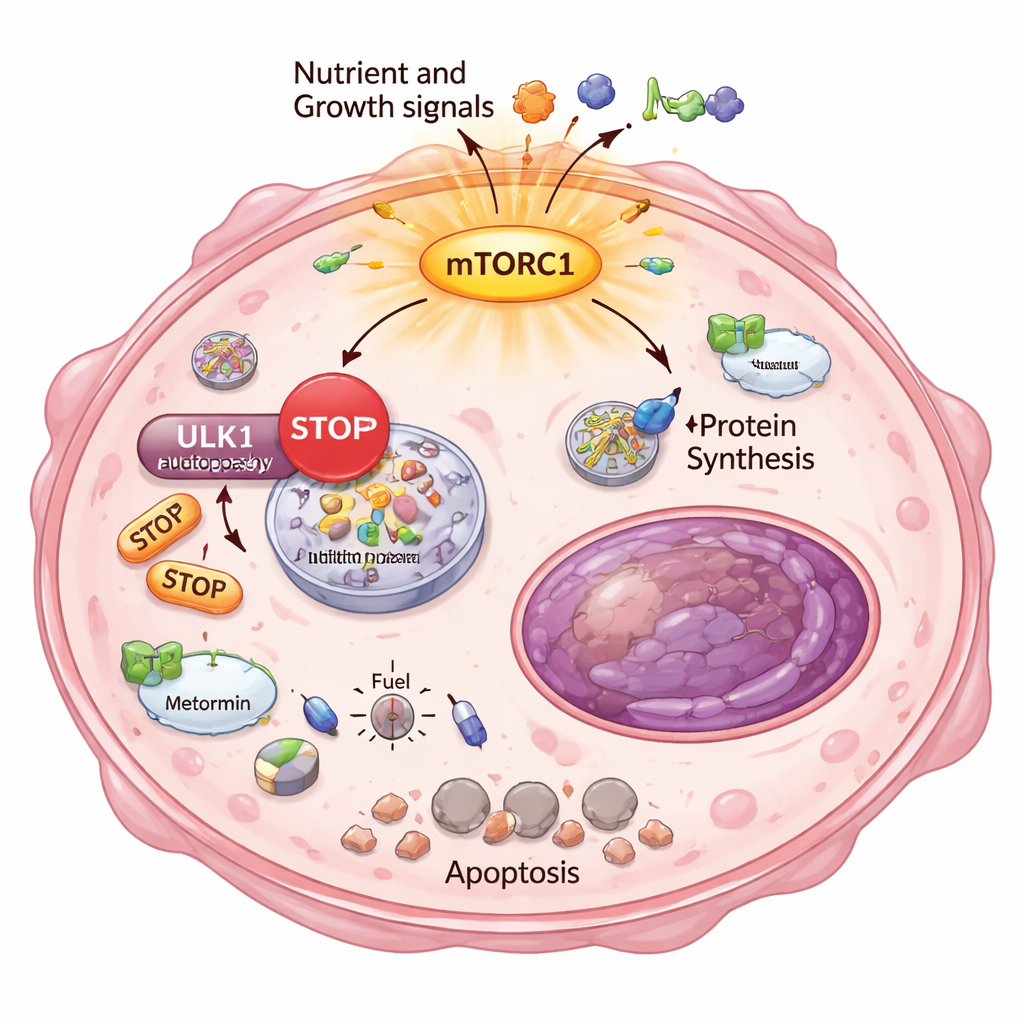
Autopulizia bloccata e crash energetico
Perché queste cellule fuggitive sarebbero così sensibili allo stress energetico? La risposta stava in un altro processo di sopravvivenza fondamentale: l’autofagia, il sistema interno di «riciclo e pulizia» della cellula. Normalmente, quando l’energia scarseggia, le cellule degradano e riutilizzano i propri componenti per restare in vita. I ricercatori hanno dimostrato che, nei cloni altamente resistenti, mTORC1 era iperattivo e poneva un freno chimico su ULK1, un avviatore chiave dell’autofagia. Usando un saggio reporter sensibile, hanno mostrato che queste cellule non riuscivano più ad attivare correttamente l’autofagia, neppure quando stimolate con farmaci metabolici. Di conseguenza, metformina e DCA provocarono una grave crisi energetica: si accesero i sensori di bassa energia, la sintesi lipidica venne bloccata e comparvero marcatori di morte cellulare irreversibile, specificamente nelle cellule fortemente resistenti.
Prove tratte da tumori reali di pazienti
I modelli di laboratorio non riflettono sempre ciò che accade nei pazienti, quindi il gruppo si è rivolto a campioni di tumore mammario umano. Hanno colorato più di cento tumori per un marcatore dell’attività di mTORC1 (4E-BP1 fosforilata) e per p62, una proteina che si accumula quando l’autofagia è bloccata. I tumori con alta attività di mTORC1 tendevano ad avere più p62, a sostegno dell’idea che un modello di «segnale di crescita sovraattivato più scarso riciclo» esista nei tumori mammari reali, non solo nelle linee cellulari. Questo suggerisce che una sottopopolazione di pazienti possa presentare tumori con la stessa debolezza metabolica osservata in laboratorio.
Cosa potrebbe significare per i trattamenti futuri
Per un pubblico non specialistico, il messaggio chiave è che quando i tumori mammari evolvono per sfuggire ai potenti inibitori di CDK4/6, possono anche ritrovarsi in un angolo metabolico. Attivando in modo permanente i segnali di crescita e disattivando il riciclo cellulare, questi tumori diventano fortemente dipendenti da un apporto energetico costante. Lo studio dimostra che questa configurazione può essere sfruttata con farmaci metabolici come metformina e DCA, già ben noti in altre malattie. È importante che gli autori propongano che semplici test tissutali per l’attività di mTORC1 e per i marcatori dell’autofagia possano aiutare a identificare le pazienti i cui tumori resistenti sono pronti per questo tipo di attacco metabolico, aprendo la strada a terapie di salvataggio più personalizzate dopo il fallimento degli inibitori di CDK4/6.
Citazione: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Parole chiave: cancro al seno, resistenza agli inibitori di CDK4/6, mTOR, autofagia, terapia metabolica