Clear Sky Science · it
Lo splicing che cambia l’isoforma oncogenica BCS1L sopprime la progressione del cancro ovarico interrompendo la funzione mitocondriale
Centrali elettriche all’interno delle cellule tumorali
Ogni cellula del nostro corpo dipende da piccole centrali elettriche chiamate mitocondri. Le cellule tumorali, che crescono e si diffondono rapidamente, sono particolarmente affamate di energia. Questo studio rivela come il cancro ovarico riorganizzi uno dei suoi principali aiutanti mitocondriali e mostra che attivare con delicatezza un “interruttore” molecolare su questo aiutante può affamare i tumori risparmiando in larga parte i tessuti sani.
Perché i tumori si affidano ai loro motori
Le cellule del cancro ovarico, come molti tumori, possono attingere flessibilmente a diverse fonti di energia. Analizzando grandi database di pazienti e profili a singola cellula, i ricercatori hanno scoperto che molti tumori ovarici mantengono i mitocondri in una modalità ad alto regime nota come fosforilazione ossidativa, o OXPHOS. I tumori con questa attività mitocondriale aumentata erano più aggressivi e più frequenti nelle malattie avanzate. Tra le molte proteine che costruiscono la macchina energetica mitocondriale, una è emersa con chiarezza: BCS1L, una chaperona che favorisce l’assemblaggio del Complesso III, un nodo centrale nella rete energetica della cellula. I tumori ad alto OXPHOS e alcuni sottotipi cellulari tumorali mostravano un’attività particolarmente pronunciata di BCS1L, suggerendo che le cellule cancerose facevano pesante affidamento su questo aiutante per mantenere i loro motori in funzione.
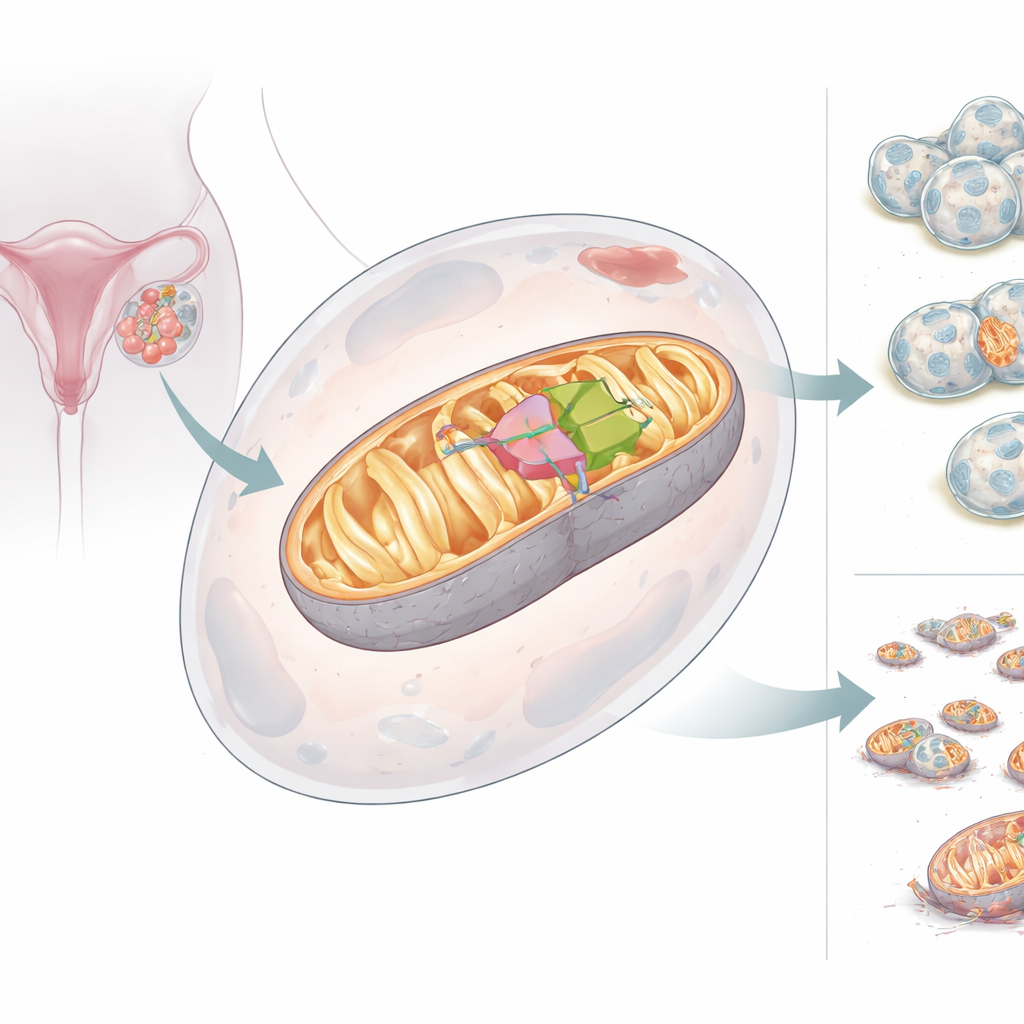
Due volti di un aiutante mitocondriale
Il gruppo ha scoperto che il gene BCS1L può produrre due versioni, o isoforme, della proteina. La forma a lunghezza intera, BCS1L-L, porta un tag di indirizzamento che la invia nei mitocondri, dove supporta il corretto assemblaggio del Complesso III e un’elevata produzione di energia. La forma più corta, BCS1L-S, è priva di un segmento chiave e non raggiunge i mitocondri; si trova invece nel fluido cellulare e nel nucleo e non sostiene la produzione energetica. Nei tessuti sani la versione corta è comune, ma nei tumori ovarici l’equilibrio si inverte: domina la forma lunga legata ai mitocondri. Quando le cellule sono state indotte a produrre più BCS1L-L, i loro mitocondri generavano più energia, mantenevano un potenziale di membrana più alto, producevano meno sottoprodotti ossidativi dannosi e resistevano alla morte cellulare. Se BCS1L veniva ridotto, i mitocondri frammentavano, la produzione di energia calava, le molecole ossidanti aumentavano e le cellule tumorali erano più soggette a morire.
Come il cancro riorganizza il messaggio
La produzione della versione lunga o corta di BCS1L dipende da come la cellula edita il suo messaggio di RNA, un processo chiamato splicing. I ricercatori hanno cercato proteine che si legano all’RNA di BCS1L e influenzano questa scelta. Hanno individuato USP39, un fattore di splicing già collegato a diversi tumori. Nelle cellule di cancro ovarico, USP39 si lega vicino al segmento di RNA che diventa l’esone 2 di BCS1L e ne favorisce l’inclusione, promuovendo quindi la versione lunga diretta ai mitocondri. Quando USP39 veniva silenziato, le cellule omettevano più frequentemente questo segmento, spostandosi verso la forma corta BCS1L-S. Questo cambiamento indeboliva il Complesso III, riduceva la respirazione mitocondriale e la produzione di ATP, aumentava lo stress ossidativo e innescava la morte delle cellule tumorali. Ripristinare BCS1L-L in queste cellule recuperava gran parte della funzione mitocondriale e della sopravvivenza, dimostrando che USP39 guida un interruttore mitocondriale critico in gran parte attraverso BCS1L.
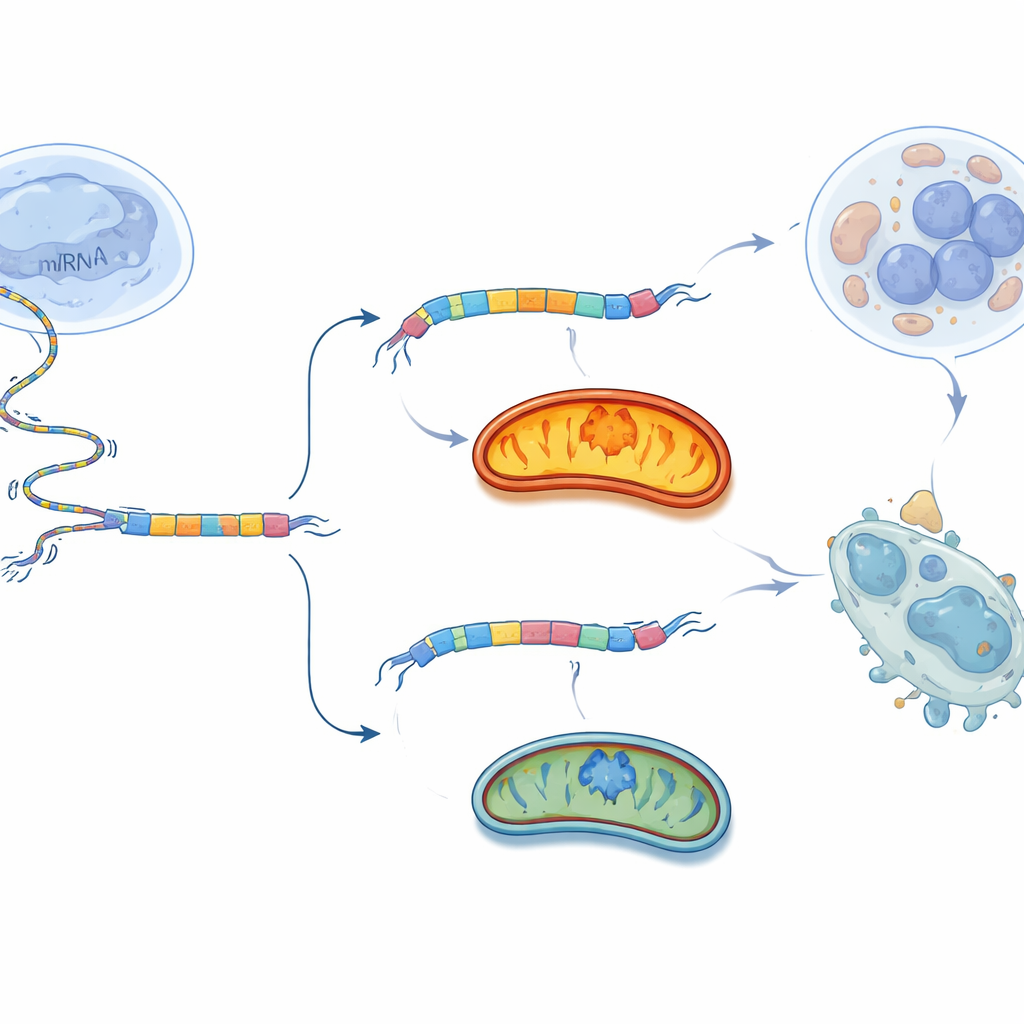
Usare l’interruttore contro il tumore
Piuttosto che bloccare i mitocondri in modo ampio, il che potrebbe danneggiare molti tessuti, il gruppo ha provato una tattica più chirurgica: spingere la scelta di splicing dello stesso BCS1L. Hanno progettato brevi frammenti di materiale genetico chiamati oligonucleotidi antisenso (ASO) che si legano proprio intorno all’esone 2 dell’RNA di BCS1L. Questi ASO agiscono come piccole mollette, cambiando il modo in cui la macchina di splicing legge il messaggio e incoraggiando la cellula a saltare l’esone 2. Nelle cellule di cancro ovarico coltivate in piastra, il miglior ASO riduceva fortemente la forma lunga BCS1L-L e aumentava la forma corta BCS1L-S. Di conseguenza, la respirazione mitocondriale e la produzione di ATP calavano, i livelli di ossidanti aumentavano e molte più cellule andavano incontro a morte programmata. Quando lo stesso ASO è stato iniettato in tumori ovarici in topi, la crescita tumorale rallentava e i tumori pesavano meno, con un effetto molto più marcato sulle cellule cancerose rispetto ai fibroblasti normali.
Cosa potrebbe significare per i pazienti
In termini semplici, questo lavoro mostra che molti tumori ovarici dipendono da una versione “turbo” di una proteina aiutante mitocondriale per alimentare la loro crescita. Un fattore di splicing, USP39, inclina la macchina di editing dell’RNA in modo che venga prodotta più di questa versione potenziata, mantenendo le centrali del tumore in ottime condizioni. Usando ASO progettati con precisione per riportare la scelta di splicing verso la versione più debole, i ricercatori possono compromettere selettivamente i mitocondri delle cellule tumorali, innescando la loro morte e lasciando la maggior parte delle cellule normali meno colpite. Sebbene la somministrazione di tali farmaci ASO ai tumori rimanga una sfida importante, questo studio indica l’interruttore di splicing di BCS1L come una leva promettente e altamente specifica per trattare il cancro ovarico.
Citazione: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Parole chiave: cancro ovarico, mitocondri, splicing dell'RNA, BCS1L, oligonucleotidi antisenso