Clear Sky Science · it
NSD2 inibisce l’espressione di PD-L1 tramite la fosforilazione ossidativa per controllare la sorveglianza immunitaria nel carcinoma epatocellulare
Perché questa storia sul cancro al fegato è importante
Il carcinoma epatocellulare, la forma più comune di tumore del fegato, viene spesso diagnosticato in fase avanzata e resiste a molti trattamenti. I farmaci immunoterapici che bloccano il “mantello di invisibilità” PD-L1 sulle cellule tumorali aiutano alcuni pazienti, ma non la maggioranza. Questo studio mette in luce un attore inatteso, una proteina chiamata NSD2, che collega il modo in cui le cellule del cancro epatico producono energia alla loro visibilità nei confronti del sistema immunitario. Comprendere questo legame potrebbe indicare nuovi modi per potenziare le terapie esistenti e per identificare i pazienti più propensi a beneficiarne.
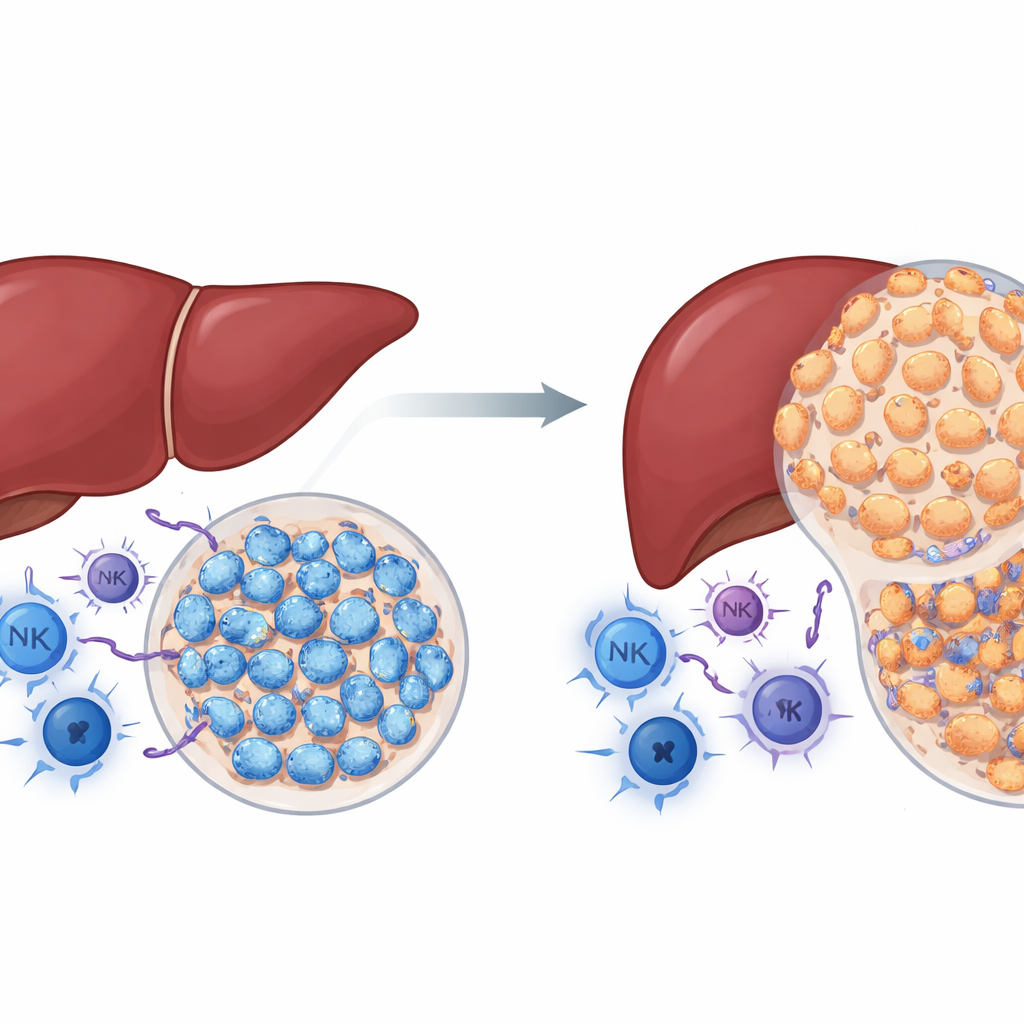
Un ruolo sorprendente per una proteina nota nel cancro
NSD2 è un enzima che modifica gli istoni, le proteine attorno alle quali è avvolto il DNA. In molti tumori, NSD2 è stato visto come un promotore della crescita tumorale. Gli autori si sono chiesti se lo stesso valga nel cancro del fegato. Utilizzando topi geneticamente modificati in cui NSD2 è attivato specificamente nelle cellule epatiche, hanno trattato gli animali con una sostanza chimica che induce in modo affidabile tumori al fegato. Contrariamente alle aspettative, i topi con sovraespressione di NSD2 hanno sviluppato molti meno tumori e di dimensioni inferiori rispetto ai topi normali, e i loro fegati mostravano meno danno, fibrosi e proliferazione cellulare. Allo stesso tempo, i tumori provenienti da fegati con NSD2 sovraespresso contenevano più cellule immunitarie antitumorali, inclusi linfociti T helper e citotossici e cellule natural killer. Questi risultati suggeriscono che, in presenza di un sistema immunitario integro, NSD2 si comporta meno come un acceleratore e più come un freno sul carcinoma epatocellulare.
Fabbriche di energia e uso del carburante nelle cellule tumorali
Per capire come NSD2 freni i tumori, il gruppo ha profilato l’attività genica nei tessuti epatici. Hanno scoperto che la sovraespressione di NSD2 attenuava fortemente i geni coinvolti nella fosforilazione ossidativa, il processo con cui i mitocondri — le “centrali elettriche” della cellula — generano energia usando l’ossigeno. Esperimenti successivi in linee cellulari di carcinoma epatocellulare murine e umane hanno mostrato che aumentare NSD2 riduceva l’espressione di molti geni della fosforilazione ossidativa, diminuiva il consumo di ossigeno e la produzione di ATP e abbassava il potenziale di membrana mitocondriale, segno di una minore attività mitocondriale. Contemporaneamente, queste cellule consumavano meno glucosio ma non spostavano il loro metabolismo verso la glicolisi, indicando una riduzione netta della produzione energetica. La perdita di NSD2 aveva gli effetti opposti, rafforzando la potenza mitocondriale e l’uso di carburante.
Come NSD2 riorganizza energia e visibilità immunitaria
Per approfondire, i ricercatori hanno combinato mappature cromatiniche a livello del genoma con dati di espressione genica e hanno identificato un insieme di geni attivati direttamente in presenza di NSD2. Due di questi, Camk2d e Prkce, sono noti per limitare l’attività mitocondriale. NSD2 aumentava una specifica marcatura istonica (H3K36me2) nei loro promotori, aumentandone l’espressione. Reintrodurre questi geni in cellule di carcinoma epatocellulare prive di NSD2 riduceva il consumo mitocondriale di ossigeno e la produzione di ATP, confermando che agiscono come freni a valle di NSD2 sulla fosforilazione ossidativa. È importante osservare che lavori precedenti avevano suggerito che mitocondri altamente attivi favoriscono alti livelli di PD-L1 sulle cellule tumorali. In linea con ciò, gli autori hanno rilevato che la sovraespressione di NSD2 riduceva i livelli di PD-L1, mentre la perdita di NSD2 aumentava PD-L1 nelle cellule tumorali epatiche e nel tessuto tumorale.
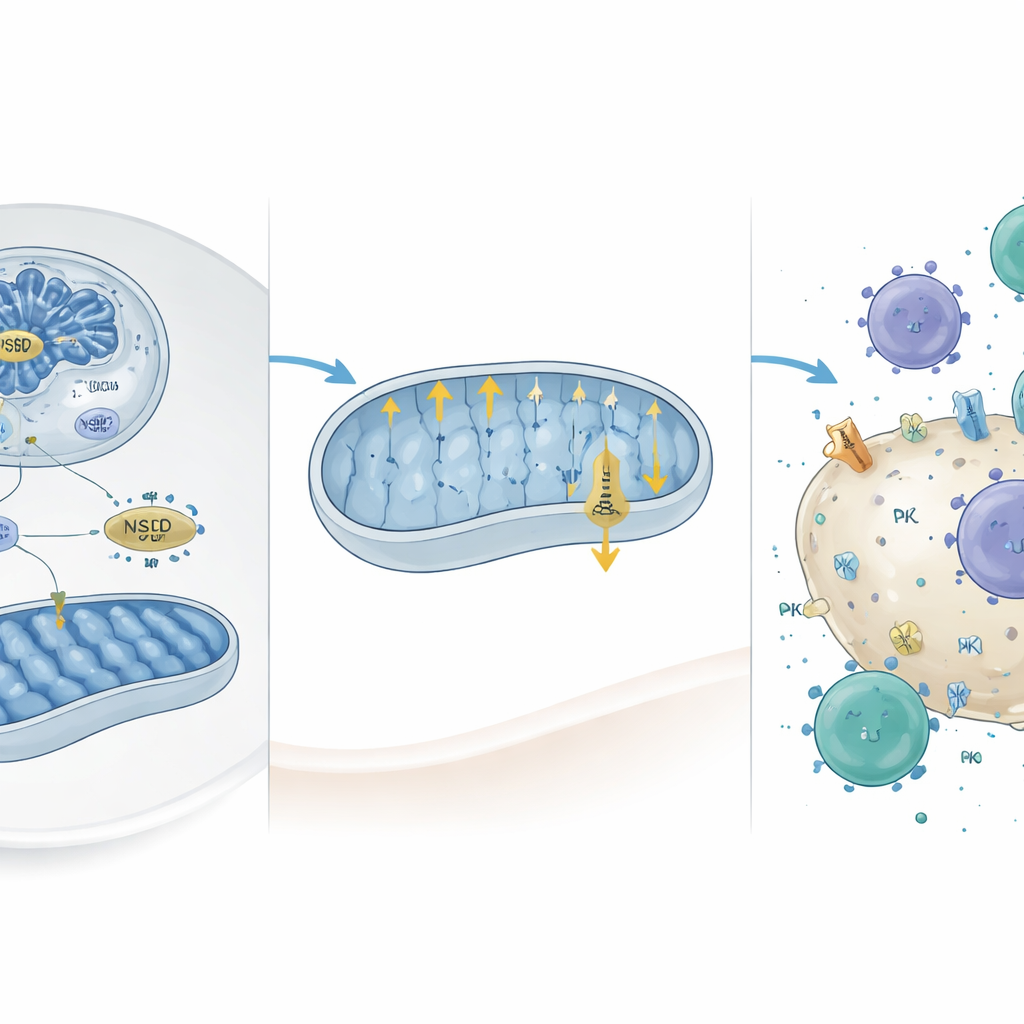
Abbassare lo scudo e risvegliare l’attacco immunitario
L’impatto funzionale di questi cambiamenti molecolari è stato testato in topi sottoposti a iniezioni epatiche di cellule tumorali ingegnerizzate per acquisire o perdere NSD2. Le cellule prive di NSD2 formarono rapidamente tumori più grandi, esprimevano più PD-L1 ed erano infiltrate da meno linfociti T e cellule natural killer, in particolare da meno linfociti T citotossici attivati. Quando i ricercatori bloccarono chimicamente il complesso V mitocondriale, un componente chiave della fosforilazione ossidativa, i livelli di PD-L1 nelle cellule carenti di NSD2 tornarono verso la normalità e le cellule immunitarie erano più efficaci nell’indurre la morte delle cellule tumorali. Analogamente, la sovraespressione di Camk2d o Prkce in cellule mancanti di NSD2, o il trattamento dei tumori con un anticorpo che blocca PD-L1, riduceva la dimensione tumorale e ripristinava l’infiltrazione delle cellule immunitarie. Nei dataset dei pazienti, una bassa espressione di NSD2 era associata a una sopravvivenza peggiore ma, in modo intrigante, a una risposta migliore alla terapia mirata su PD-L1, suggerendo che lo stato di NSD2 potrebbe aiutare a predire chi beneficia di tali farmaci.
Cosa significa per la cura futura del cancro al fegato
Per il lettore generale, il messaggio chiave è che questo studio ridefinisce NSD2 come un fattore oncosoppressore nel carcinoma epatocellulare, almeno in presenza di un sistema immunitario funzionante. Abbassando la produzione energetica cellulare basata sull’ossigeno, NSD2 riduce indirettamente PD-L1 sulle cellule tumorali, rimuovendo parte del loro mantello di invisibilità e permettendo alle cellule immunitarie di riconoscerle e attaccarle. Questa catena appena descritta NSD2–energia–PD-L1 suggerisce due idee pratiche: primo, i pazienti i cui tumori sono privi di NSD2 potrebbero essere candidati particolarmente adatti ai farmaci che bloccano PD-L1; secondo, combinare farmaci che inibiscono la produzione di energia mitocondriale con l’immunoterapia potrebbe offrire un’efficace strategia combinata contro il carcinoma epatocellulare.
Citazione: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Parole chiave: carcinoma epatocellulare, NSD2, fosforilazione ossidativa, PD-L1, immunoterapia tumorale