Clear Sky Science · it
La regolazione dello splicing di DDX39B mediata da SNRPD2 favorisce la progressione del cancro endometriale sopprimendo l’attivazione di esoni crittici di CTSC
Perché i messaggi nascosti nei geni del cancro contano
Il cancro endometriale, un tumore comune dell’utero, è in aumento a livello mondiale, eppure molti pazienti con malattia avanzata dispongono ancora di poche opzioni efficaci. Questo studio rivela come un processo sottile all’interno delle cellule — il modo in cui tagliano e ricuciono i messaggi genetici — possa guidare la crescita e la diffusione dei tumori endometriali. Mostrando un fragile “schema elettrico” su cui le cellule tumorali fanno affidamento, il lavoro indica nuove modalità per spegnere i tumori usando terapie genetiche di precisione.
Un cancro in crescita che necessita di nuove risposte
Il cancro endometriale è ormai il tumore ginecologico più frequente in molti Paesi occidentali, con casi e decessi in aumento sia in Occidente sia in Cina. Chirurgia, radioterapia, chemioterapia, terapie ormonali e immunoterapia sono tutte utilizzate, ma sono lungi dall’essere perfette. La rimozione dell’utero compromette la fertilità, i trattamenti ormonali spesso falliscono e i tumori aggressivi tendono a ricomparire. Queste sfide hanno spinto i ricercatori a scavare più a fondo nelle cellule tumorali alla ricerca di punti deboli molecolari che possano essere bersagliati con terapie più mirate.
La macchina dello splicing cellulare come punto debole
Per funzionare, i nostri geni vengono prima copiati in lunghe molecole di RNA che devono essere ritagliate e ricucite in un processo chiamato splicing. Macchine proteiche specializzate, chiamate spliceosomi, decidono quali porzioni mantenere e quali scartare, modificando di fatto il copione che le cellule usano per produrre proteine. Il gruppo si è concentrato su una componente dello spliceosoma chiamata SNRPD2, parte di una famiglia di proteine “Sm” che aiutano ad assemblare la macchina dello splicing. Analizzando ampi database di geni e proteine tumorali e campioni di pazienti, hanno scoperto che i livelli di SNRPD2 sono marcatamente più alti nei tumori endometriali rispetto al rivestimento uterino normale, e che i pazienti i cui tumori presentano più SNRPD2 tendono ad avere una prognosi peggiore.
Spegnere un editor maestro rallenta i tumori
Per verificare se SNRPD2 sia un semplice spettatore o un driver attivo, i ricercatori ne hanno ridotto l’espressione in linee cellulari di cancro endometriale coltivate in laboratorio. Quando SNRPD2 è stato silenziato, le cellule si dividevano più lentamente, formavano meno colonie ed erano meno capaci di muoversi e invadere membrane — comportamenti associati alla metastasi. Quando queste cellule modificate sono state impiantate in topi, i tumori risultanti erano molto più piccoli e mostravano meno cellule in divisione attiva. Importante, il team ha progettato oligonucleotidi antisenso — brevi frammenti di DNA sintetico con carattere farmacologico — che prendono di mira specificamente l’RNA di SNRPD2. In un modello xenotrapianto derivato da pazienti, in cui frammenti tumorali umani crescono in topi immunodeficienti, questi farmaci antisenso hanno ridotto drasticamente i livelli di SNRPD2 e la dimensione dei tumori, suggerendo che SNRPD2 potrebbe essere modulato farmacologicamente in modo clinicamente significativo.
Una catena in tre passaggi dall’errore di splicing alla crescita tumorale
Analizzando i dati genetici, gli investigatori hanno chiesto come la perdita di SNRPD2 riorganizzi i messaggi di RNA in tutto il genoma. Hanno scoperto che quando SNRPD2 è ridotto, un enzima chiave del processamento dell’RNA chiamato DDX39B comincia a funzionare in modo difettoso. Normalmente, DDX39B aiuta a rimuovere un introne specifico — un segmento di RNA che dovrebbe essere eliminato — dal proprio messaggio. In assenza di sufficiente SNRPD2, questo introne resta incluso, generando una versione difettosa dell’RNA di DDX39B che la cellula degrada rapidamente. Il calo di DDX39B ha poi un effetto a catena su un altro gene, CTSC, che codifica per un enzima proteolitico noto per sostenere la crescita e la diffusione tumorale. In condizioni normali, un esone nascosto “crittico” nell’RNA di CTSC viene ignorato, permettendo la produzione di una proteina CTSC completa e attiva. Con DDX39B ridotto, questo esone crittico viene incluso per errore, inserendo segnali di stop prematuri nell’RNA. Il messaggio CTSC malformato viene degradato prima di poter produrre proteina, e le cellule tumorali perdono parte della loro aggressività.
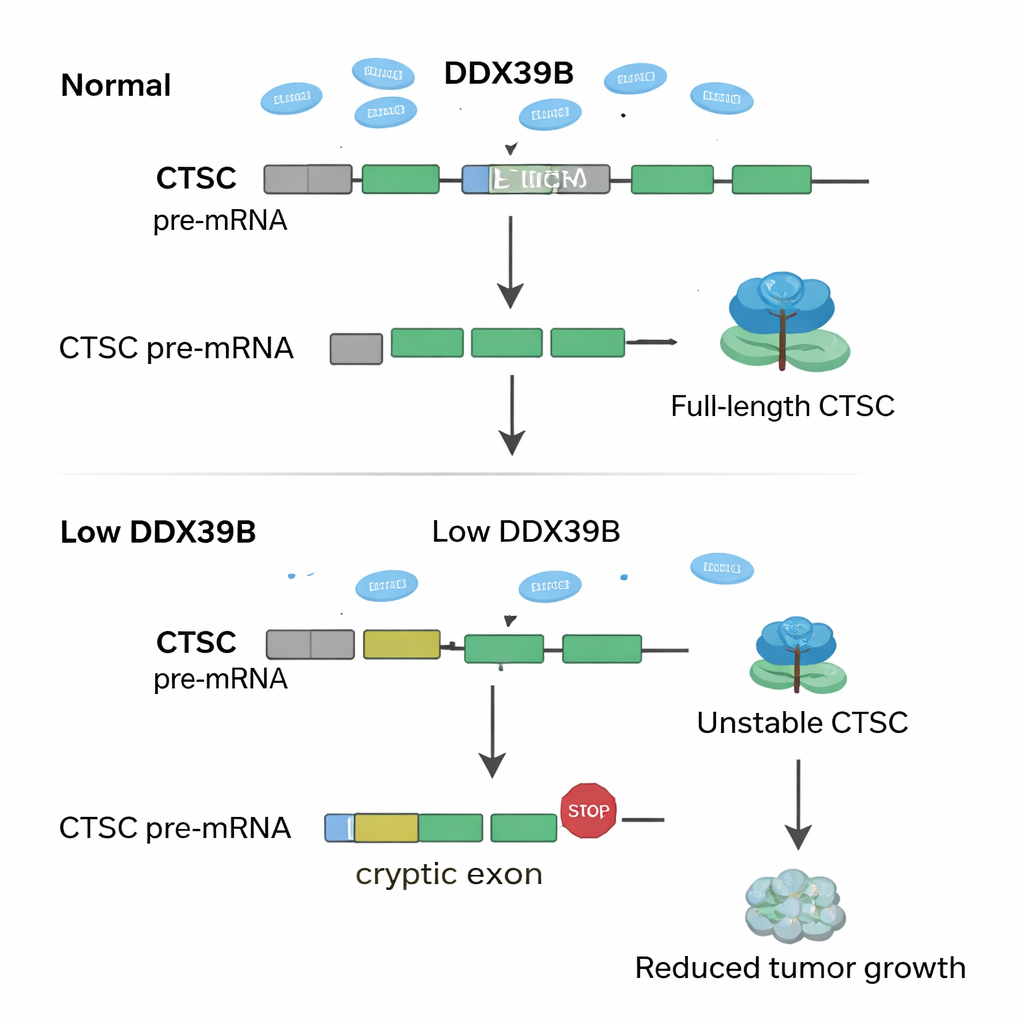
Cosa significa questo per i trattamenti futuri
In termini semplici, gli autori scoprono un sistema a catena — SNRPD2 → DDX39B → CTSC — che le cellule del cancro endometriale sfruttano per prosperare. Alti livelli di SNRPD2 mantengono abbondante DDX39B; DDX39B a sua volta impedisce a CTSC di utilizzare esoni crittici dannosi, preservando la proteina CTSC a piena potenza che favorisce la crescita e la diffusione del tumore. Quando SNRPD2 viene bloccato, questa catena crolla, i livelli di CTSC diminuiscono e i tumori si indeboliscono. Per i non specialisti, l’idea chiave è che le cellule tumorali dipendono da un editing dell’RNA molto preciso e che anche piccoli “errori” indotti possono avvelenare selettivamente la loro crescita. Mirare a SNRPD2 con farmaci antisenso, o forzare direttamente l’uso di esoni crittici in CTSC, potrebbe offrire nuove terapie più mirate per i pazienti con cancro endometriale.
Citazione: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Parole chiave: cancro endometriale, splicing dell'RNA, SNRPD2, DDX39B, CTSC