Clear Sky Science · it
La lisil ossidasi indotta da HIF2α protegge la gravidanza rimodellando i collageni all’interfaccia feto-materna
Perché l’utero deve prepararsi a un nuovo arrivo
Prima che una gravidanza possa instaurarsi, un embrione precoce deve compiere qualcosa di notevole: insinuarsi nella parete uterina e costruire un sistema di supporto vitale, la placenta. Questo articolo esplora come il tessuto materno si rimodelli silenziosamente per accogliere l’embrione, concentrandosi su come i bassi livelli di ossigeno e un enzima poco noto contribuiscano a preparare l’endometrio. Comprendere questa danza finemente regolata può chiarire perché alcune gravidanze falliscono molto presto e suggerire nuovi modi per prevenire infertilità e complicazioni gestazionali.
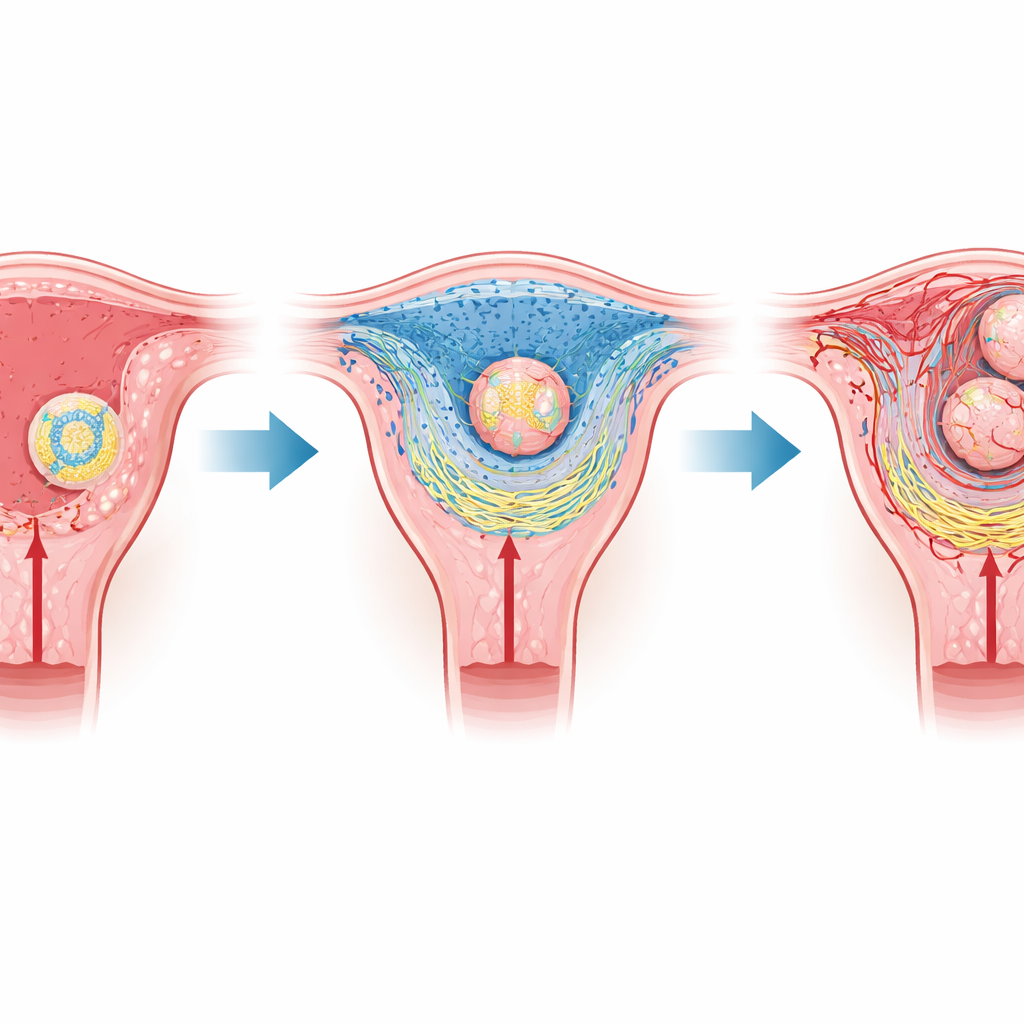
Un incontro delicato tra madre ed embrione
Nei mammiferi come topi e umani, la fase iniziale della gravidanza dipende dall’impianto, quando l’embrione si attacca e poi invade l’endometrio. L’embrione è avvolto da uno strato di cellule specializzate che poi formeranno la placenta, mentre il tessuto materno si trasforma in uno strato cuscinetto chiamato decidua. Più vicino all’embrione si trova una sottile regione nota come zona deciduale primaria, priva di vasi sanguigni e quindi povera di ossigeno. Studi precedenti hanno mostrato che questa nicchia naturalmente ipossica favorisce l’impianto, ma non era chiaro come una condizione fisica così semplice potesse riorganizzare interi tessuti.
La bassa ossigenazione come interruttore nascosto
Gli autori hanno utilizzato una tecnica potente detta trascrittomica spaziale, che mappa l’attività genica direttamente sui tagli tissutali, per studiare gli uteri di topo nei giorni in cui gli embrioni si attaccano e invadono. Si sono concentrati su una proteina chiamata HIF2α, che si attiva in condizioni di bassa ossigenazione e funziona come un interruttore genetico. Nei topi normali, le cellule della zona deciduale primaria mostravano una forte attivazione di geni legati all’ipossia e alla costruzione del materiale di impalcatura circostante, inclusi i collageni che costituiscono la matrice extracellulare. Quando HIF2α è stato rimosso solo dall’utero, la disposizione complessiva dei tipi cellulari appariva sorprendentemente normale. Ma a elevata risoluzione la rete di collagene risultava disorganizzata, la superficie epiteliale non si apriva correttamente e le cellule embrionali faticavano a penetrare il tessuto materno.
Un enzima che reticola l’impalcatura
Approfondendo, il gruppo ha identificato un attore chiave a valle di HIF2α: la lisil ossidasi, o Lox, un enzima che reticola chimicamente le fibre di collagene e contribuisce a irrigidire e stabilizzare i tessuti. Nelle gravidanze normali, i livelli di Lox aumentavano bruscamente intorno agli embrioni proprio quando questi iniziavano a invadere. Negli uteri privi di HIF2α, l’espressione di Lox calava e le fibre di collagene apparivano frammentate anziché costituire una fitta maglia. Per testare direttamente l’importanza di Lox, i ricercatori hanno generato topi in cui Lox era eliminata solo nell’utero. Queste femmine restavano gravide meno spesso, ospitavano meno embrioni e mostravano frequentemente segni di perdita embrionale e sanguinamento in stadi più avanzati della gestazione, nonostante i primi passaggi di attacco e ispessimento tissutale sembrassero inizialmente normali.
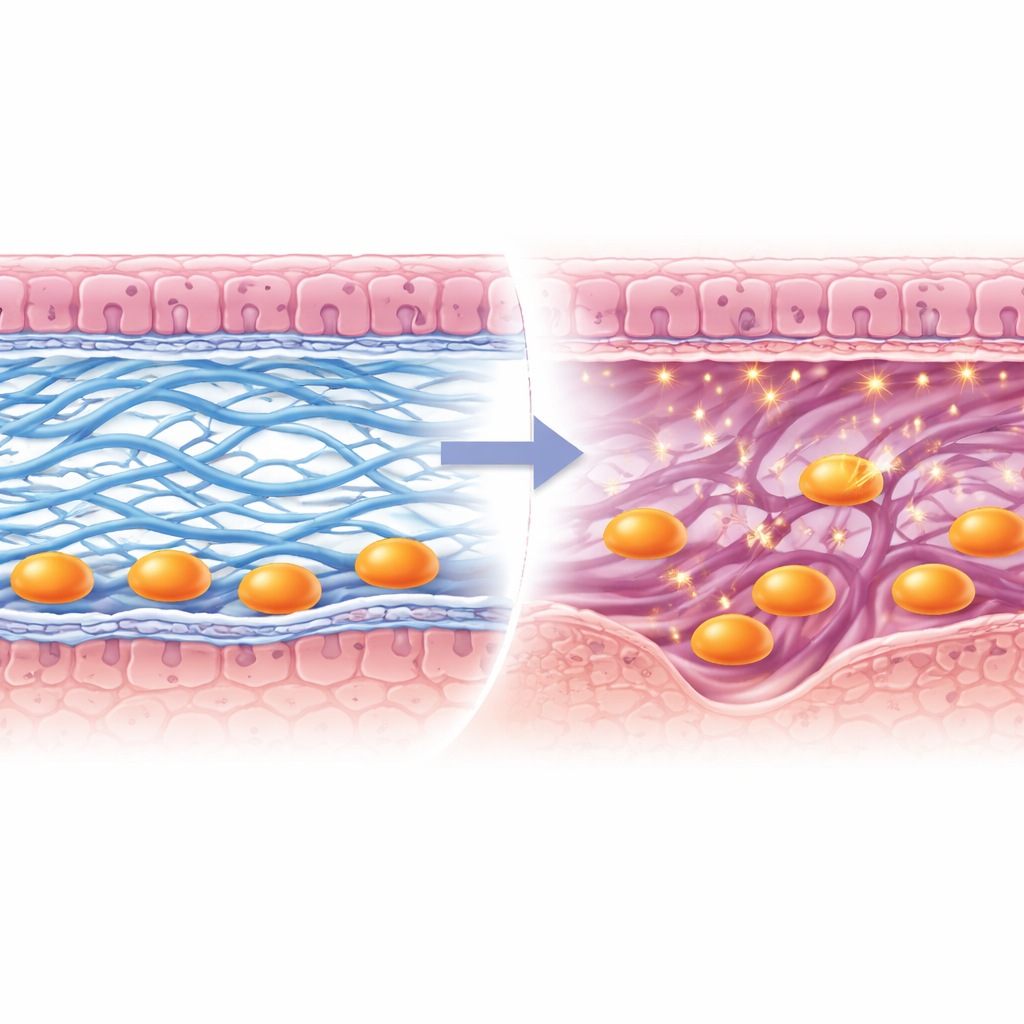
Aprire un varco per la placenta
Imaging attento ha rivelato cosa andava storto quando Lox mancava. Una sottile lamina ricca di proteine detta membrana basale, che normalmente si degrada per permettere il passaggio delle cellule embrionali, restava in gran parte intatta. Le fibre di collagene di tipo I nello stroma sottostante non formavano fascetti robusti e continui, mentre il collagene di tipo IV nella membrana basale non veniva rimosso correttamente vicino alle cellule invasive. Di conseguenza, le cellule trofoblastiche—i pionieri di origine embrionale che costruiscono la placenta—restavano intrappolate in superficie invece di scavare nel tessuto materno. Il gruppo ha anche osservato che un enzima che taglia il collagene, Mmp9, non veniva attivato in questi trofoblasti, ostacolandone ulteriormente la progressione. Col tempo, le strutture placentari si formavano male, gli embrioni crescevano in modo anomalo e il successo della gravidanza diminuiva.
Cosa significa per la salute della gravidanza
Punti messi insieme, i risultati delineano una catena di eventi in cui la bassa ossigenazione nella zona di impianto precoce attiva HIF2α, che a sua volta potenzia Lox. Lox rimodella e reticola le fibre di collagene e contribuisce allo smantellamento della membrana basale, permettendo anche l’attivazione di enzimi come Mmp9 per fare spazio. Questo rimodellamento fornisce sia un’impalcatura strutturale sia una porta aperta per le cellule trofoblastiche che devono invadere e costruire la placenta. Per un lettore non specialistico, il messaggio è che il successo della gravidanza dipende non solo da embrioni sani e ormoni, ma anche dalla riorganizzazione silenziosa dell’architettura tissutale materna. Le interruzioni di questo asse ipossia–HIF2α–Lox potrebbero essere alla base di alcuni casi di infertilità inspiegata, aborto spontaneo e disturbi legati a una scarsa invasione placentare, suggerendo nuovi marker diagnostici e bersagli terapeutici per sostenere la gravidanza precoce.
Citazione: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Parole chiave: impianto dell’embrione, matrice extracellulare uterina, lisil ossidasi, invasione trofoblastica, sviluppo della placenta