Clear Sky Science · it
Mirare la fosfatasi mitocondriale PGAM5 attenua la ferroptosi e la pancreatite acuta aumentando l’espressione di FSP1 mediata da NRF2
Perché le cellule stressate e i pancreas dolenti sono importanti
Quando le cellule sono sottoposte a uno stress eccessivo, possono morire in modi che danneggiano l’intero organismo. Una di queste modalità, chiamata ferroptosi, è guidata dal ferro e da reazioni chimiche incontrollate che ossidano i lipidi delle membrane cellulari. Questo processo è stato collegato a lesioni d’organo, inclusa una condizione dolorosa e talvolta letale nota come pancreatite acuta. Lo studio alla base di questo articolo individua un interruttore di controllo chiave all’interno dei mitocondri — le centrali energetiche della cellula — che può modulare la ferroptosi, e dimostra come bloccare questo interruttore possa proteggere il pancreas in un modello murino.
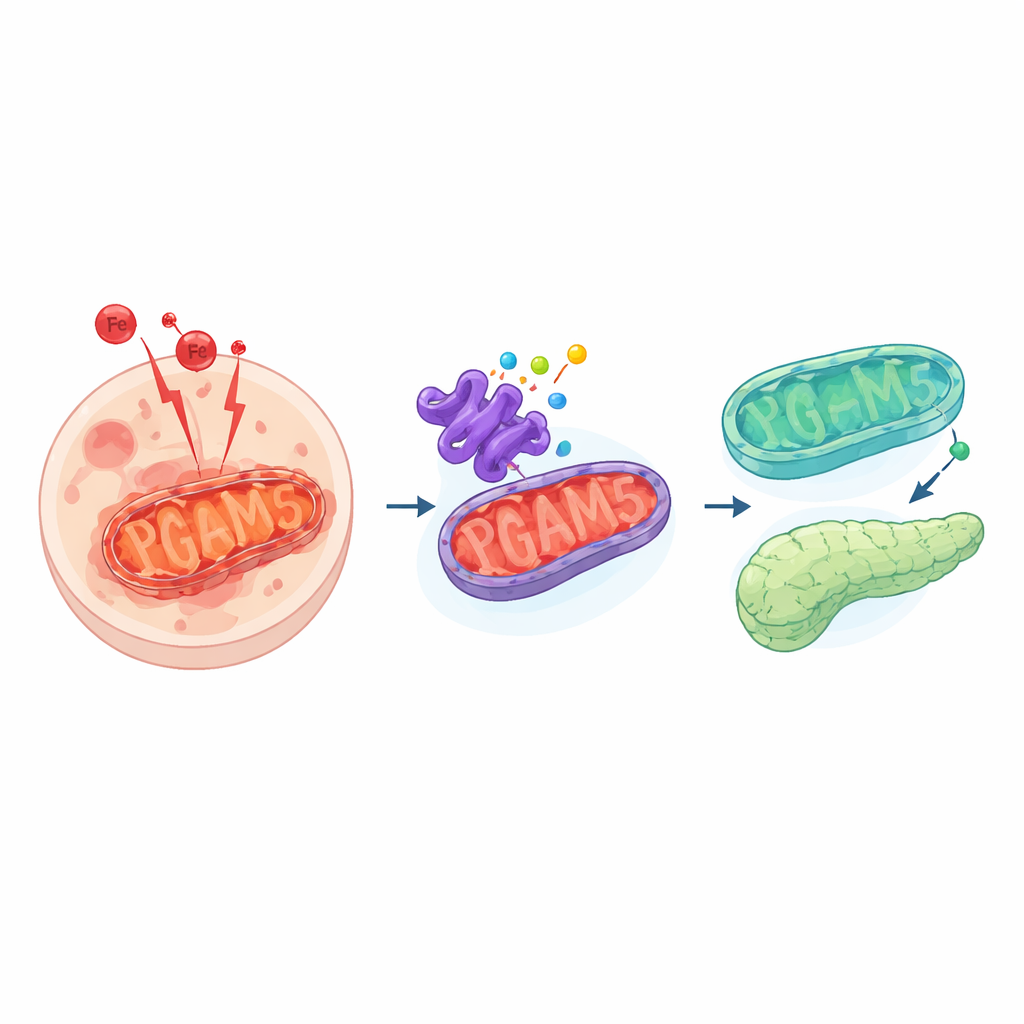
Una forma pericolosa di morte cellulare
La ferroptosi è diversa dalle forme di morte cellulare più familiari, come l’apoptosi. Invece di una distruzione ordinata, le cellule che subiscono ferroptosi affrontano una tempesta di reazioni guidate dal ferro che rendono rancidi i lipidi delle membrane. Questo genera sottoprodotti tossici e perforazioni nelle membrane che finiscono per uccidere la cellula. Normalmente, le cellule tengono la situazione sotto controllo con sistemi protettivi che disattivano queste specie reattive. Quando tali sistemi falliscono o vengono travolti, la ferroptosi può propagare il danno nei tessuti, contribuendo a malattie che vanno dal cancro all’insufficienza d’organo.
Un interruttore mitocondriale nel mirino
I ricercatori si sono concentrati su una proteina chiamata PGAM5, che si trova sulla faccia interna dei mitocondri e funge da hub di segnalazione. PGAM5 aiuta a controllare la morfologia mitocondriale, risponde allo stress e influenza il modo in cui le cellule gestiscono l’ossidazione. Sorprendentemente, quando il gruppo ha ridotto PGAM5 o ha forzato la sua sovraespressione, le cellule sono diventate più resistenti alla ferroptosi. L’inibizione chimica di PGAM5, il knockdown genetico e la sovraespressione hanno tutti ridotto l’accumulo di sottoprodotti lipidici dannosi e la morte cellulare indotta da un farmaco che provoca ferroptosi. Ciò ha rivelato che il sistema è finemente regolato: sia una quantità troppo bassa sia una troppo alta di PGAM5 spingono le cellule verso uno stato più protetto.
Attivare uno scudo interno
Analizzando più a fondo, gli autori hanno scoperto che l’influenza di PGAM5 passa attraverso un asse protettivo che coinvolge altri due attori: NRF2 e FSP1. NRF2 è un regolatore maestro che, quando attivo nel nucleo, attiva un ampio insieme di difese antiossidanti. FSP1 è uno dei suoi effettori a valle che aiuta a rigenerare un antiossidante liposolubile, bloccando il danno lipidico alla membrana cellulare. Quando i livelli di PGAM5 venivano modificati, le cellule incrementavano sia i livelli di trascritto sia quelli proteici di NRF2, e NRF2 si spostava più facilmente dal citoplasma al nucleo. Lì aumentava la produzione di FSP1. Bloccare FSP1 o NRF2 annullava la protezione, ripristinando la sensibilità alla ferroptosi, il che dimostra che la catena PGAM5–NRF2–FSP1 è essenziale per la resilienza osservata.
Lo stress energetico come messaggero nascosto
Lo studio ha anche rivelato come lo stress mitocondriale venga tradotto in questa risposta protettiva. Disgregare PGAM5 disturbava l’equilibrio mitocondriale e alterava la valuta energetica della cellula: il rapporto tra molecole a bassa energia (AMP e ADP) e l’ATP ad alta energia aumentava, segnalando stress energetico. Questo, a sua volta, attivava l’enzima sensore energetico AMPK. L’AMPK attivata modificava direttamente NRF2 in modo da favorirne l’ingresso nel nucleo, incrementando ulteriormente la produzione di FSP1. Quando l’AMPK veniva rimossa dal sistema, NRF2 non si accumulava più nel nucleo, i livelli di FSP1 diminuivano e le cellule soccombevano di nuovo alla ferroptosi. Dunque, PGAM5 collega lo stato mitocondriale a una risposta energetica e antiossidante più ampia che protegge le cellule dalla morte indotta dal ferro.
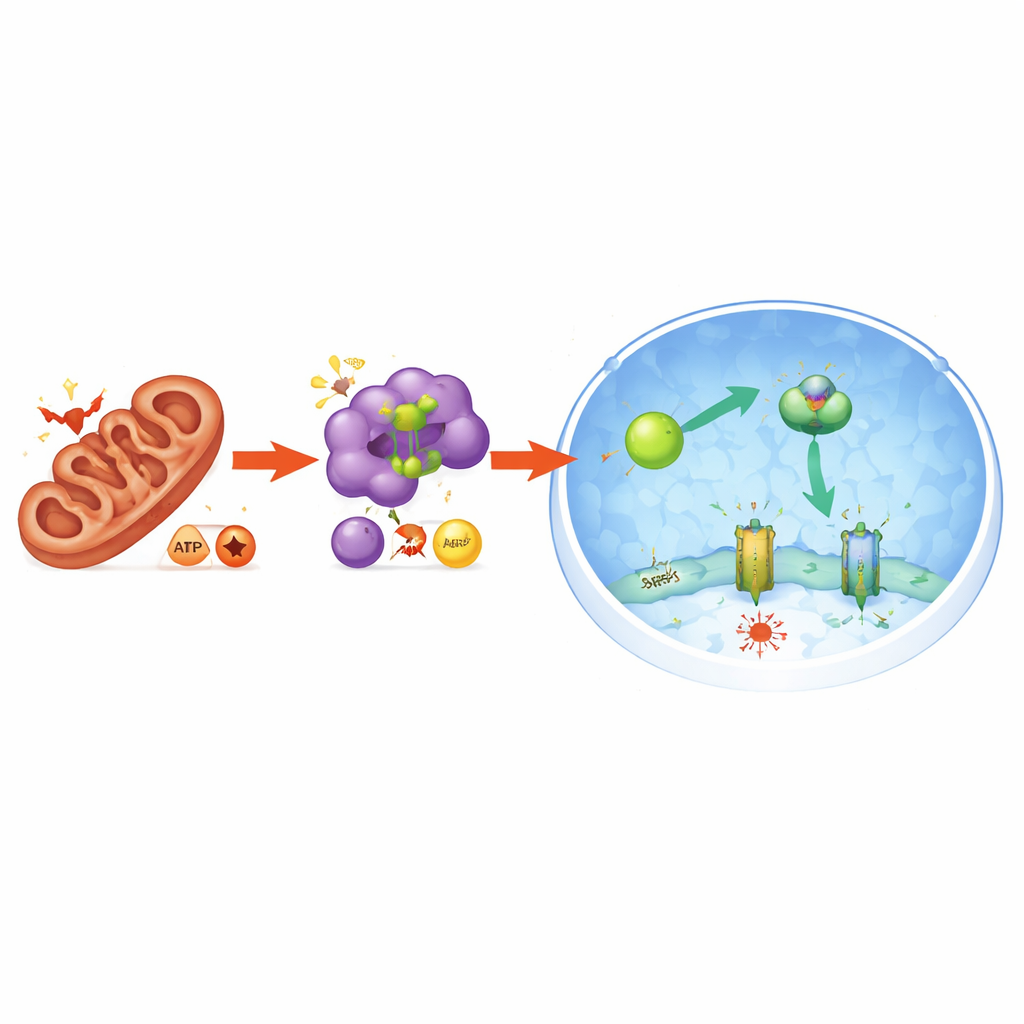
Proteggere il pancreas negli animali vivi
Per verificare se questo meccanismo ha rilevanza in un organo intero, gli scienziati hanno utilizzato un modello murino di pancreatite acuta indotta da dosi elevate dell’aminoacido arginina. In questo modello, il pancreas mostra danni estesi, livelli elevati nel sangue di enzimi che segnalano lesione tissutale e un’ondata di molecole infiammatorie. Anche i marcatori della perossidazione lipidica — una firma della ferroptosi — aumentavano nettamente nel pancreas. Il trattamento dei topi con un composto inibitore di PGAM5 ha attenuato questi sintomi: i marcatori ematici di danno sono diminuiti, il tessuto pancreatico appariva più sano al microscopio e i segnali infiammatori si riducevano. Allo stesso tempo, i marcatori di ferroptosi calavano, mentre aumentavano l’attività di AMPK e i livelli di NRF2 e FSP1 nel pancreas, in linea con la via protettiva osservata in coltura cellulare.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro identifica PGAM5 come un punto di controllo centrale che collega lo stress mitocondriale, lo stato energetico cellulare e un potente programma antiossidante che blocca la ferroptosi. Riducendo l’attività di PGAM5, le cellule attivano AMPK e NRF2, aumentano FSP1 e resistono meglio al danno lipidico indotto dal ferro. Nei topi, questa strategia riduce il danno pancreatico nella pancreatite acuta. Per il lettore non specialistico, il messaggio è che i ricercatori hanno individuato un nuovo “interruttore” interno che può prevenire una forma distruttiva di morte cellulare. Pur restando molto da fare prima dell’applicazione clinica, mirare a PGAM5 o ai suoi partner a valle potrebbe aprire nuove strade per trattare condizioni in cui ferroptosi e fallimento mitocondriale esercitano un ruolo dannoso.
Citazione: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Parole chiave: ferroptosi, mitocondri, pancreatite acuta, stress ossidativo, morte cellulare