Clear Sky Science · it
La ubiquitinazione di mH2A1 mediata da UBE3A attiva la trascrizione di TERT per promuovere la resistenza alla senescenza nel carcinoma pancreatico
Perché questa ricerca è importante per i pazienti
Il carcinoma pancreatico è tra i tumori più letali, in parte perché le cellule tumorali sono particolarmente abili a eludere i freni naturali dell’invecchiamento. Questo studio scopre un “circuito di sabotaggio” molecolare nascosto che aiuta le cellule del pancreas a restare giovani, continuare a dividersi e resistere alle terapie. Comprendendo questo circuito, i ricercatori indicano un nuovo modo per indurre la senescenza in queste cellule e poi eliminarle selettivamente, aprendo la strada a terapie combinate più intelligenti.
La senescenza come freno naturale ai tumori
Tutte le cellule portano un orologio interno che alla fine le induce a smettere di dividersi, un processo noto come senescenza. Nelle lesioni pancreatiche precoci, questo orologio può rallentare lo sviluppo tumorale mettendo le cellule precancerose in una pensione permanente. Molti trattamenti antitumorali funzionano anche in parte costringendo le cellule tumorali in questo stato di invecchiamento. Tuttavia, se queste cellule senescenti non vengono rimosse, possono alimentare l’infiammazione e favorire la ricomparsa del cancro. Da qui l’idea terapeutica emergente: prima indurre la senescenza nelle cellule tumorali, poi eliminare quelle cellule invecchiate con farmaci “senolitici” che sono particolarmente tossici per esse.
Un enzima promotore del cancro sotto i riflettori
Per trovare geni che aiutano le cellule del carcinoma pancreatico a sfuggire alla senescenza, il gruppo ha analizzato grandi banche dati di pazienti e poi ha validato i risultati in campioni tumorali e linee cellulari. Hanno individuato una proteina chiamata UBE3A, un enzima che etichetta altre proteine per la loro distruzione. I livelli di UBE3A erano molto più elevati nei tumori pancreatici rispetto al tessuto normale circostante, e i pazienti con maggior espressione di UBE3A tendevano ad avere tumori più grandi, più avanzati e una sopravvivenza peggiore. In colture cellulari, l’aumento di UBE3A accelerava la crescita, riduceva i marcatori classici della senescenza cellulare e diminuiva le secrezioni infiammatorie tipiche delle cellule senescenti. Il silenziamento di UBE3A aveva l’effetto opposto e, nei modelli murini, riduceva drasticamente la crescita tumorale e le metastasi epatiche. 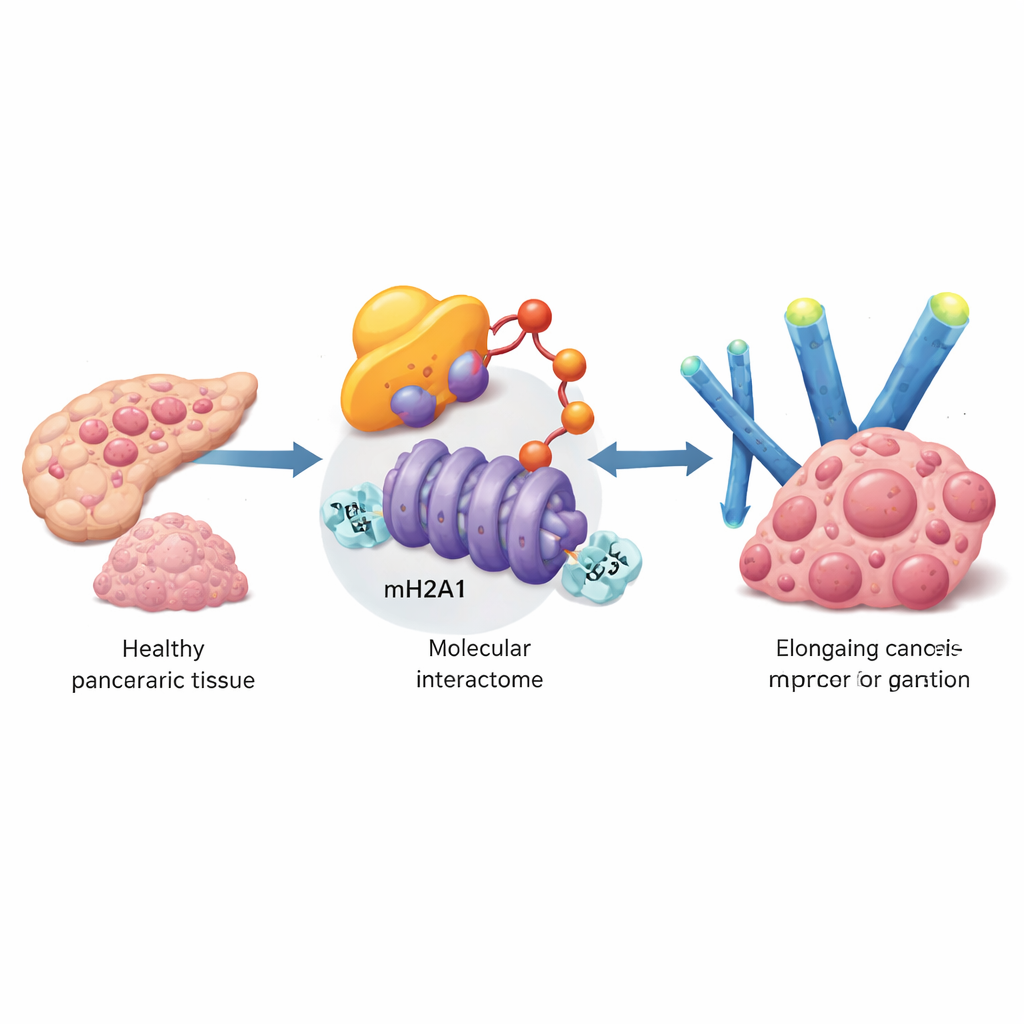
Come le cellule tumorali cancellano un freno cromatinico
Addentrandosi nei meccanismi, i ricercatori hanno chiesto su quali molecole agisca UBE3A. Usando sofisticati screening con spettrometria di massa, hanno scoperto che UBE3A si lega e coniuga chimicamente una variante istonica speciale chiamata macroH2A1 (mH2A1), che aiuta a compattare il DNA e normalmente funge da freno sull’attività genica. UBE3A attacca una catena di tag “distruggimi” a mH2A1 in una posizione specifica, inducendone la degradazione tramite la macchina cellulare di smaltimento delle proteine. Nei tumori pancreatici, i livelli di mH2A1 erano più bassi dove UBE3A era alto, e il ripristino di mH2A1 contrastava la capacità di UBE3A di bloccare la senescenza e promuovere la crescita tumorale. Questo rivela un passaggio chiave: le cellule del carcinoma pancreatico rimuovono un segno cromatinico protettivo usando UBE3A per eliminare mH2A1.
Sbloccare la telomerasi per mantenere le cellule giovani
La domanda successiva era quali geni venissero derepressi quando mH2A1 viene rimosso. Combinando RNA‑seq e mappe dei legami al DNA, il gruppo ha identificato il gene della telomerasi TERT come bersaglio centrale. La telomerasi mantiene i cappucci protettivi alle estremità dei cromosomi, permettendo alle cellule di continuare a dividersi invece di entrare in senescenza. Lo studio mostra che mH2A1 si trova normalmente in una regione potenziatrice (enhancer) all’interno del gene TERT, dove recluta un altro enzima, EZH2, per depositare un marchio chimico repressivo sugli istoni vicini. Questa combinazione mantiene TERT spento e lascia che i telomeri si accorcino. Quando UBE3A distrugge mH2A1, il complesso repressivo si dissolve, l’enhancer diventa attivo, TERT si accende, i telomeri vengono mantenuti e le cellule del carcinoma pancreatico acquisiscono resistenza all’invecchiamento. Forme mutanti di UBE3A incapaci di etichettare le proteine, o mH2A1 mutante non suscettibile all’etichettatura, interrompono questo circuito e ripristinano il freno della senescenza.
Abbinare l’induzione della senescenza alla pulizia senolitica
Infine, i ricercatori hanno testato se questa via potesse essere sfruttata terapeuticamente. L’inibizione di UBE3A ha spinto le cellule del carcinoma pancreatico verso la senescenza e ha aumentato la loro dipendenza dalle proteine anti‑morte della famiglia BCL‑2 — una vulnerabilità nota delle cellule senescenti. Il gruppo ha quindi combinato l’inibizione di UBE3A con ABT‑263, un farmaco senolitico che prende di mira queste proteine di sopravvivenza. Nelle cellule in coltura, la combinazione ha indotto molte più cellule tumorali ad andare incontro ad apoptosi rispetto a ciascun trattamento da solo. Nei modelli murini, i tumori con UBE3A ridotto si sono ridotti ancora di più quando gli animali hanno ricevuto ABT‑263, e i marcatori di proliferazione all’interno dei tumori sono calati nettamente. 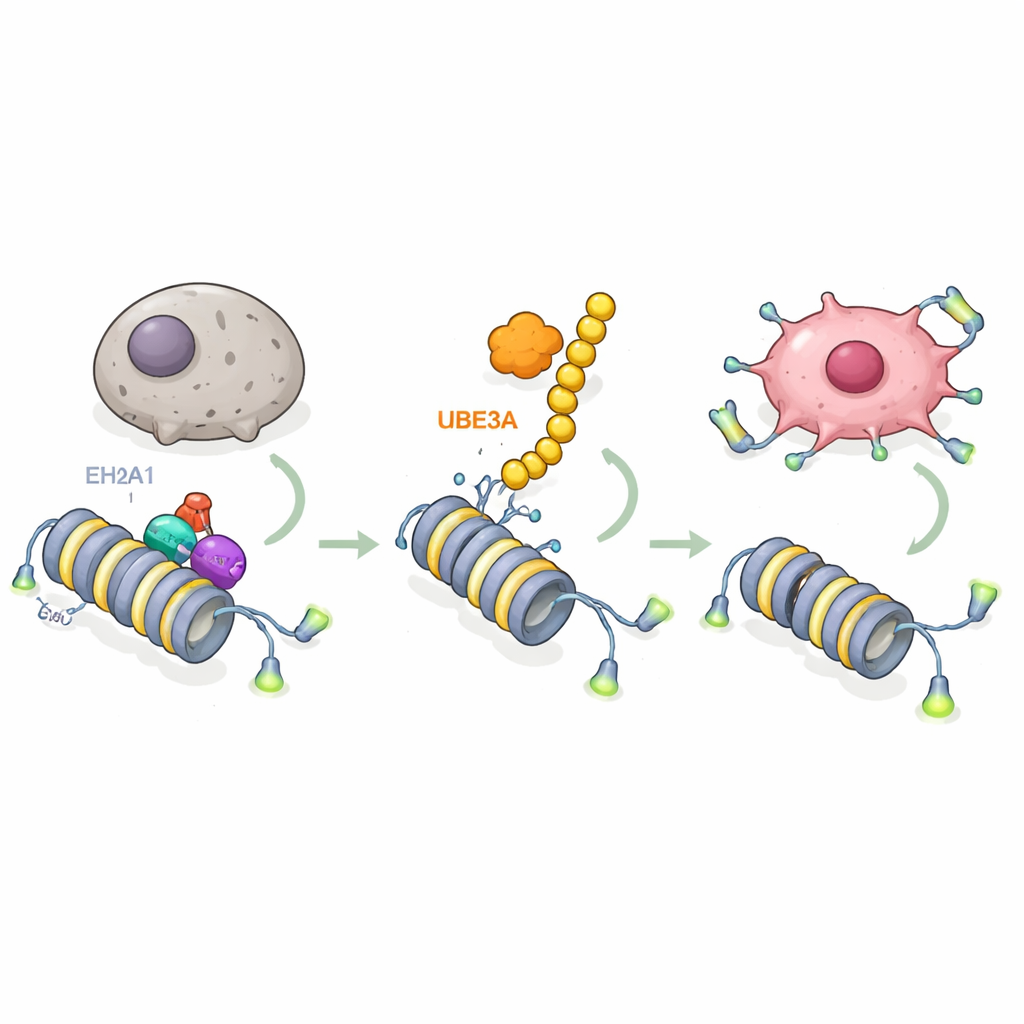
Cosa significa per i trattamenti futuri
Questo lavoro rivela una catena dettagliata di eventi tramite cui le cellule del carcinoma pancreatico evitano l’invecchiamento: UBE3A distrugge il freno cromatinico mH2A1, il che a sua volta solleva la repressione del gene della telomerasi TERT e aiuta a mantenere i telomeri, permettendo alle cellule di continuare a dividersi. Mirando a UBE3A, i medici potrebbero essere in grado di riattivare il programma naturale di invecchiamento cellulare e poi usare farmaci senolitici come ABT‑263 per eliminare selettivamente queste cellule tumorali vulnerabili e invecchiate. Sebbene siano necessari ulteriori studi per tradurre questo meccanismo in terapie per i pazienti, l’asse UBE3A–mH2A1–TERT offre una promettente nuova leva su uno dei tumori più resistenti ai trattamenti.
Citazione: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Parole chiave: carcinoma pancreatico, senescenza cellulare, telomerasi, ligasi dell’ubiquitina, terapia senolitica