Clear Sky Science · it
Un piccolo inibitore molecolare della proteina GTPasi ARF1 limita la crescita e le metastasi di cellule tumorali del fegato e del colon
Perché questa ricerca è importante
I tumori del fegato e del colon sono tra i più letali, e i trattamenti attuali spesso riducono le masse a fronte di effetti collaterali pesanti. Questo studio esplora un tipo di farmaco che non si limita a intossicare le cellule a rapida proliferazione, ma che piuttosto penetra nelle cellule tumorali e scardina un «centro di controllo» proteico su cui esse fanno affidamento per crescere e diffondersi. Mirando a questo hub, il composto sperimentale punta a rallentare la crescita del tumore risparmiando il tessuto sano.
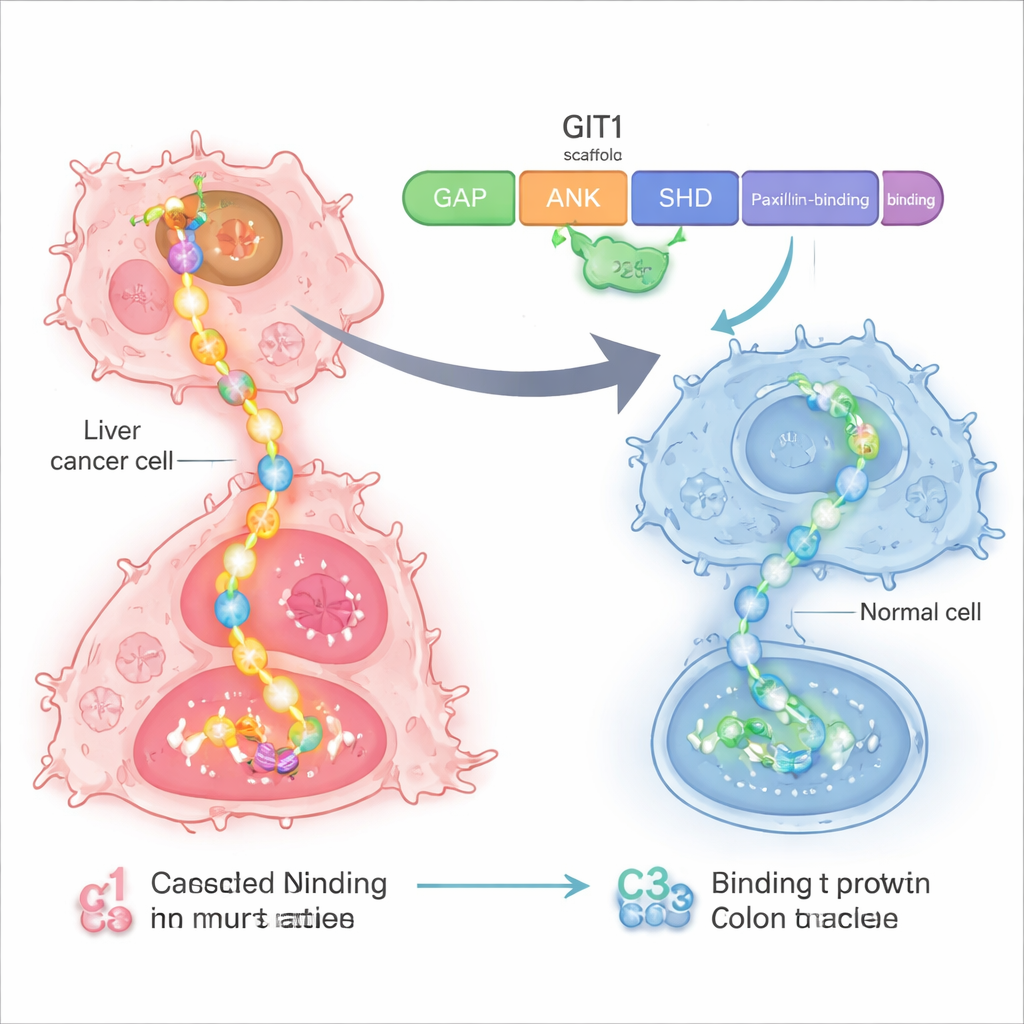
Un hub di controllo vulnerabile all’interno delle cellule tumorali
I ricercatori si sono concentrati su una proteina chiamata GIT1, che funziona come una impalcatura o una ciabatta elettrica all’interno della cellula. Nei tumori del fegato e del colon, GIT1 e la sua proteina partner MAT2B sono sovraespressi. Insieme assemblano vari componenti di una via di crescita majeure nota come RAS–RAF–MEK–ERK, una catena di segnali che istruisce le cellule a dividersi e migrare. Lavori precedenti avevano mostrato che quando GIT1 e MAT2B sono abbondanti, i tumori di fegato e colon crescono più rapidamente e si diffondono più facilmente, mentre la riduzione di queste proteine rallenta la crescita tumorale. Questo ha reso lo scaffold GIT1–MAT2B un bersaglio interessante per una terapia più precisa.
Progettare una piccola molecola senza un progetto strutturale
Una sfida chiave è stata l’assenza della struttura cristallina tridimensionale di GIT1, per cui il team non poteva semplicemente «consultare» la forma della proteina. Hanno quindi impiegato modelli computazionali per prevedere la struttura di una regione di GIT1 composta da ripetizioni ankyrin, situata vicino ai siti di legame di MAT2B e di altre proteine di segnalazione. Hanno poi effettuato uno screening virtuale di una vasta libreria di piccole molecole contro questo modello per valutare quali potessero legarsi a quell’area. Tra i nove candidati testati in cellule, una molecola — denominata composto 3 (C3) — è emersa come particolarmente promettente. C3 si è legata specificamente a GIT1, ma non al parente vicino GIT2, e ha ridotto l’attività del segnale di crescita ERK in diverse linee cellulari tumorali.
Fermare la divisione e la diffusione delle cellule tumorali
Quando le cellule tumorali di fegato e colon sono state trattate con C3, la loro crescita è rallentata e a dosi più elevate molte cellule sono morte, mentre le cellule epatiche e renali non tumorali sono rimaste in gran parte indifferenti. C3 ha causato l’arresto delle cellule al confine tra le fasi G2 e M del ciclo cellulare, il checkpoint immediatamente prima e durante la mitosi quando una cellula si divide in due. Il composto ha anche ridotto drasticamente la capacità delle cellule tumorali di formare colonie e di migrare su una piastra — due misure in vitro associate alla ricrescita tumorale e alle metastasi. A livello molecolare, C3 ha indebolito le interazioni tra GIT1, MAT2B e le proteine di segnalazione RAF–MEK–ERK, portando a una minore attività di MEK ed ERK e a una riduzione della ciclica D1, motore del ciclo cellulare.
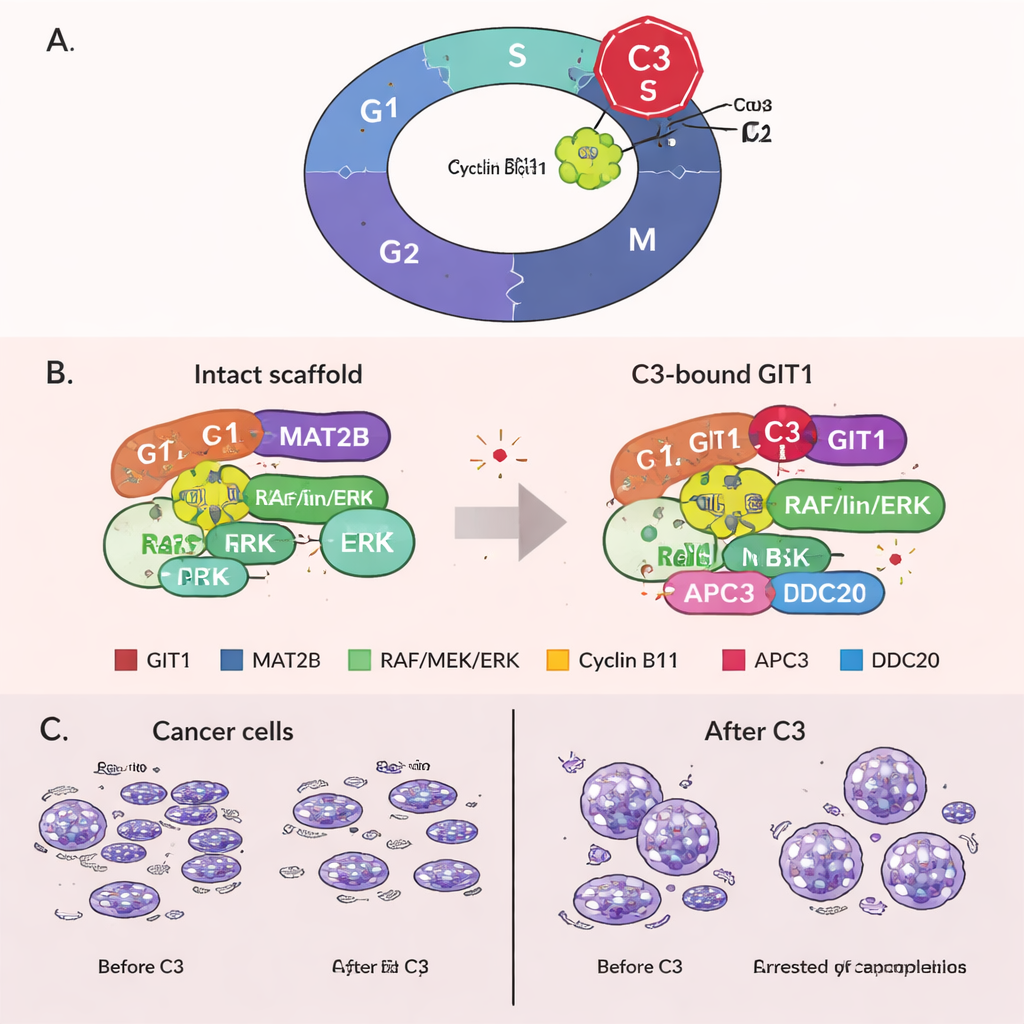
Bloccare le cellule in mitosi attraverso un ruolo nuovo di GIT1
In modo inaspettato, il team ha scoperto un nuovo ruolo di GIT1 negli stadi finali della divisione cellulare. Hanno osservato che GIT1 si lega alla cicline B1, una proteina che favorisce l’ingresso in mitosi, e anche a componenti di una macchina proteica chiamata complesso promotore dell’anafase (APC/C), che normalmente etichetta la ciclina B1 per la degradazione permettendo alle cellule di uscire dalla mitosi. Il trattamento con C3 ha rafforzato il legame tra GIT1 e la ciclina B1 ma ha indebolito le connessioni tra GIT1, ciclina B1 e i componenti dell’APC/C. Di conseguenza, la ciclina B1 non veniva più degradata efficacemente, i suoi livelli rimanevano elevati e le cellule rimanevano intrappolate in mitosi. Questo prolungato arresto è noto per indurre la morte cellulare, offrendo un secondo meccanismo con cui C3 può uccidere le cellule tumorali. È importante che, quando GIT1 è stato sperimentalmente ridotto, C3 abbia perso gran parte della sua capacità di aumentare la ciclina B1, bloccare il ciclo cellulare e sopprimere la crescita, dimostrando che i suoi effetti dipendono realmente da GIT1.
Risultati promettenti in modelli animali
I ricercatori sono poi passati a modelli murini per verificare se C3 potesse funzionare in organismi viventi. In topi immunocompetenti con tumori colorettali impiantati, iniezioni di C3 direttamente nei tumori ne hanno rallentato nettamente la crescita senza tossicità evidente per gli organi principali. In due modelli aggiuntivi — cellule umane di tumore del colon cresciute nel fegato di topi immunodeficienti e cellule murine di tumore del colon che si erano diffuse al fegato in topi immunocompetenti — C3 somministrato per via intraperitoneale ha ridotto il carico tumorale e i segni di diffusione. Esami del sangue e istologici hanno suggerito che i trattamenti erano ben tollerati, e studi farmacocinetici hanno mostrato che i livelli del farmaco nel circolo sanguigno rimanevano sufficientemente elevati per diverse ore dopo la somministrazione.
Cosa potrebbe significare per i futuri trattamenti del cancro
Per un lettore non specialista, il messaggio chiave è che gli autori hanno trovato un modo per attaccare il cancro non puntando un singolo enzima mutato, ma interrompendo un assemblaggio multiproteico di cui le cellule tumorali dipendono sia per i segnali di crescita sia per la divisione cellulare corretta. La loro piccola molecola, C3, si lega specificamente a GIT1, rimodella la sua rete di partner, attenua una via di crescita principale e intrappola le cellule tumorali in un ingorgo fatale durante la mitosi. Sebbene C3 sia ancora uno strumento sperimentale e non un farmaco per i pazienti, il lavoro dimostra che mirare a proteine impalcatura come GIT1 può aprire una nuova strada per trattare i tumori di fegato e colon con maggiore precisione e potenzialmente meno effetti collaterali.
Citazione: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Parole chiave: tumore del fegato, tumore del colon, terapia mirata, arresto del ciclo cellulare, proteina impalcatura