Clear Sky Science · it
Ricollegare il destino delle cellule di melanoma: i modulatori TRPM8 innescano l'apoptosi e potenziano la citotossicità delle cellule NK
Perché rivolgere un “sensore del freddo” contro il cancro della pelle è importante
Il melanoma è una forma aggressiva di cancro della pelle che spesso impara a sfuggire sia ai farmaci sia al sistema immunitario. Questo studio esplora una vulnerabilità inaspettata nelle cellule di melanoma: una proteina chiamata TRPM8, nota principalmente come sensore che permette alle cellule nervose di percepire il freddo o il mentolo. I ricercatori mostrano che farmaci progettati per bloccare TRPM8 possono spingere le cellule di melanoma all’autodistruzione e al contempo renderle più riconoscibili e attaccabili dalle cellule immunitarie natural killer (NK). Questa doppia azione suggerisce una nuova strategia per trattare melanomi avanzati e resistenti.
Un interruttore nascosto sulle cellule di melanoma
Analizzando grandi database sul cancro e studiando cellule di melanoma derivate dai pazienti in laboratorio, il team ha scoperto che TRPM8 è molto più abbondante nel melanoma metastatico rispetto alla pelle normale, incluse melanociti sani e fibroblasti dermici. Mediante tecniche di imaging, hanno mostrato che TRPM8 si trova sia sulla superficie cellulare sia sulle membrane interne, collocandosi in posizioni strategiche per influenzare il comportamento cellulare. Applicando una serie di nuove molecole mirate a TRPM8, due composti (denominati 4 e 9) si sono distinti costantemente: riducevano nettamente la sopravvivenza delle cellule di melanoma nel tempo lasciando in gran parte intatte le cellule cutanee normali. Test genetici hanno confermato che, quando TRPM8 veniva rimosso, questi farmaci perdeva-no il loro potere citotossico, e quando TRPM8 veniva aumentato, le cellule di melanoma diventavano ancora più sensibili, dimostrando che l’effetto dipende da questo specifico canale. 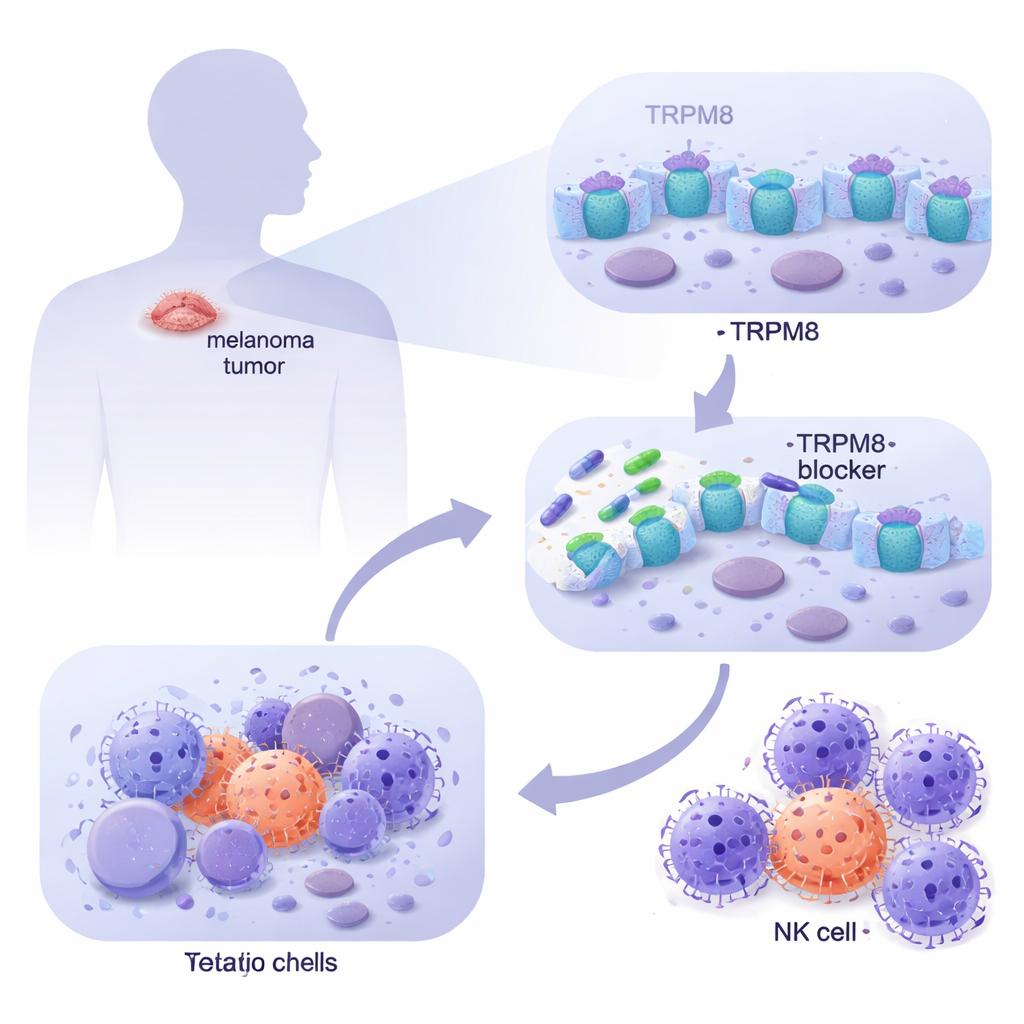
Forzare le cellule cancerose in una crisi energetica
A differenza dei classici attivatori di TRPM8 come il mentolo, che inducono un’ondata di calcio nelle cellule, questi nuovi bloccanti non hanno provocato cambiamenti nel calcio. Invece, hanno scatenato un’ondata di stress ossidativo all’interno delle cellule di melanoma. I composti hanno rapidamente aumentato le specie reattive dell’ossigeno, in particolare nei mitocondri, le centrali energetiche della cellula. Questo scoppio ossidativo ha fatto perdere ai mitocondri la loro carica elettrica, li ha frammentati e ha provocato il rilascio di citocromo c, un passaggio chiave per attivare il programma interno di “suicidio” della cellula. Antiossidanti che neutralizzavano queste specie reattive hanno in gran parte salvato le cellule, indicando che lo squilibrio redox non è un effetto collaterale ma il motore della morte cellulare. A valle, marcatori classici della morte come l’attivazione della caspasi-3 e la scissione della PARP hanno confermato che le cellule stavano subendo apoptosi programmata piuttosto che un danno casuale.
Disarmare i segnali di sopravvivenza e risvegliare un guardiano
Il colpo ossidativo ha scatenato una risposta allo stress più ampia. I farmaci hanno attivato ATM, un sensore del danno al DNA, e hanno portato all’accumulo e all’attivazione di p53, la nota proteina oncosoppressore che decide se una cellula danneggiata debba ripararsi o morire. Allo stesso tempo, i composti hanno indebolito una delle principali vie di sopravvivenza del melanoma: la via PI3K–AKT. Normalmente TRPM8 interagisce fisicamente con componenti della PI3K per contribuire a mantenere AKT nella sua forma attiva e promotrice di crescita. Dopo il trattamento, questa interazione si è dissolta e l’attività di AKT è diminuita, inclinando ulteriormente l’equilibrio verso la morte cellulare. È importante notare che questi cambiamenti sono stati pronunciati nelle cellule di melanoma ma non in cellule non cancerose, suggerendo una finestra terapeutica in cui il tumore viene colpito duramente mentre il tessuto sano è risparmiato.
Rendere i tumori più visibili alle “squadre d’assalto” immunitarie
La pericolosità del melanoma risiede anche nella sua capacità di sfuggire alla sorveglianza immunitaria. I ricercatori hanno quindi indagato cosa succede alle cellule tumorali che sopravvivono a basse dosi dei bloccanti TRPM8 per periodi più lunghi. Hanno scoperto che queste cellule residue cominciavano a esprimere maggiormente un marcatore di superficie chiamato ULBP1, che funge da segnale di soccorso riconosciuto dai recettori NKG2D sulle cellule NK. Altri segnali correlati non sono cambiati, indicando un effetto selettivo. In sferoidi di melanoma tridimensionali, che imitano meglio i tumori reali, il pretrattamento con i bloccanti TRPM8 non solo ha ridotto le dimensioni delle strutture e aumentato la morte cellulare, ma le ha rese molto più vulnerabili all’attacco delle cellule NK. Quando ULBP1 o NKG2D venivano bloccati con anticorpi, questo aumento dell’uccisione scompariva in gran parte, dimostrando che il miglioramento della clearance immunitaria avviene attraverso questo specifico “stretta di mano” tra tumore e cellule NK. 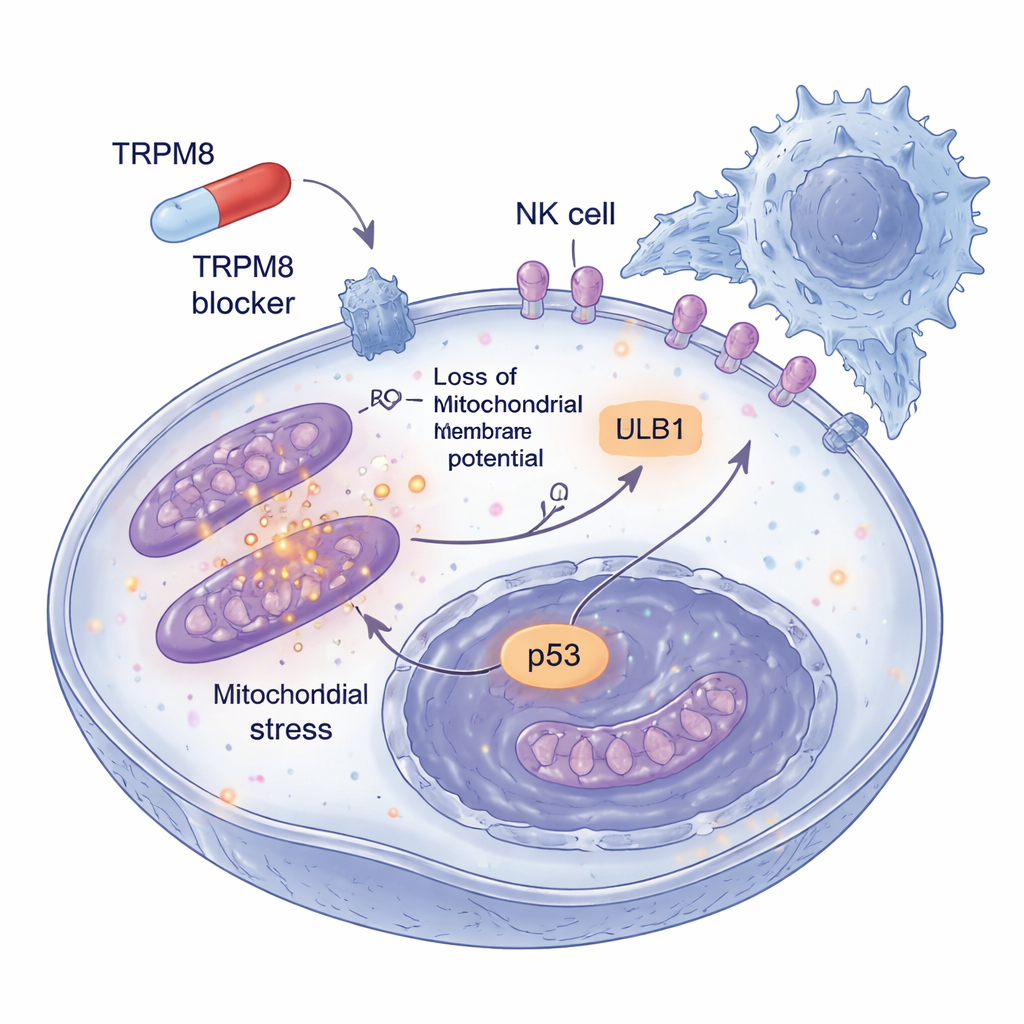
Cosa potrebbe significare per la cura futura del melanoma
In termini semplici, bloccare il “sensore del freddo” TRPM8 lo trasforma in una leva terapeutica: spinge le cellule di melanoma in una crisi mitocondriale e del DNA fatale e al contempo le segnala per l’eliminazione da parte delle cellule NK. Poiché i farmaci risparmiano le cellule della pelle normale e non danneggiano le cellule NK stesse, offrono una base promettente per nuovi trattamenti. Gli autori suggeriscono che i bloccanti di TRPM8 potrebbero essere combinati con immunoterapie esistenti per attaccare il melanoma avanzato e resistente ai farmaci su due fronti: uccidere direttamente le cellule tumorali e rendere i sopravvissuti più facilmente individuabili e distruggibili dal sistema immunitario.
Citazione: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Parole chiave: melanoma, TRPM8, mitocondri, stress ossidativo, cellule natural killer