Clear Sky Science · it
La TRIM29 indotta dalla lattilazione promuove comportamento invasivo e metastasi linfonodali nel cancro gastrico attraverso la via Wnt/β-catenina mediata da hnRNPA1
Perché questa ricerca è importante
Il cancro gastrico (allo stomaco) è uno dei tumori più letali al mondo in gran parte perché si diffonde precocemente ai linfonodi vicini, rendendo difficile la guarigione solo con la chirurgia. Questo studio rivela come una modifica chimica legata al metabolismo tumorale potenzi una proteina chiamata TRIM29, aiutando le cellule tumorali a invadere i tessuti circostanti, a formare nuovi vasi linfatici e a resistere alla chemioterapia. Comprendere questa catena di eventi indica nuove strategie per rallentare o bloccare la diffusione del cancro gastrico.
Una partnership pericolosa nei tumori gastrici
I ricercatori hanno iniziato confrontando campioni di cancro gastrico con tessuto sano vicino provenienti da 100 pazienti, oltre a grandi database pubblici di geni. Hanno scoperto che TRIM29, una proteina in passato collegata alla regolazione immunitaria e ad altri tumori, era costantemente più elevata nelle cellule tumorali. I pazienti i cui tumori presentavano livelli più alti di TRIM29 avevano una maggiore probabilità di mostrare coinvolgimento dei linfonodi e dei vasi sanguigni e una sopravvivenza complessiva peggiore. Questi schemi suggerivano che TRIM29 non è solo presente, ma è attivamente coinvolta nell’aumentare l’aggressività del cancro gastrico.
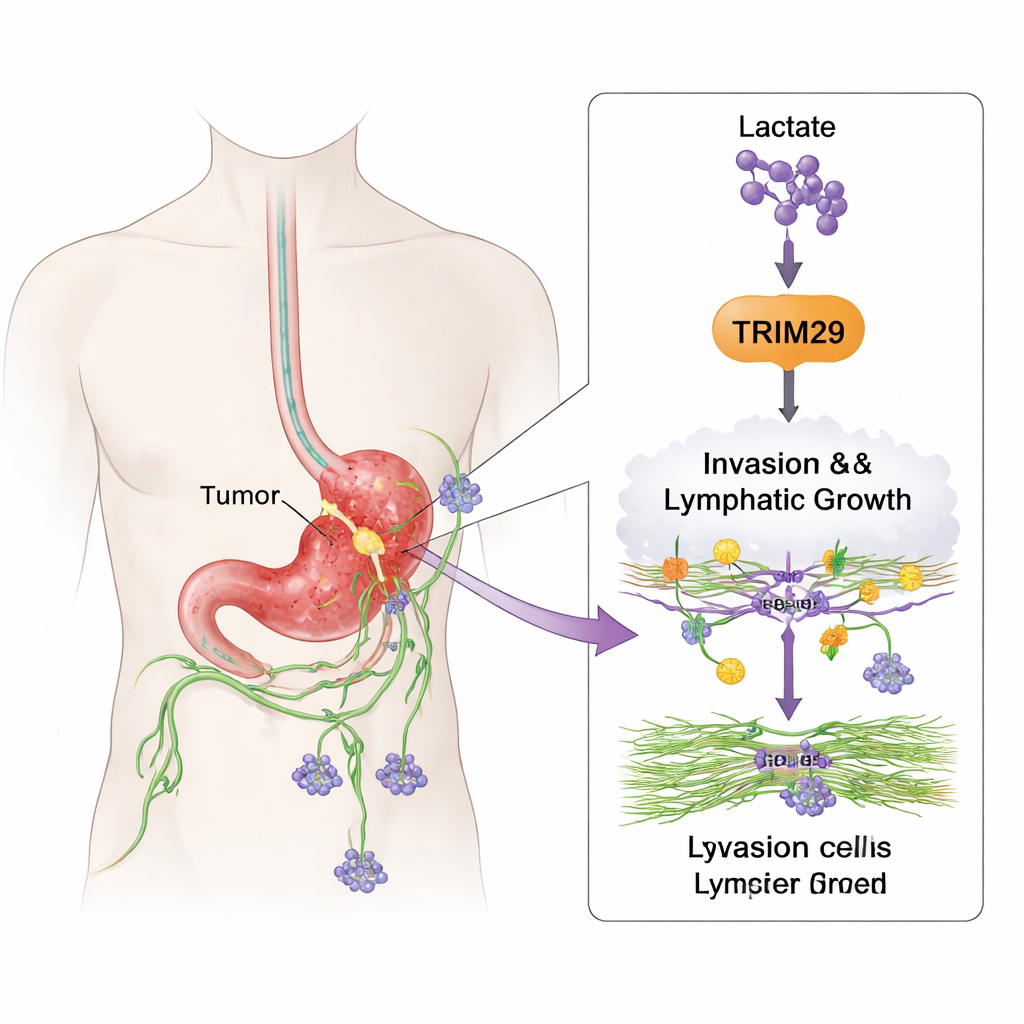
Come le cellule tumorali imparano a viaggiare
Per capire cosa fa effettivamente TRIM29, il team ha modificato i suoi livelli in linee cellulari di cancro gastrico. Quando hanno ridotto TRIM29, le cellule sono diventate nettamente meno mobili e meno in grado di attraversare gel tridimensionali che mimano i tessuti. L’aumento di TRIM29 ha avuto l’effetto opposto, rendendo le cellule più invasive. I ricercatori hanno anche esaminato le cellule endoteliali linfatiche, che rivestono i vasi linfatici. Le cellule tumorali ricche di TRIM29 hanno indotto queste cellule vascolari a germogliare e a formare strutture tubolari, segno di nuova crescita linfatica (linfangiogenesi). Nei modelli murini, i tumori con alto TRIM29 hanno prodotto più metastasi epatiche e linfonodali, mentre quelli con TRIM29 silenziata si sono diffusi meno e hanno formato meno vasi linfatici.
Staffetta molecolare: proteggere un regolatore chiave
Approfondendo, gli scienziati hanno scoperto che TRIM29 si lega fisicamente a un’altra proteina, hnRNPA1, nota per influenzare l’elaborazione degli RNA ed è collegata alla diffusione tumorale. Normalmente hnRNPA1 può essere segnato per la degradazione da un’altra proteina enzimatica, ZFP91, attraverso il sistema di smaltimento cellulare. TRIM29 interferisce con questo processo competendo con ZFP91 per il legame con hnRNPA1. Quando TRIM29 è abbondante, protegge hnRNPA1 dall’essere segnato e degradato. Di conseguenza hnRNPA1 diventa più stabile e si accumula nelle cellule tumorali, innescando una cascata di segnali che porta all’attivazione della via Wnt/β-catenina, un noto promotore della crescita e della migrazione tumorale. Questo a sua volta aumenta la produzione di VEGF‑C, una molecola che stimola la formazione di nuovi vasi linfatici, offrendo alle cellule tumorali più “strade” per fuggire.
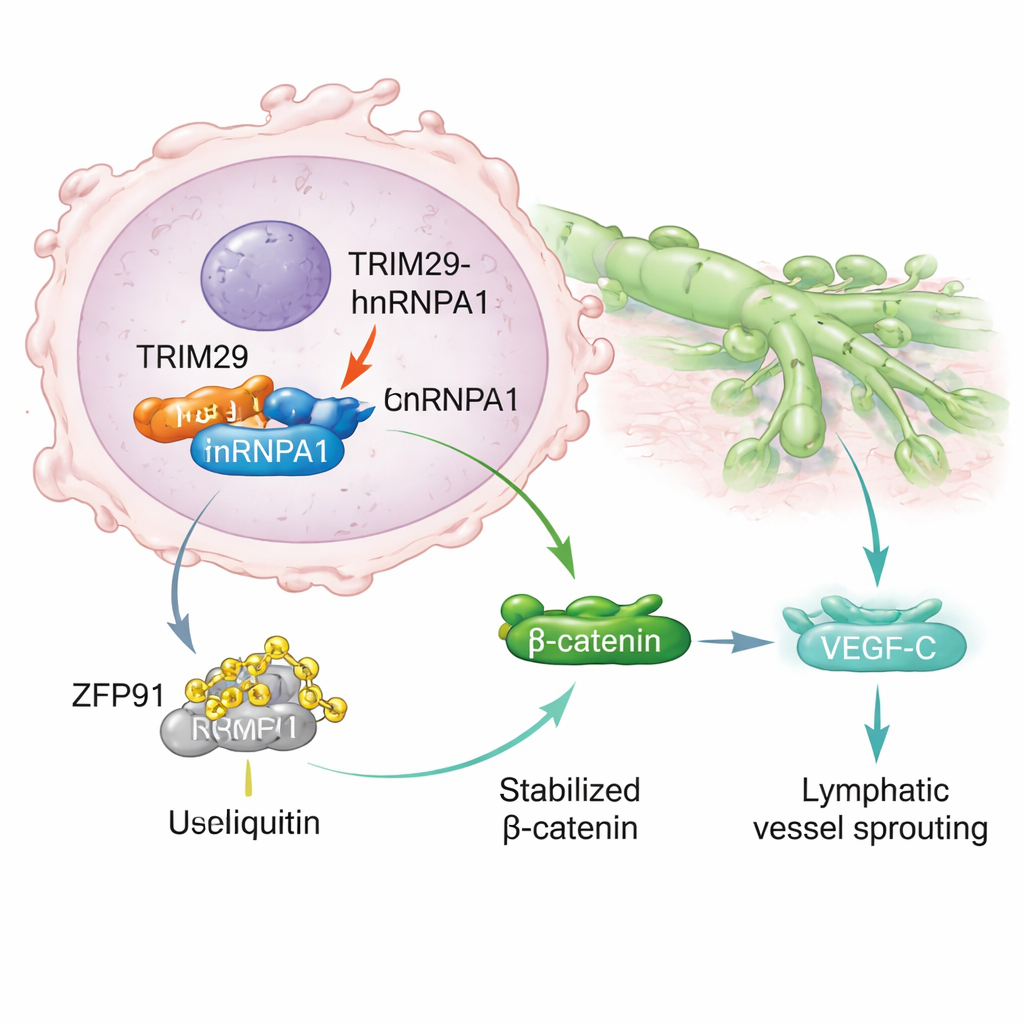
Alimentare il cancro con il lattato
Lo studio collega inoltre questo comportamento invasivo al modo in cui i tumori metabolizzano gli zuccheri. I tumori in rapida crescita spesso fanno affidamento su un tipo di metabolismo che produce grandi quantità di lattato, un sottoprodotto un tempo considerato semplice rifiuto. Qui gli autori mostrano che il lattato può modificare chimicamente le proteine istoniche che impacchettano il DNA, specificamente in un sito chiamato H3K9. Questa “lattilazione” funziona come un interruttore acceso per il gene TRIM29, aumentandone l’attività. Quando hanno ridotto la produzione di lattato usando farmaci metabolici, i livelli di TRIM29 sono diminuiti; quando hanno aumentato il lattato, TRIM29 è salito. I tessuti di cancro gastrico dei pazienti mostravano livelli più alti di questa lattilazione H3K9, che correlavano con TRIM29 elevata, maggiore diffusione ai linfonodi e sopravvivenza peggiore. In sostanza, il metabolismo alterato del tumore contribuisce a scrivere un programma genetico più aggressivo.
Nuovi modi per potenziare la chemioterapia
I vasi linfatici fanno più che trasportare cellule tumorali; possono anche drenare via i farmaci chemioterapici dai tumori. Utilizzando innesti tumorali derivati da pazienti e cresciuti in topi, i ricercatori hanno testato se bloccare TRIM29 e la crescita dei vasi linfatici potesse migliorare l’efficacia del 5‑fluorouracile (5‑FU), un farmaco standard per il cancro gastrico. L’inibizione di TRIM29 o il blocco della linfangiogenesi hanno reso ciascuno il 5‑FU più efficace nel ridurre le dimensioni del tumore e la divisione cellulare. La combinazione di entrambe le strategie ha prodotto la risposta più forte, suggerendo un potenziale modo per superare alcune forme di resistenza ai farmaci nelle malattie avanzate.
Cosa significa per i pazienti
Questo lavoro dipinge un quadro passo dopo passo: i tumori gastrici generano eccesso di lattato, che attiva TRIM29; TRIM29 quindi protegge hnRNPA1, stabilizza una via di crescita e incrementa la formazione di vasi linfatici e la diffusione ai linfonodi. Dal punto di vista clinico, alti livelli di TRIM29 e i relativi marchi di lattilazione identificano i pazienti a maggior rischio di malattia aggressiva. In futuro, farmaci che riducono la segnalazione del lattato, bloccano TRIM29 o prevengono la crescita dei vasi linfatici potrebbero essere combinati con la chemioterapia esistente per impedire la diffusione del cancro gastrico e migliorare l’efficacia dei trattamenti.
Citazione: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Parole chiave: metastasi del cancro gastrico, TRIM29, lattato e lattilazione, linfangiogenesi, via Wnt beta-catenina