Clear Sky Science · it
KIF20A inibisce l’ubiquitinazione di DHX9 dipendente da TRIM21 per aumentare la stabilità di SOX2, potenziando la stemness e la resistenza alla ferroptosi nell’OSCC
Perché questa ricerca conta per i pazienti con tumore orale
Il carcinoma squamoso orale, una forma comune di cancro della bocca, spesso recidiva e resiste ai trattamenti. Molti insuccessi di chirurgia, chemioterapia e radioterapia sono riconducibili a un piccolo e ostinato gruppo di «cellule staminali tumorali» in grado di rigenerare il tumore e resistere alla morte cellulare. Questo studio svela un circuito molecolare chiave che aiuta queste cellule a sopravvivere e a resistere a una forma più recente di morte cellulare chiamata ferroptosi, e indica una strategia farmacologica che potrebbe rendere più efficace la chemioterapia standard.
Un motore nascosto nei tumori della bocca
I ricercatori hanno iniziato confrontando campioni tumorali di pazienti con carcinoma orale con il tessuto sano circostante. Hanno rilevato che una proteina chiamata KIF20A era costantemente molto più espressa nelle cellule tumorali. Analizzando dataset più ampi di pazienti, chi presentava livelli elevati di KIF20A nel tumore tendeva ad avere una sopravvivenza più breve, suggerendo che questa proteina è associata a malattia aggressiva. 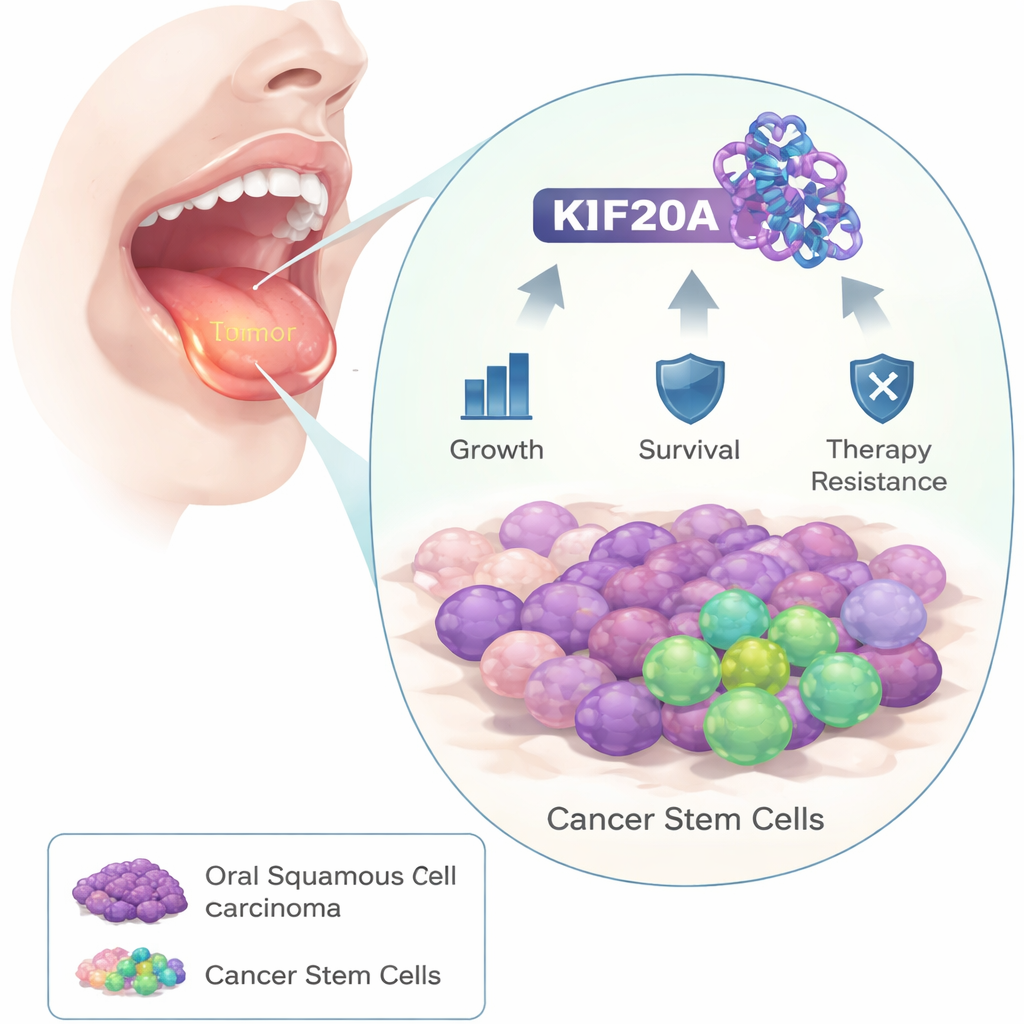
Come KIF20A protegge un importante fattore dell’RNA
Per capire cosa faccia concretamente KIF20A, il team ha utilizzato metodi di mappatura delle proteine per cercare i suoi partner all’interno delle cellule tumorali. Un partner centrale emerso è stato DHX9, una proteina che contribuisce alla gestione delle molecole di RNA e influenza la durata di certi messaggi cellulari. Gli scienziati hanno scoperto che KIF20A si lega a DHX9 e impedisce che venga marcato per la degradazione da un’altra proteina, la ligasi E3 TRIM21, che normalmente tagga DHX9 con catene di ubiquitina destinandolo al trituratore proteico della cellula. Bloccando questa marcatura, KIF20A rallenta il degrado di DHX9 e ne aumenta i livelli, soprattutto nel citoplasma, dove può agire su specifici target di RNA.
Dalla stabilità degli RNA alle cellule staminali tumorali e alla resistenza alla ferroptosi
Con DHX9 più stabile emerge un altro attore cruciale: SOX2, un gene maestro che aiuta le cellule a mantenere uno stato staminale e a resistere ai trattamenti. Lo studio mostra che DHX9 protegge l’RNA di SOX2 dalla degradazione, permettendo la sintesi di più proteina SOX2. Nelle cellule del carcinoma orale, l’eccesso di KIF20A portava a livelli più alti di DHX9 e SOX2, a maggiore formazione di sferoidi tumorali in coltura e a una frazione più ampia di cellule che esprimevano marcatori staminali — segni di una «stemness» tumorale più robusta. KIF20A rendeva inoltre le cellule meno vulnerabili alla ferroptosi, un tipo di morte cellulare mediata dal ferro e dai lipidi che si sta esplorando come modalità per eliminare cellule tumorali resistenti. Quando KIF20A veniva spento, i tumori nei topi si riducevano più facilmente e aumentavano i marker di ferroptosi, indicando la perdita di questa protezione.
Un circuito molecolare con un punto debole farmacologicamente aggredibile
Mettendo insieme questi elementi, gli autori propongono un asse KIF20A–DHX9–SOX2: KIF20A stabilizza DHX9, DHX9 stabilizza l’RNA di SOX2, e SOX2 a sua volta mantiene le cellule staminali tumorali e blocca la ferroptosi. Questo circuito si connette inoltre alla via PI3K–AKT, una principale rotta di crescita e sopravvivenza in molti tumori. 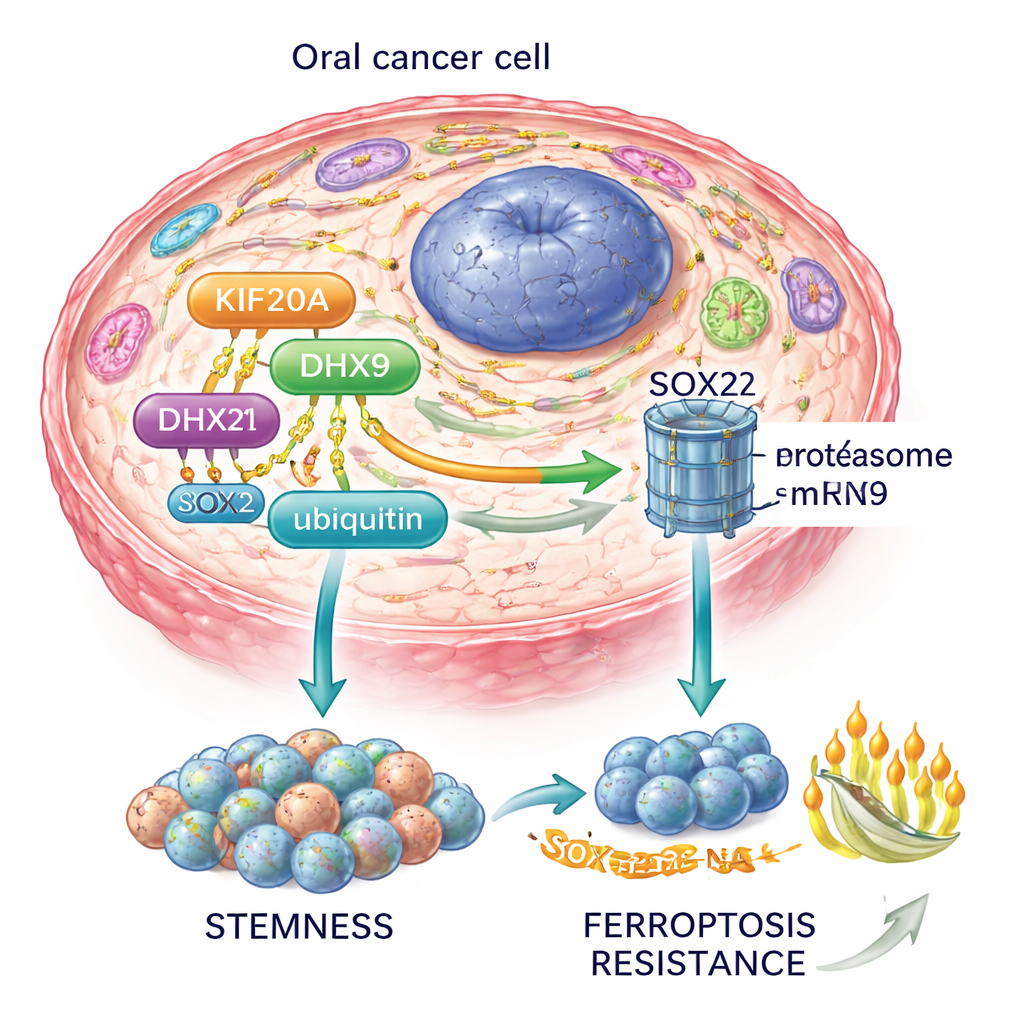
Un candidato farmaco per indebolire i tumori resistenti
Per fare un passo verso la terapia, il team ha cercato in ampi database droga–gene composti predetti a controbilanciare i pattern genici correlati a KIF20A. Hanno identificato ENMD-2076, un inibitore orale multitarget delle chinasi già testato in altri tumori. Nelle cellule di carcinoma orale con alta espressione di KIF20A, ENMD-2076 ha ridotto i livelli di KIF20A, DHX9 e SOX2, attenuato le vie legate alla stemness e rallentato la crescita. In combinazione con il chemioterapico standard cisplatino, ENMD-2076 ha prodotto un effetto anticancro più potente rispetto a ciascun farmaco da solo sia in colture cellulari sia nei tumori murini, senza tossicità aggiuntiva evidente.
Cosa significa per le terapie future
Per un pubblico non specialista, il messaggio è che questo studio rivela come una singola proteina iperattiva, KIF20A, aiuti i tumori della bocca a mantenere viva una piccola riserva di cellule «seme» e a proteggerla da una promettente forma di morte cellulare. Mappando questa catena — da KIF20A a DHX9 a SOX2 — i ricercatori individuano nuovi bersagli farmacologici e mostrano che un farmaco sperimentale esistente, ENMD-2076, può indebolire questo asse e rendere il cisplatino più efficace nei modelli. Pur richiedendo ulteriori studi per verificarne la sicurezza e i benefici nei pazienti, i risultati supportano la prospettiva che bloccare questo circuito possa aiutare a prevenire le recidive e a superare la resistenza ai farmaci nel carcinoma orale.
Citazione: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Parole chiave: carcinoma squamoso orale, cellule staminali tumorali, ferroptosi, KIF20A, SOX2