Clear Sky Science · it
La selenometionina come inibitore della ferroptosi a doppio meccanismo: biosintesi di GPX4 guidata dall’apporto di selenio oltre la transsulfatazione e scavenging dei ROS mediato dalla capacità reduttrice indipendente dall’attività di GPX4
Perché proteggere le nostre cellule da una «morte da ruggine» è importante
Le cellule del nostro organismo possono morire in modi diversi, e uno dei più recenti e affascinanti è chiamato ferroptosi — un tipo di danno alle membrane cellulari guidato dal ferro, simile a una «ruggine». Questo processo è oggi collegato a patologie che vanno dal danno renale alla neurodegenerazione. L’elemento traccia selenio, noto a molti per gli integratori alimentari, gioca un ruolo chiave nell’arrestare questa forma pericolosa di morte cellulare. Questo studio esplora come un aminoacido comune contenente selenio, la selenometionina, possa proteggere le cellule dalla ferroptosi attraverso non una ma due distinte strategie protettive.
Un nuovo difensore scoperto in una vasta ricerca di farmaci
Per identificare piccole molecole in grado di bloccare la ferroptosi, i ricercatori hanno screeningato migliaia di composti tratti da farmaci approvati dalla FDA e prodotti naturali. Hanno usato una molecola chimica chiamata RSL3 per indurre la ferroptosi in linee cellulari tumorali umane e hanno monitorato la morte cellulare e l’accumulo di grassi ossidati danneggiati nelle membrane. Tra tutti i candidati, la selenometionina è emersa come un forte protettore: ha ridotto sia il danno lipidico sia la morte cellulare in diversi tipi cellulari e in due principali modelli di ferroptosi — uno guidato dall’inibizione diretta di GPX4 (con RSL3) e un altro dalla deprivazione di cistina, un mattoncino per l’antiossidante glutatione. Questi risultati collocano la selenometionina come un inibitore della ferroptosi ampio e robusto. 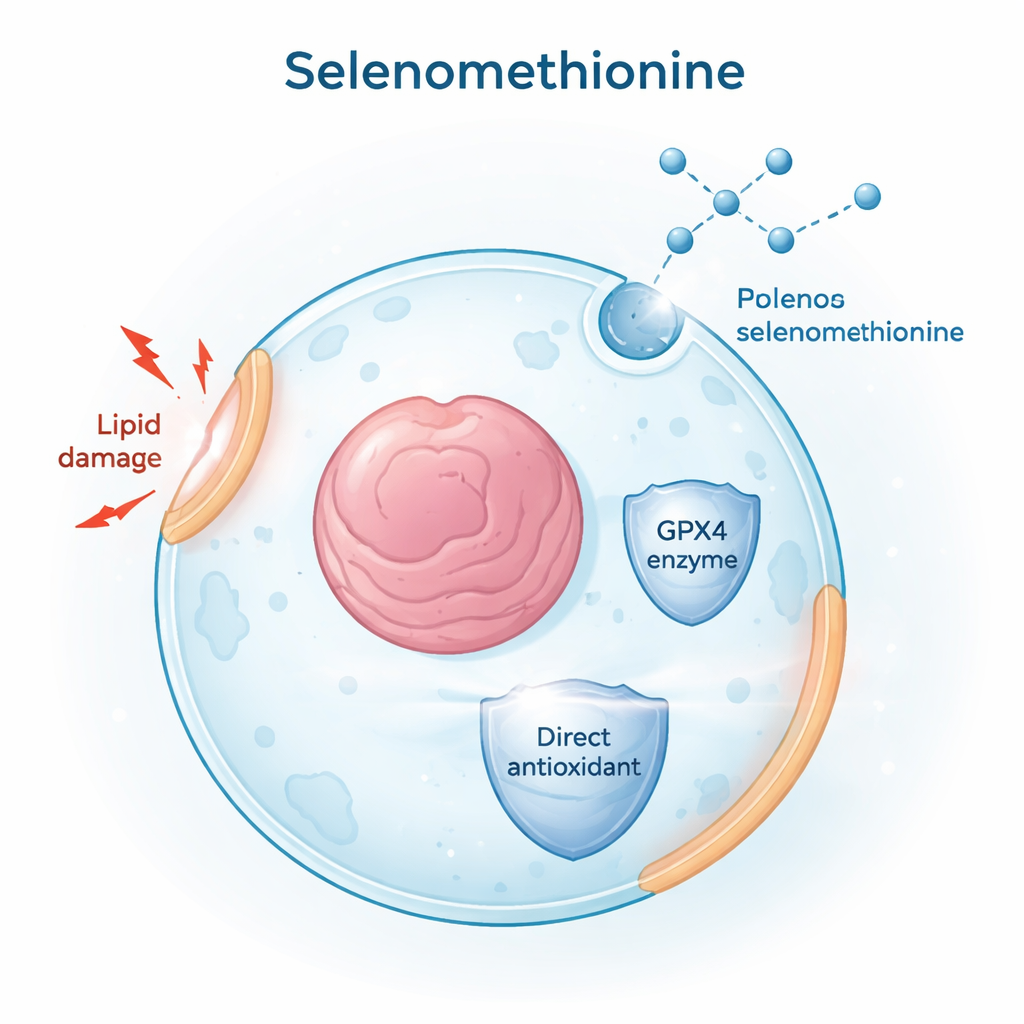
Apporto di selenio per un enzima protettivo chiave
Una barriera anti-ferroptosi centrale nelle cellule è un enzima chiamato GPX4, che dipende dal selenio per funzionare. Il gruppo ha voluto capire se la selenometionina si limita ad alimentare questa via o se fa di più. Hanno tracciato come il selenio proveniente dalla selenometionina possa essere convertito in forme adatte alla costruzione di GPX4, anche quando una via abituale, detta transsulfatazione, era compromessa o bloccata. Usando silenziamenti genetici e inibitori chimici di enzimi nelle vie zolfo–selenio, hanno trovato che la selenometionina aumentava comunque i livelli di GPX4 e proteggeva le cellule. Ciò dimostra che le cellule possono sfruttare più rotte metaboliche per estrarre selenio dalla selenometionina e mantenere la produzione di GPX4, anche nei tessuti dove la via classica è debole.
Protezione che non dipende dall’enzima abituale
Con sorpresa, quando i ricercatori eliminarono completamente GPX4 dalle cellule usando l’editing genetico CRISPR, la selenometionina continuò a proteggere dalla ferroptosi. Riduceva ancora il danno lipidico alle membrane e la morte cellulare, indicando che GPX4 non è tutta la storia. Esperimenti aggiuntivi suggerirono che parte di questa protezione coinvolge l’incorporazione della selenometionina nelle proteine appena sintetizzate, ma che ciò rappresenta solo una parte dell’effetto. Gli autori si concentrarono dunque sulla reattività chimica della selenometionina stessa. Scoprirono che può neutralizzare direttamente specie reattive dell’ossigeno (ROS), incluso il perossido di idrogeno, e viene convertita in una forma ossidata, il «solfossido». La spettrometria di massa confermò questo prodotto, e somministrare alle cellule la versione solfossido ridusse anch’essa la ferroptosi, implicando che le cellule possono rimetterla in ciclo riduttivo fino a rigenerare la selenometionina attiva.
Dalla coltura cellulare alla protezione dei reni in animali vivi
Per verificare se questi meccanismi hanno rilevanza nell’organismo intero, il gruppo si rivolse a un modello murino di danno renale acuto indotto dal farmaco anticancro cisplatino, una condizione nota per coinvolgere la ferroptosi. I topi trattati con cisplatino mostrarono perdita di peso, reni ingrossati, funzione renale compromessa e alti livelli di marker di ferroptosi. Quando gli animali ricevettero selenometionina, molti di questi problemi migliorarono: il peso corporeo si riprese, il rigonfiamento renale diminuì, i parametri ematici della funzione renale si normalizzarono, i segnali infiammatori calarono e i marker chimici del danno lipidico diminuirono. Il tessuto renale mostrò inoltre livelli più alti di GPX4 e minori lesioni strutturali. Questi benefici erano comparabili a quelli osservati con ferrostatin-1, un noto inibitore sperimentale della ferroptosi. 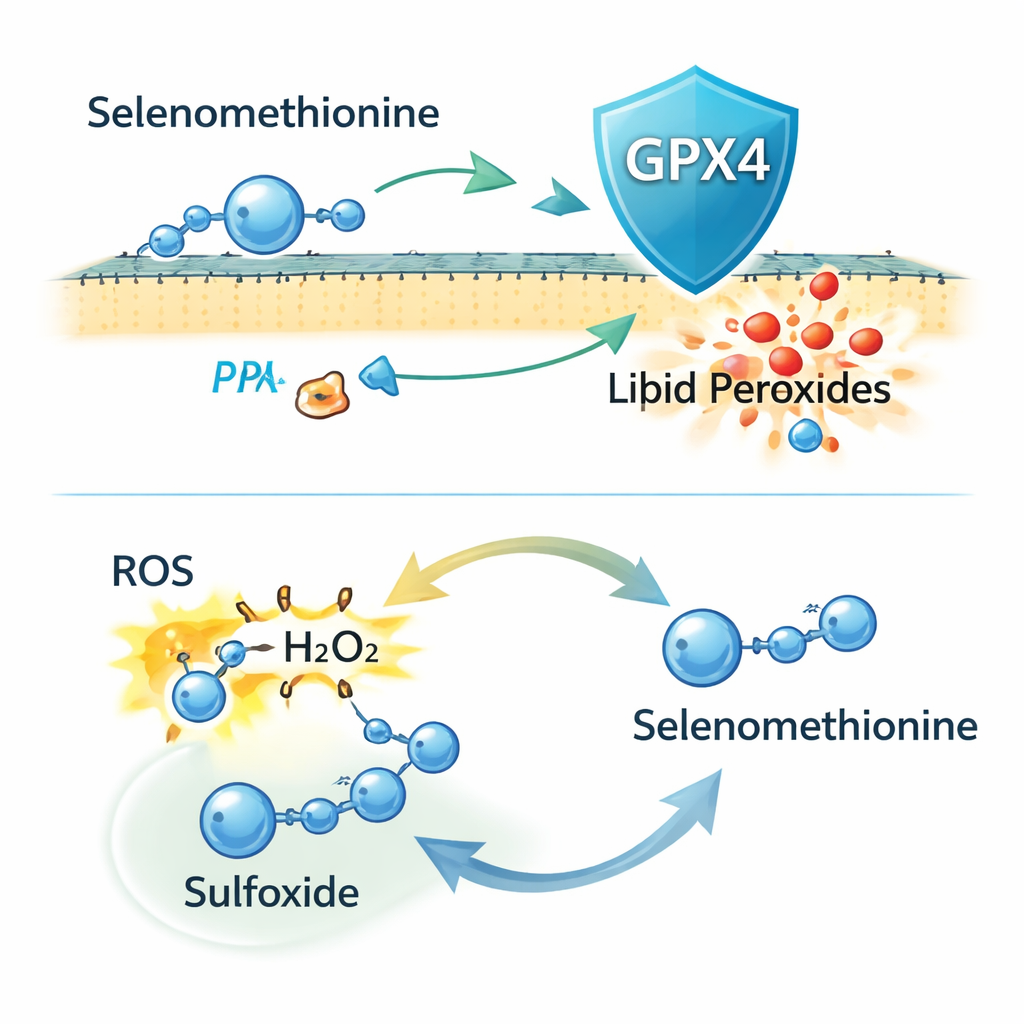
Cosa significa per le terapie future
In termini pratici, questo lavoro suggerisce che la selenometionina agisce come un estintore a doppio scopo contro una «rugginizzazione» delle membrane cellulare alimentata dal ferro. Da un lato fornisce selenio perché le cellule possano costruire più dell’enzima GPX4, che funziona come un servizio di pulizia interno per i lipidi danneggiati. Dall’altro, la selenometionina stessa può assorbire ossidanti dannosi e essere riciclata, offrendo una protezione di riserva indipendente da GPX4. Nel loro insieme, queste caratteristiche rendono la selenometionina un candidato promettente per prevenire o trattare malattie in cui la ferroptosi gioca un ruolo centrale, come il danno renale indotto da farmaci e, potenzialmente, altre condizioni guidate da stress ossidativo incontrollato.
Citazione: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Parole chiave: ferroptosi, selenio, selenomethionina, stress ossidativo, danno renale acuto