Clear Sky Science · it
La subunità Cct3 della chaperonina TRiC è necessaria per il trasporto assone, la mielinizzazione e la rifinitura della giunzione neuromuscolare
Quando il cablaggio nervoso va storto
I nostri cervelli e corpi dipendono da lunghi filamenti nervosi, simili a cavi, per trasmettere segnali in modo rapido e affidabile. Per svolgere questo compito, molti nervi sono avvolti da mielina isolante e le loro terminazioni devono formare contatti precisi con i muscoli. Questo articolo esplora cosa succede quando viene meno un importante “aiutante” cellulare per il ripiegamento delle proteine, chiamato Cct3. Utilizzando zebrafish e tessuto umano, gli autori mostrano come questa singola componente di una grande macchina chaperonica possa alterare la mielina, le connessioni nervo–muscolo e il sistema di trasporto interno che mantiene le cellule nervose vive e funzionali.
Un sarto cellulare per costruire i nervi
All’interno di ogni cellula, le proteine di nuova sintesi devono assumere la forma corretta, un po’ come cucire su misura un abito. Il complesso TRiC, che include la subunità Cct3, è uno dei principali “sarti”, aiutando circa il 10% delle proteine cellulari — in particolare le proteine strutturali actina e tubulina — a ripiegarsi correttamente. Questi elementi costitutivi formano l’impalcatura interna della cellula e le piste lungo le quali vengono spostati carichi vitali. Nei pazienti portatori di versioni difettose di CCT3 e geni correlati, le immagini cerebrali mostrano una riduzione della materia bianca (il cablaggio ricco di mielina del cervello) e problemi nei nervi periferici e nei muscoli. Gli autori si sono prefissati di capire come la perdita di Cct3 faccia deragliare lo sviluppo e la funzione nervosa.
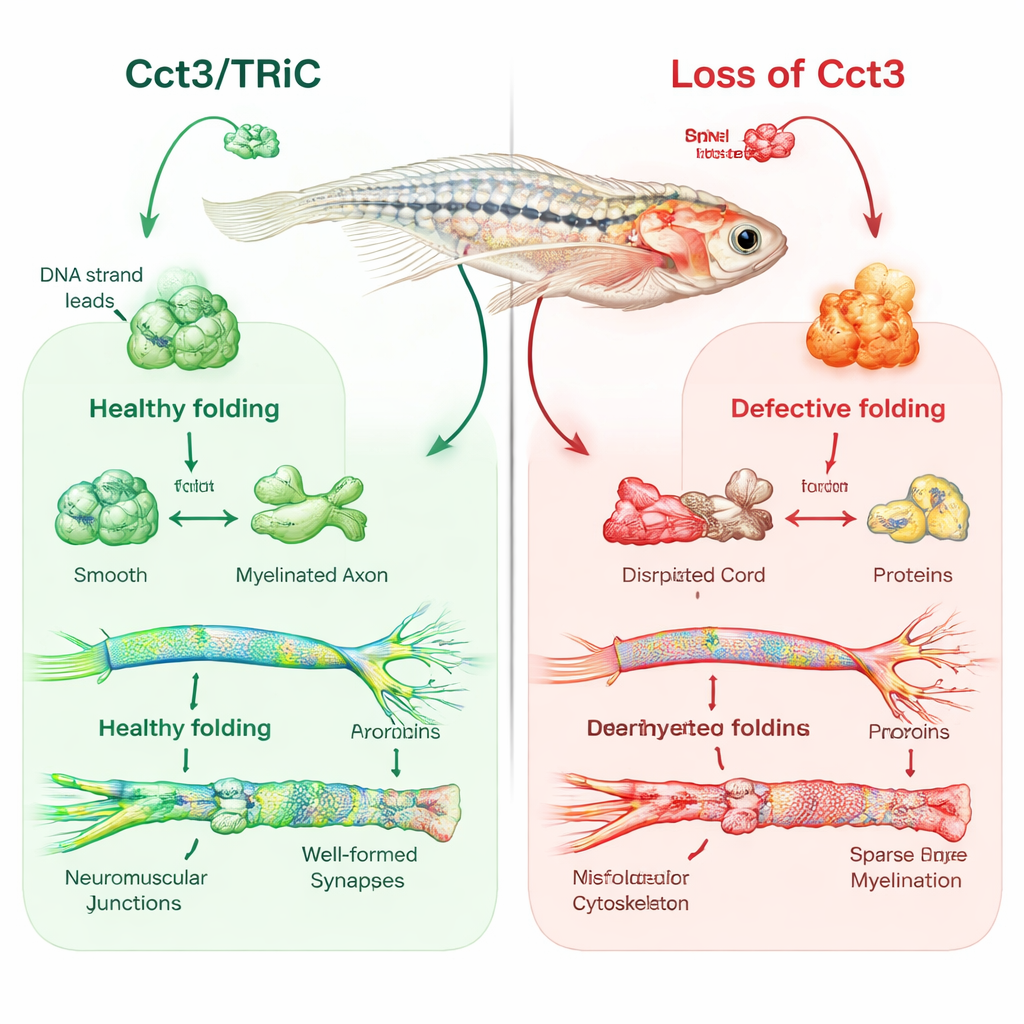
Lo zebrafish come finestra sull’isolamento nervoso
Il gruppo ha utilizzato l’editing genetico CRISPR/Cas9 per creare zebrafish privi di cct3 funzionale. Questi piccoli pesci presentavano cervelli e occhi più piccoli, accumulo di liquido intorno al cuore, risposte deboli al tatto e morivano entro pochi giorni. Quando i ricercatori hanno ripristinato cct3 normale iniettando il suo RNA messaggero, molti di questi difetti sono migliorati, confermando che la perdita di Cct3 era la causa principale. Concentrandosi sulla mielina, hanno impiegato marcatori fluorescenti e microscopia elettronica per visualizzare gli strati isolanti intorno ai nervi. Nei pesci normali, le cellule mielinizzanti nel cervello e nei nervi periferici avvolgevano gli assoni con guaine ordinate e stratificate entro il quarto giorno di sviluppo. Al contrario, i mutanti cct3 avevano molte meno cellule mielinizzanti e praticamente nessuna mielina corretta attorno a molti assoni, nonostante quegli assoni apparissero esternamente di forma normale.
Cellule di supporto fragili e collegamenti nervo–muscolo sotto stress
Per scoprire perché la mielina mancava, gli autori hanno esaminato le cellule di Schwann e le correlate cellule della cresta neurale — le cellule di supporto che avvolgono i nervi periferici. Nei pesci normali, queste cellule estendevano lunghi sottili processi e poi affinarono la loro forma mentre formavano segmenti di mielina. Nei mutanti si arrotondavano, accorciavano i processi e si frammentavano. I loro nuclei si disgregavano con un pattern tipico della morte cellulare programmata, e comparve un marcatore chiave della morte (Caspasi 3 attivata), indicando che molte di queste cellule morivano precocemente. Nel frattempo, alle giunzioni neuromuscolari dove i nervi incontrano il muscolo, il modello dei “punti caldi” dei recettori sui muscoli non si è raffinato. Invece di molti piccoli ammassi precisi, i mutanti presentavano meno aree ma più grandi di recettori, richiamando le pieghe sinaptiche semplificate osservate in un paziente umano con una mutazione di CCT3.
Piste interne spezzate e traffico di carichi rallentato
Poiché TRiC aiuta a ripiegare actina e tubulina, gli autori hanno osservato da vicino l’impalcatura interna degli assoni motori. Hanno trovato che i livelli complessivi di tubulina erano fortemente ridotti nei mutanti e il numero di microtubuli normali — i tubi cavi che fungono da piste per il trasporto — calava drasticamente sia nei nervi centrali sia in quelli periferici. Anche i “tag” chimici sulla tubulina, importanti per microtubuli stabili e idonei al trasporto, risultavano gravemente alterati. Utilizzando immagini in vivo di mitocondri ed endosomi fluorescenti all’interno degli assoni motori, hanno osservato come questi carichi si muovessero. Nei pesci sani, gli organelli viaggiavano velocemente e in modo direzionale lungo l’assone. Nei mutanti, molti organelli si bloccavano o ondeggiavano avanti e indietro, coerente con piste danneggiate e trasporto interrotto.
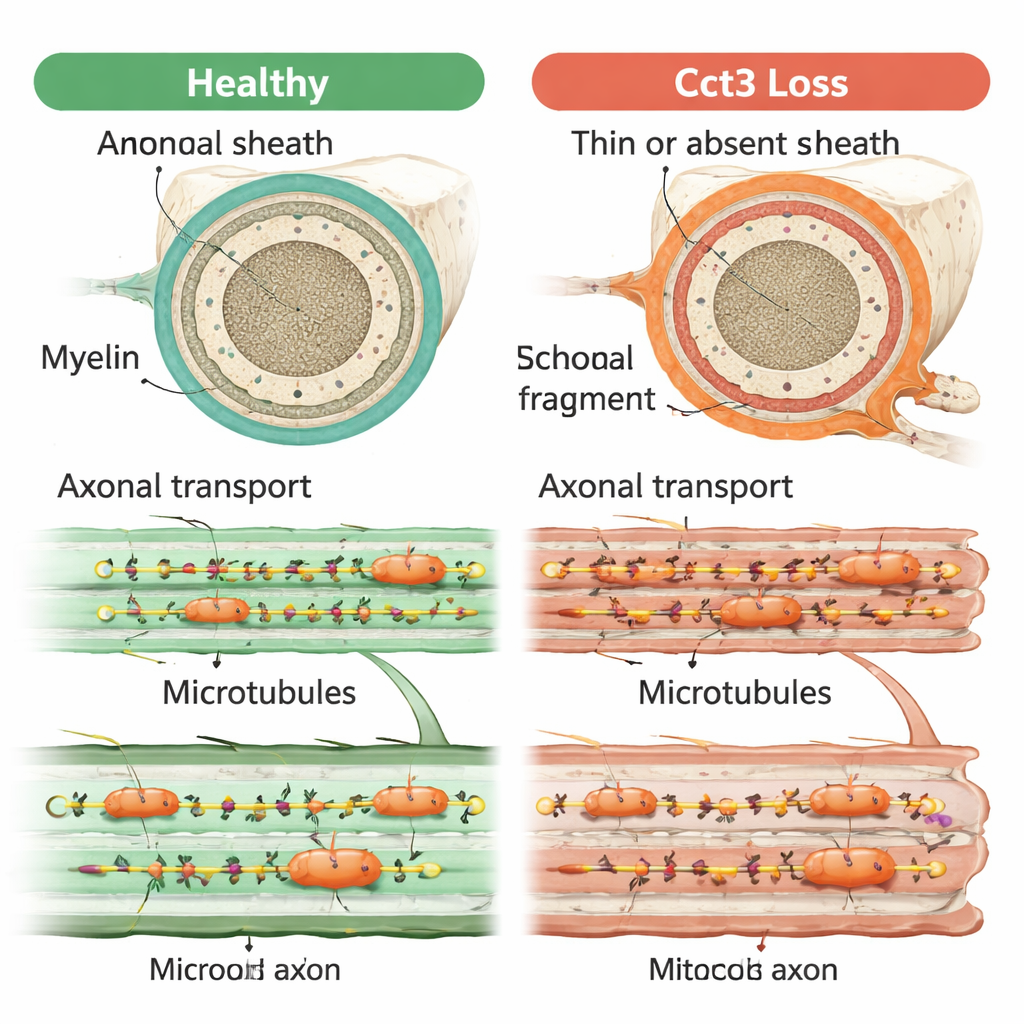
Un problema centrale dietro molti sintomi
Nel complesso, i risultati mostrano che Cct3 è essenziale per diversi aspetti interconnessi della salute dei nervi: sostiene la sopravvivenza delle cellule di supporto mielinizzanti, permette un corretto avvolgimento della mielina e consente alle giunzioni neuromuscolari in maturazione di affinarsi. Tutti questi ruoli possono essere ricondotti alla sua funzione nel ripiegamento e nel mantenimento delle proteine che costruiscono il citoscheletro e le piste di microtubuli usate per il trasporto assone. Quando queste piste falliscono, segnali e materiali chiave non possono raggiungere i punti giusti lungo il nervo, indebolendo probabilmente sia la comunicazione con le cellule mielinizzanti sia la conformazione dei contatti nervo–muscolo. Questo lavoro suggerisce che il trasporto assone compromesso possa essere il filo conduttore che collega i diversi problemi cerebrali e nervosi osservati nei disturbi legati a TRiC.
Citazione: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Parole chiave: mielinizzazione, trasporto assone, giunzione neuromuscolare, chaperoni molecolari, modello di zebrafish