Clear Sky Science · it
Traffico e segnalazione BDNF-TrkB compromessi nei neuroni del prosencefalo basale nella sindrome di Down
Perché questo studio sul cervello è importante
Le persone con sindrome di Down vivono più a lungo che in passato, ma corrono anche un rischio molto elevato di sviluppare una demenza simile all’Alzheimer in età adulta. Questo studio analizza in profondità singole cellule cerebrali per capire perché certi neuroni sono così vulnerabili. Seguendo come queste cellule spostano e rispondono a una molecola chiave «fertilizzante» per il cervello, i ricercatori mettono in luce un ingorgo interno ai neuroni che potrebbe contribuire alla perdita di memoria e indicare nuove strategie terapeutiche.
Il «fertilizzante» cerebrale e la salute dei neuroni
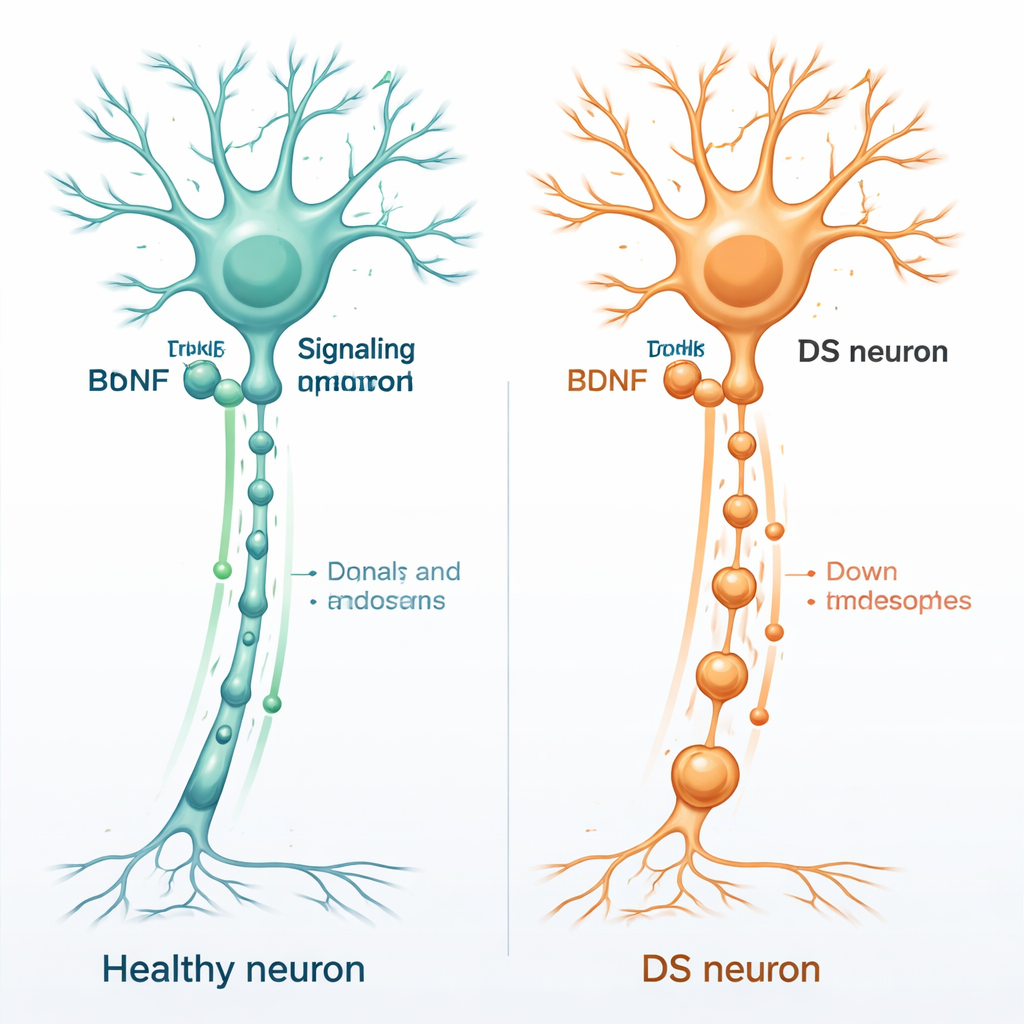
I neuroni sani dipendono da una serie di molecole di supporto chiamate neurotrofine, che funzionano come un fertilizzante per le cellule nervose. Una delle più importanti è il fattore neurotrofico derivato dal cervello, o BDNF. Il BDNF si lega a una proteina di ancoraggio sui neuroni chiamata TrkB, di solito alle estremità distali delle fibre nervose. Una volta che il BDNF si combina con TrkB, l’intero complesso viene internalizzato in piccole bolle di membrana e trasportato indietro lungo il lungo assone verso il corpo cellulare. Queste bolle mobili, note come endosomi di segnalazione, comunicano al nucleo quali geni attivare per mantenere il neurone vivo, connesso e adattabile.
Quando i contenitori intracellulari diventano troppo grandi
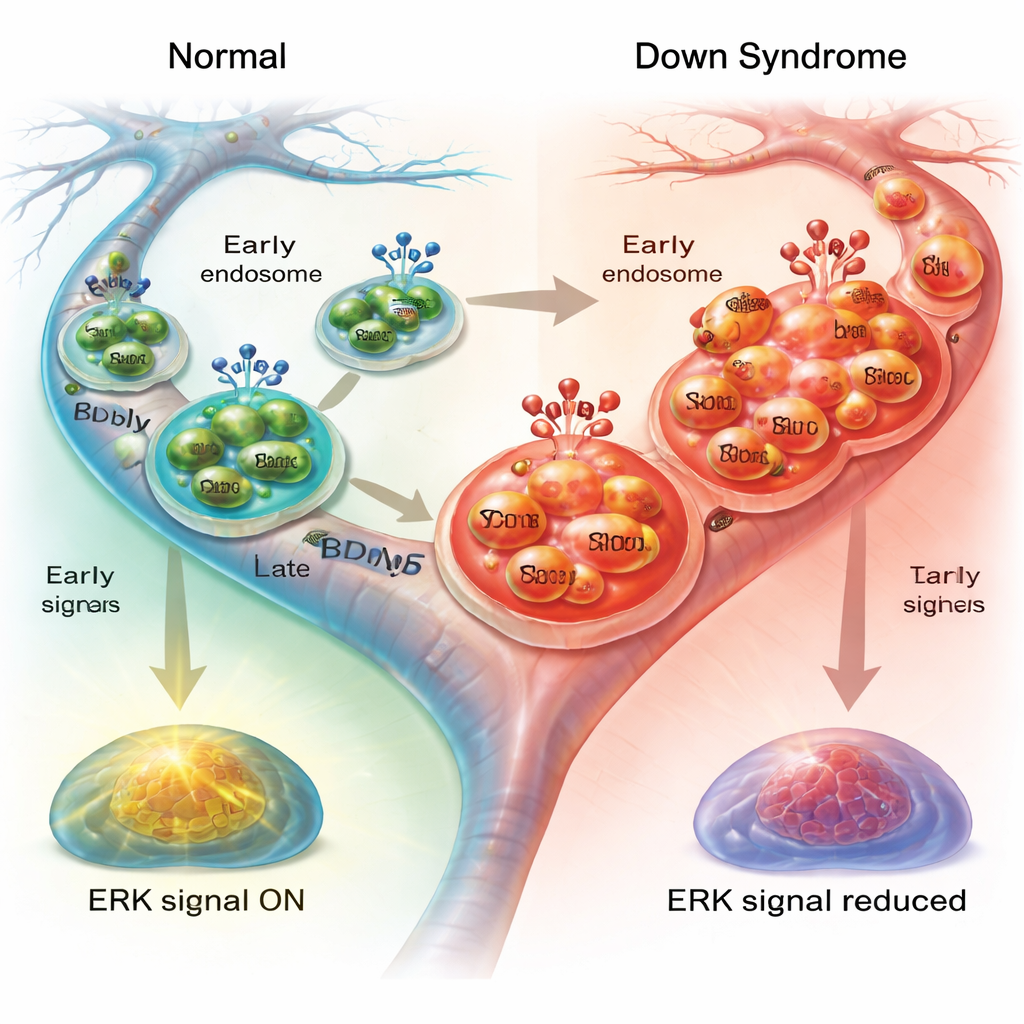
Il gruppo si è concentrato sui neuroni del prosencefalo basale, un insieme di cellule che sostiene fortemente memoria e attenzione ed è tra i primi a degenerare sia nella sindrome di Down sia nella malattia di Alzheimer. Utilizzando un modello murino della sindrome di Down chiamato Dp1Tyb, hanno colorato i neuroni per un marcatore degli endosomi precoci e li hanno confrontati con neuroni normali. I neuroni della sindrome di Down contenevano molti più endosomi precoci e questi erano oltre il 50% più grandi del normale. Queste strutture sono regolate da Rab5, un interruttore molecolare che aiuta a formare e smistare questi «contenitori» intracellulari. I ricercatori hanno rilevato che Rab5 era bloccato in uno stato iperattivo nei neuroni della sindrome di Down, anche prima della stimolazione con BDNF, suggerendo che il sistema endosomiale fosse già portato in sovraccarico.
Ingorghi lungo la fibra nervosa
Successivamente, gli scienziati si sono chiesti se questo paesaggio interno distorto interferisse con il trasporto dei segnali BDNF. Hanno coltivato neuroni in dispositivi microfluidici che separano i corpi cellulari dalle terminazioni assonali, permettendo di stimolare soltanto le punte degli assoni. Seguendo traccianti fluorescenti innocui che condividono la stessa via di trasporto dei complessi BDNF–TrkB, hanno misurato la velocità con cui gli endosomi di segnalazione viaggiavano verso i corpi cellulari. Nei neuroni normali, l’aggiunta di BDNF rendeva gli endosomi circa il 30% più veloci e riduceva le pause, riflettendo una risposta robusta ai segnali di crescita. Nei neuroni della sindrome di Down, invece, il BDNF non riusciva ad accelerare il trasporto né a ridurre le pause. Un esperimento separato che ha seguito i recettori TrkB reali ha confermato che in meno casi questi raggiungevano con successo il corpo cellulare nelle cellule della sindrome di Down.
Segnali intracellulari attenuati
Perché queste bolle in movimento sostengano la salute neuronale, devono attivare vie di segnalazione interne una volta raggiunta la destinazione. Una via chiave coinvolge ERK1/2, una coppia di enzimi che trasmette il messaggio del BDNF al nucleo e aiuta a regolare lo scheletro cellulare e la macchina del trasporto. Quando i ricercatori hanno misurato l’attivazione di ERK1/2 dopo il trattamento con BDNF, hanno riscontrato un aumento netto nei neuroni normali ma una risposta molto più debole nei neuroni della sindrome di Down, particolarmente negli assoni. Il blocco di ERK1/2 in neuroni sani ha parzialmente riprodotto il trasporto lento osservato nelle cellule della sindrome di Down, rallentando gli endosomi e aumentando le pause. Al contrario, il blocco di ERK1/2 ha avuto scarso effetto aggiuntivo sui neuroni della sindrome di Down, coerente con una segnalazione già attenuata.
Cosa significa per l’invecchiamento cerebrale nella sindrome di Down
Nel complesso, i risultati suggeriscono un problema auto-rinforzante nei neuroni vulnerabili: Rab5 è iperattivo, gli endosomi precoci si ingrossano e i complessi BDNF–TrkB rimangono intrappolati in compartimenti che non si muovono efficacemente. Di conseguenza, meno segnali di crescita raggiungono il corpo cellulare, la segnalazione ERK1/2 è indebolita e la macchina che alimenta il trasporto a lunga distanza risulta ulteriormente compromessa. Nel corso degli anni, questo sistema di comunicazione difettoso potrebbe contribuire alla perdita precoce e grave dei neuroni del prosencefalo basale osservata nelle persone con Alzheimer correlato alla sindrome di Down. Evidenziando questo legame tra il «controllo del traffico» endosomiale e la segnalazione dei fattori di crescita, lo studio indica nuove idee terapeutiche mirate a normalizzare l’attività di Rab5, ripristinare la funzione degli endosomi e rafforzare le risposte a BDNF per aiutare a proteggere questi neuroni critici.
Citazione: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Parole chiave: Sindrome di Down, Malattia di Alzheimer, BDNF, trasporto assonale, endosomi