Clear Sky Science · it
La segnalazione endoteliale di IRE1 mantiene l'integrità della barriera emato-encefalica e limita la neuroinfiammazione dopo trauma cranico
Perché proteggere la parete interna del cervello è importante
Dopo un colpo alla testa, il danno immediato è solo una parte della storia. Nelle ore e nei giorni successivi, il cervello avvia una potente risposta di stress e immunitaria che può silenziosamente ampliare l'entità della lesione. Questo studio esplora come un piccolo sistema sensoriale dello stress all'interno delle cellule che rivestono i vasi sanguigni cerebrali contribuisca a mantenere sigillata e calma la parete interna del cervello — la barriera emato-encefalica — dopo un trauma cranico. Comprendere questa difesa nascosta potrebbe indicare nuove terapie per limitare le disabilità persistenti dopo un trauma cranico.
I guardiani del cervello sotto stress
Il cervello si affida a una barriera specializzata formata dalle cellule endoteliali, che rivestono l'interno dei vasi e controllano strettamente ciò che può passare dal sangue al tessuto cerebrale. Il trauma cranico (TBI) può compromettere questa barriera emato-encefalica, permettendo a molecole infiammatorie e cellule immunitarie di entrare e aggravare il danno. All'interno di queste cellule endoteliali opera un sistema di controllo qualità chiamato risposta alle proteine non ripiegate, che aiuta le cellule a gestire lo stress all'interno di una struttura chiamata reticolo endoplasmatico. Uno dei suoi componenti chiave, noto come IRE1, si comporta da sensore e regolatore quando le cellule sono sotto pressione. I ricercatori si sono chiesti: questo sensore di stress endoteliale aiuta a difendere la barriera dopo il TBI, o peggiora la situazione?
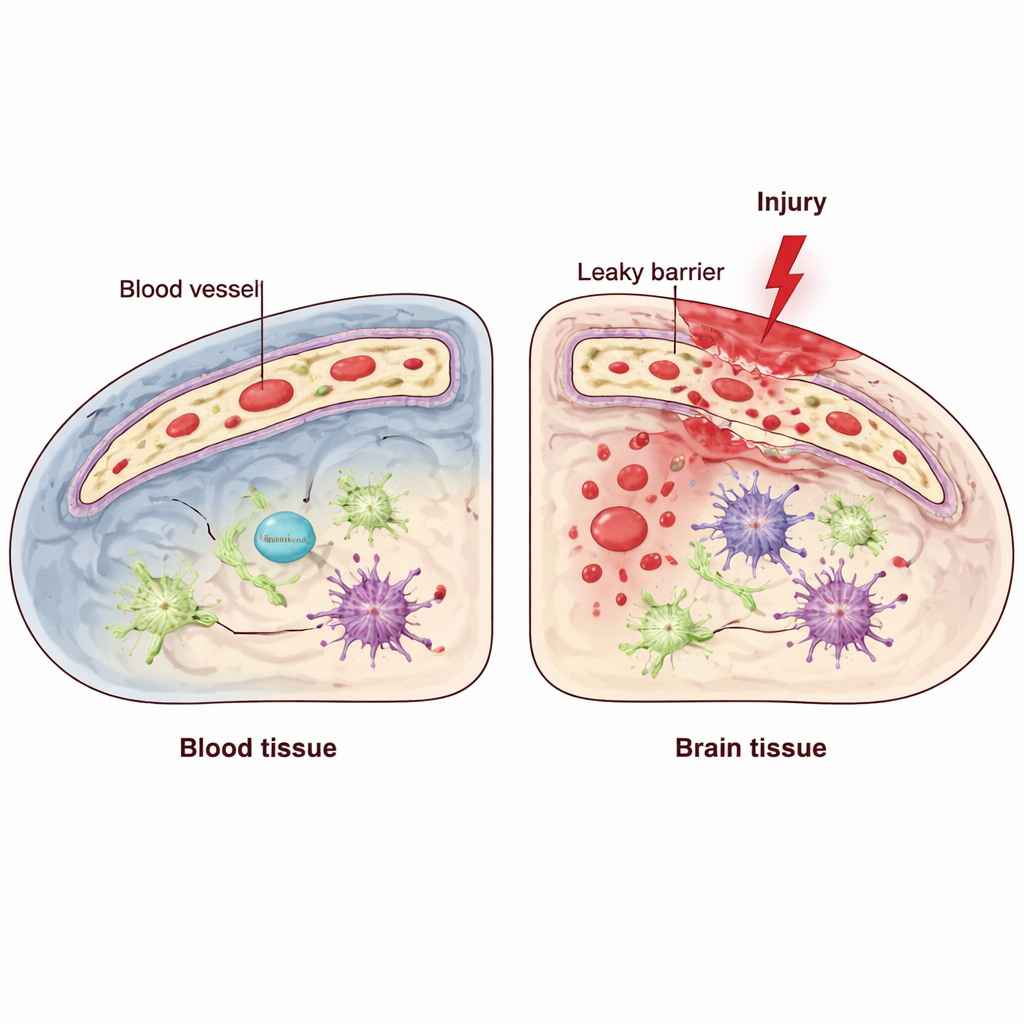
Spegnere un sensore cellulare nelle cellule dei vasi
Per scoprirlo, il gruppo ha utilizzato topi geneticamente modificati in cui IRE1 poteva essere spento selettivamente solo nelle cellule endoteliali. Hanno quindi creato una lesione controllata nell'area motoria della corteccia, riproducendo aspetti del TBI umano, e hanno confrontato questi animali con fratelli di cucciolata normali. Hanno testato il movimento con prove che misurano l'equilibrio e la precisione del posizionamento delle zampe, ed esaminato il tessuto cerebrale con microscopia ad alta risoluzione e tecniche molecolari. Nei topi normali l'attività di IRE1 aumentava nelle cellule dei vasi vicino alla lesione poco dopo il trauma, suggerendo che le cellule endoteliali percepiscono e rispondono rapidamente allo stress. Quando IRE1 mancava specificamente in queste cellule, gli animali si comportavano peggio nei test motori, indicando una recupero funzionale meno efficace.
Vasi che perdono, più cellule immunitarie e neuroni morenti
I ricercatori hanno quindi esaminato quanto bene la barriera emato-encefalica resistesse. Normalmente grandi proteine plasmatiche come gli anticorpi rimangono all'interno dei vasi. Dopo il TBI è previsto un certo grado di perdita vicino alla lesione, ma i topi privi di IRE1 endoteliale mostravano una fuoriuscita molto più estesa di queste proteine nel cervello. La microscopia ha rivelato che una molecola di giunzione chiave, la VE-caderina, che aiuta a sigillare le cellule endoteliali tra loro, era ridotta nell'area lesa quando IRE1 mancava, nonostante il numero complessivo di vasi apparisse simile. Questa permeabilità era accompagnata da un'afflusso di cellule immunitarie nel cervello attorno alla lesione e da livelli elevati di segnali infiammatori. Nelle stesse regioni i neuroni mostravano maggiore tendenza alla degenerazione e alla morte programmata, e la zona di tessuto danneggiato che circondava il nucleo della lesione era visibilmente più ampia.
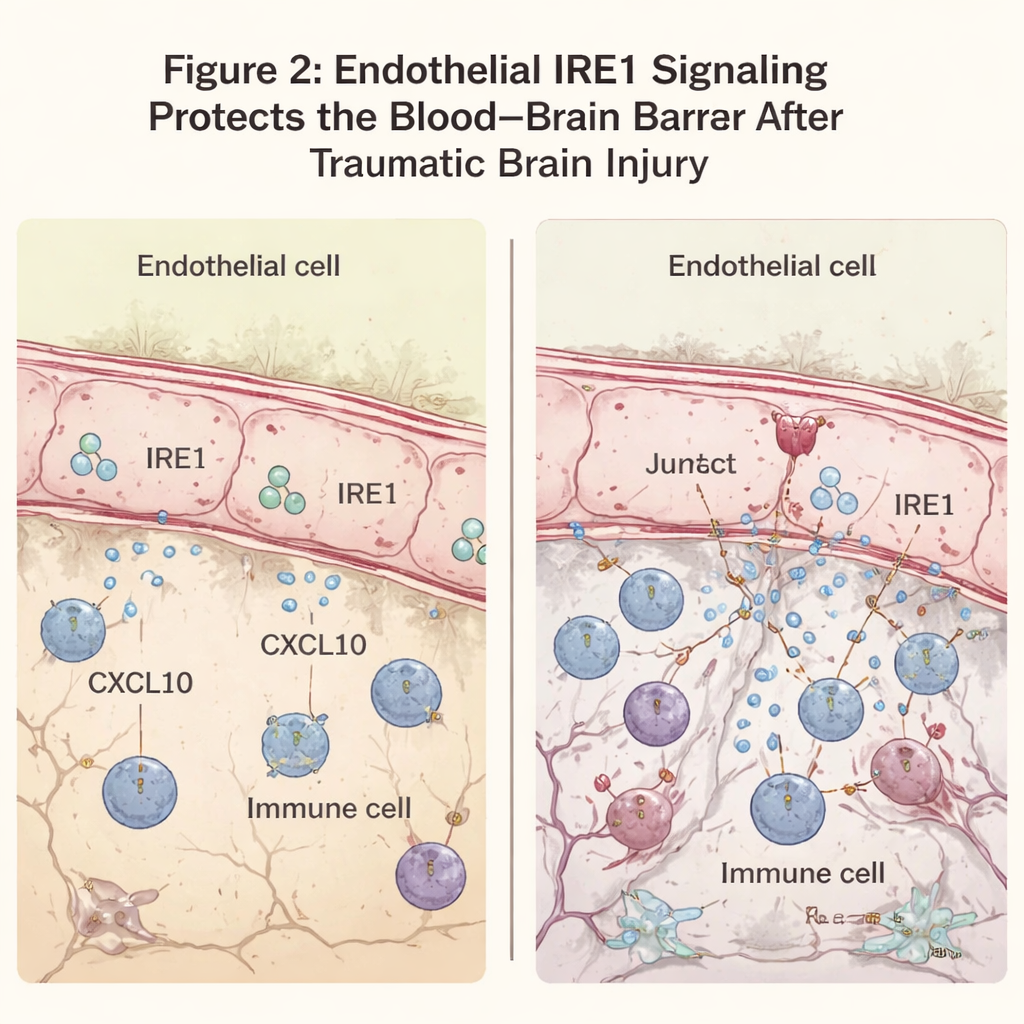
Un farmaco anti-stress calma la tempesta di segnali
Per capire i meccanismi molecolari, il gruppo ha analizzato quali geni venivano attivati dopo la lesione. Nei topi privi di IRE1 endoteliale, i geni coinvolti nelle risposte antivirali e infiammatorie risultavano fortemente aumentati. Tra questi spiccava CXCL10, una chemochina — una specie di segnale molecolare — che attrae cellule immunitarie e può indebolire ulteriormente la barriera. CXCL10 era particolarmente elevata nelle cellule endoteliali vicino alla lesione quando IRE1 era assente. In cellule endoteliali cerebrali coltivate esposte a uno stimolo infiammatorio, ridurre lo stress del reticolo endoplasmatico con un farmaco chiamato TUDCA abbassava sia l'attività di IRE1 sia la produzione di CXCL10. Somministrato a topi lesionati, TUDCA riduceva CXCL10 e i marcatori delle cellule immunitarie nella corteccia danneggiata e migliorava le prestazioni motorie, suggerendo che attenuare questa via di stress può alleviare il danno secondario.
Cosa significa per le persone con lesioni alla testa
In termini semplici, questo lavoro suggerisce che il sensore di stress IRE1 nelle cellule che rivestono i vasi cerebrali agisce da guardiano dopo un trauma cranico. Quando è presente e funziona, contribuisce a mantenere la barriera emato-encefalica compatta, riduce il rilascio di segnali chimici che richiamano cellule immunitarie e limita la diffusione dell'infiammazione e la perdita neuronale attorno alla lesione. Quando è disattivato, la barriera diventa più permeabile, le cellule immunitarie entrano in massa e più tessuto cerebrale viene danneggiato. Poiché le cellule dei vasi sono relativamente accessibili ai farmaci che circolano nel sangue, mirare alle loro risposte di stress — con composti come la TUDCA o con terapie future più precise — potrebbe diventare una strategia pratica per ridurre i danni a lungo termine dopo un trauma cranico.
Citazione: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Parole chiave: trauma cranico, barriera emato-encefalica, cellule endoteliali, neuroinfiammazione, stress cellulare