Clear Sky Science · it
CD36 aumenta la sensibilità delle cellule del carcinoma mammario triplo negativo alla ferroptosi indotta dal palmitato
Perché il grasso intorno ai tumori può essere amico e nemico
I tumori mammari crescono in un tessuto naturalmente ricco di grasso, e si sa che le cellule tumorali “si nutrono” degli acidi grassi vicini. Questo studio esplora una svolta sorprendente: nelle condizioni giuste, uno dei grassi più comuni nel corpo, l’acido palmitico, può effettivamente aiutare a uccidere una forma particolarmente aggressiva di cancro al seno innescando un tipo specifico di morte cellulare. Capire come avvenga questo processo potrebbe indicare nuove terapie per pazienti che attualmente hanno poche opzioni.
Un carcinoma mammario difficile da trattare sotto il microscopio
Il carcinoma mammario triplo negativo (TNBC) è privo dei recettori ormonali e dei fattori di crescita che molti farmaci moderni prendono di mira, rendendolo uno dei tipi di cancro al seno più difficili da trattare. Questi tumori vivono a stretto contatto con le cellule adipose, che rilasciano grandi quantità di acidi grassi, incluso il grasso saturo acido palmitico. I ricercatori hanno voluto capire se l’acido palmitico si limitasse ad alimentare la crescita tumorale o se potesse anche creare una debolezza sfruttabile per uccidere le cellule cancerose.
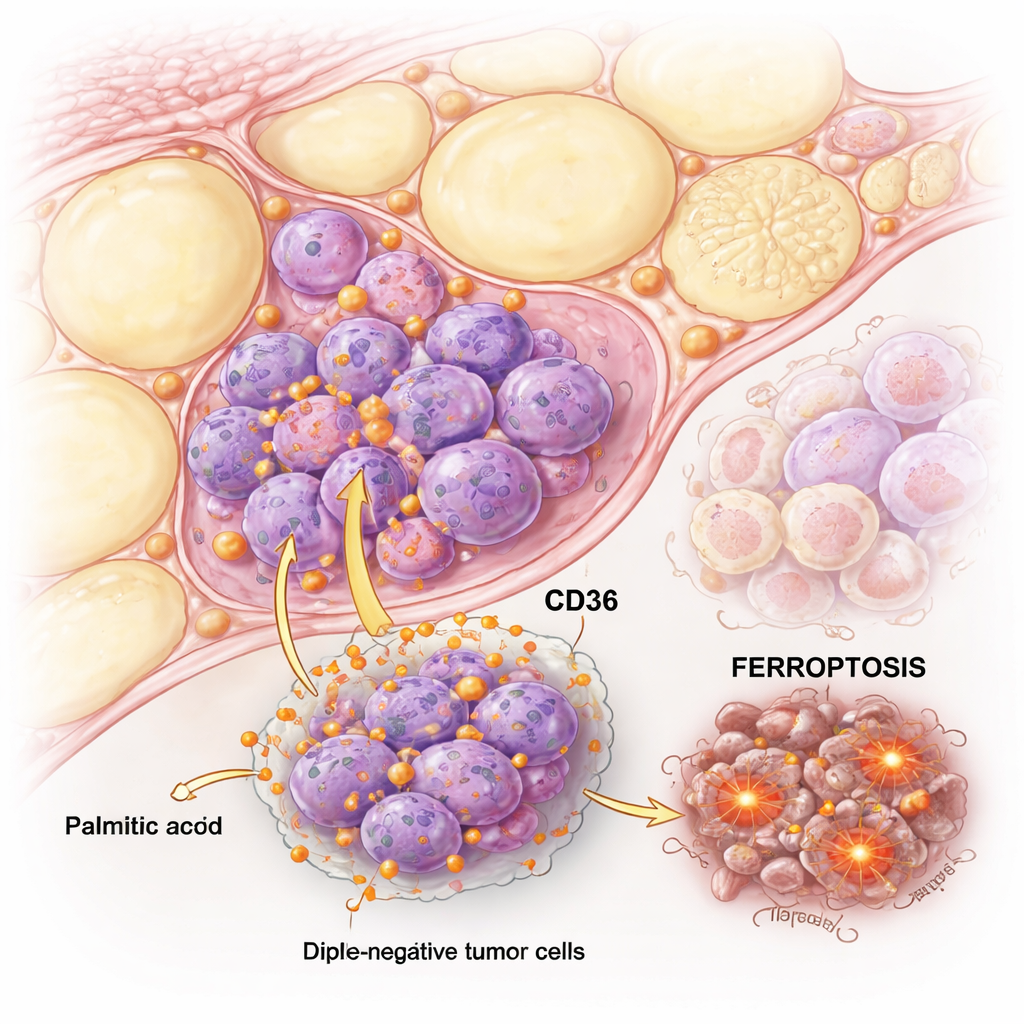
Quando l’acido palmitico spinge le cellule tumorali oltre il limite
Il team ha confrontato cellule TNBC con cellule del carcinoma mammario “luminale” sensibili agli ormoni ed le ha esposte a quantità crescenti di acido palmitico. Entrambi i tipi di cellule potevano essere danneggiati da dosi elevate, ma le cellule TNBC risultavano molto più sensibili. Test dettagliati hanno mostrato che nelle cellule luminali l’acido palmitico scatenava principalmente l’apoptosi classica, una forma ordinata di morte cellulare. Nelle cellule TNBC, invece, l’acido palmitico attivava sia l’apoptosi sia un altro percorso meno familiare chiamato ferroptosi, che dipende dal ferro e dalla distruzione dei lipidi delle membrane cellulari.
Una porta per gli acidi grassi chiamata CD36
Per capire perché le cellule TNBC reagivano in modo così diverso, i ricercatori si sono concentrati su CD36, una proteina sulla superficie cellulare che funziona come una porta per gli acidi grassi a catena lunga. Le cellule TNBC mostravano naturalmente livelli di CD36 molto più alti rispetto alle cellule luminali, e l’esposizione all’acido palmitico aumentava ulteriormente i livelli di CD36. Ciò significava che le cellule TNBC assorbivano più acido palmitico, accumulavano più lipidi danneggiati, producevano più specie reattive dell’ossigeno nei mitocondri e accumulavano più ferro libero all’interno della cellula—segnali chiave della ferroptosi. Quando CD36 veniva bloccata con un farmaco, o ridotta con strumenti genetici, la ferroptosi indotta dall’acido palmitico diminuiva nettamente.
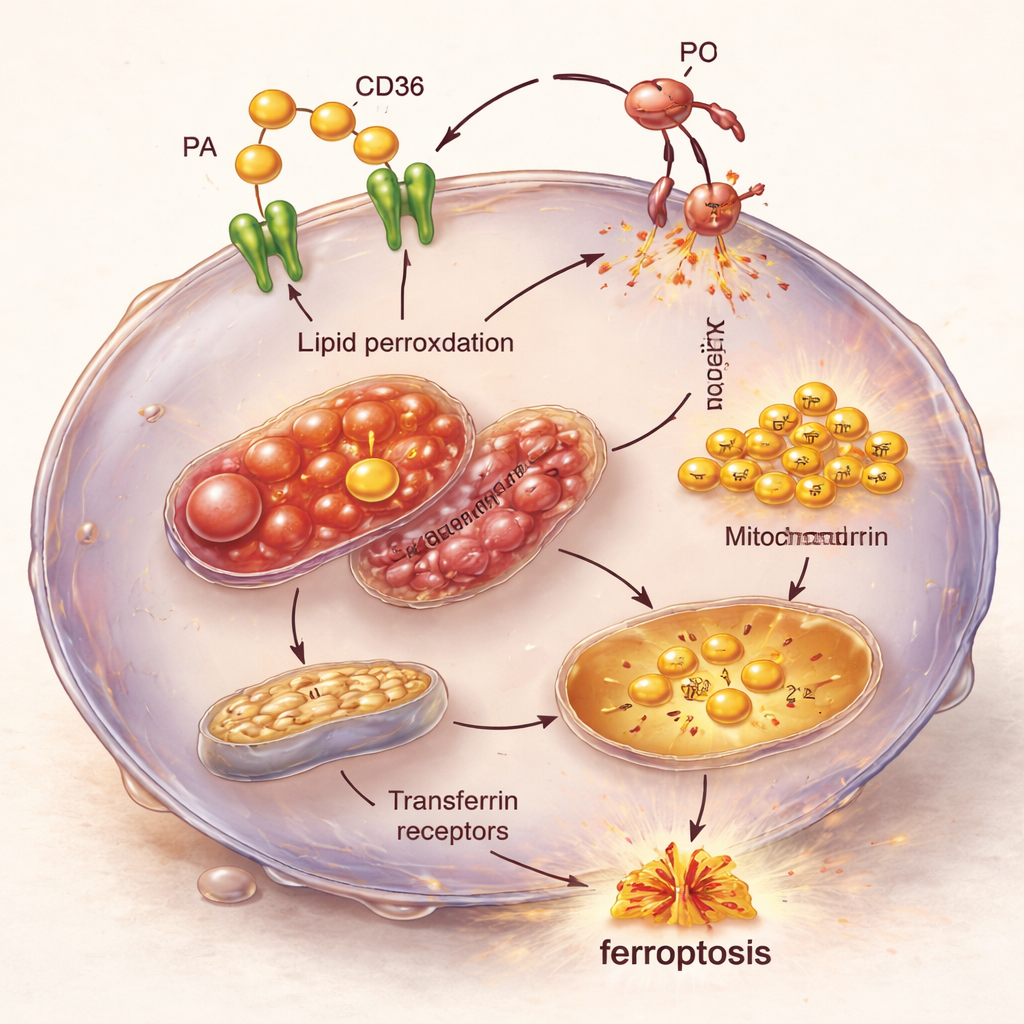
Ingrandendo la reazione a catena all’interno della cellula
La microscopia e le analisi dell’attività genica hanno rivelato la catena di eventi interna dietro questa vulnerabilità. Le cellule TNBC sovraccariche di acido palmitico e CD36 mostravano mitocondri gonfi e strutturalmente danneggiati e livelli crescenti di ferro introdotto tramite i recettori della transferrina. Allo stesso tempo, venivano attivati geni che favoriscono la ferroptosi, mentre venivano soppressi i geni che normalmente proteggono da questa forma di morte cellulare. Il risultato è una tempesta perfetta: eccesso di grasso in ingresso, maggiore disponibilità di ferro per guidare reazioni chimiche e difese indebolite contro il danno lipidico, che insieme spingono le cellule TNBC verso la ferroptosi.
Quali pazienti potrebbero trarne più beneficio?
Il cancro non è uniforme, nemmeno all’interno del TNBC. Utilizzando campioni tumorali cresciuti in topi e grandi banche dati di pazienti, gli autori hanno scoperto che CD36 era particolarmente elevato in un sottotipo di TNBC chiamato luminal androgen receptor (LAR), già noto per essere più sensibile alla ferroptosi. Altri sottotipi di TNBC con alto assorbimento di ferro tendevano anch’essi a mostrare livelli superiori di CD36. Questo schema suggerisce che CD36 potrebbe servire come marcatore per identificare i pazienti i cui tumori sono naturalmente predisposti a terapie basate sulla ferroptosi.
Trasformare un grasso comune in un alleato terapeutico
In termini semplici, questo lavoro mostra che un grasso abbondante nella dieta e nell’organismo, l’acido palmitico, può aiutare a uccidere certe cellule del carcinoma mammario triplo negativo quando esprimono alti livelli del trasportatore di grassi CD36. Favorendo il sovraccarico lipidico, l’accumulo di ferro e il danno alle membrane cellulari, CD36 rende queste cellule tumorali più propense a subire la ferroptosi, un destino distruttivo dal quale non possono sfuggire. Se terapie future riusciranno ad attivare in modo sicuro questo percorso—o a combinarlo con farmaci che indeboliscono ulteriormente le difese cellulari—i clinici potrebbero trasformare questa debolezza metabolica in un nuovo, più preciso modo di attaccare alcuni dei tumori mammari più aggressivi.
Citazione: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Parole chiave: carcinoma mammario triplo negativo, ferroptosi, CD36, acido palmitico, metabolismo tumorale