Clear Sky Science · it
Deubiquitinazione mediata da USP30 dell’esochinasi 2 controlla il destino metabolico del glucosio e la progressione tumorale
Come le cellule tumorali riorientano l’uso dello zucchero
Le cellule tumorali sono famose per la loro “voglia di dolce”: bruciano lo zucchero in modi insoliti per alimentare una rapida crescita. Questo studio individua un nuovo interruttore, una proteina chiamata USP30, che aiuta le cellule tumorali a decidere come impiegare il glucosio. Regolando con precisione un’altra proteina, l’esochinasi 2 (HK2), USP30 può spingere le cellule cancerose a bruciare più zucchero e a crescere più velocemente, indicando un nuovo possibile bersaglio per futuri farmaci antitumorali. 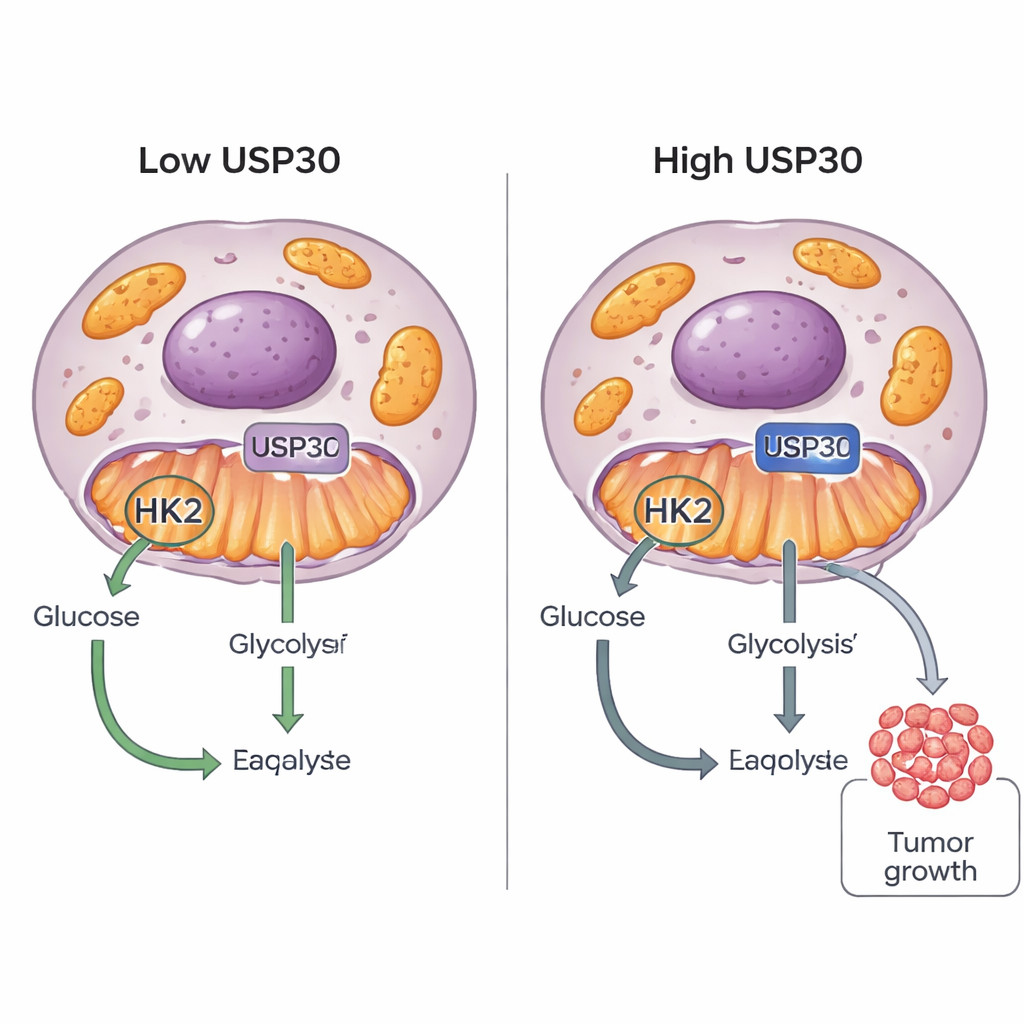
Uno stile di vita affamato di zucchero all’interno dei tumori
La maggior parte delle cellule sane estrae energia dai nutrienti in modo efficiente, ma molte cellule cancerose preferiscono una via rapida e meno efficiente chiamata glicolisi aerobica, nota anche come effetto Warburg. Assorbono grandi quantità di glucosio e lo convertono rapidamente in lattato, anche quando l’ossigeno è abbondante. Questa strategia fa più che produrre energia: fornisce mattoni per DNA, lipidi e proteine, aiuta i tumori a sopportare lo stress e può indebolire le risposte immunitarie. Alla porta d’ingresso di questo percorso c’è l’esochinasi, un enzima che aggiunge un gruppo fosfato al glucosio in entrata, impegnandolo nella successiva degradazione e nelle reazioni di supporto alla crescita.
Un enzima mitocondriale sotto i riflettori
USP30 è un enzima posizionato sulla superficie esterna dei mitocondri, le centrali energetiche della cellula. Appartiene a una famiglia di “deubiquitinasi” che rimuovono piccole etichette proteiche chiamate ubiquitina da altre proteine, modificandone spesso la stabilità, la localizzazione o l’attività. USP30 era già noto per ruoli nelle cellule cerebrali e nel controllo della qualità mitocondriale, ma il suo impatto sul cancro non era chiaro. Analizzando grandi database genomici tumorali, i ricercatori hanno osservato che i tumori con livelli più alti di USP30 tendevano a mostrare firme metaboliche di maggiore consumo di glucosio e minore ossidazione dei grassi, suggerendo che USP30 potrebbe favorire lo spostamento dei tumori verso uno stile di vita alimentato a zucchero.
Collegare USP30 ai guardiani dello zucchero della cellula
Per esplorare questo legame, il gruppo ha ridotto o eliminato USP30 in diverse linee cellulari tumorali e ha misurato come processavano l’energia. Usando strumenti che tracciano in tempo reale la produzione di acido e l’uso di ossigeno, hanno scoperto che la perdita di USP30 riduceva marcatamente sia la glicolisi sia la respirazione mitocondriale. La produzione di lattato e il consumo di glucosio sono diminuiti, indicando che il motore dello smaltimento dello zucchero delle cellule si era rallentato. Una serie di esperimenti di spettrometria di massa ha poi rivelato che USP30 interagisce fisicamente con diversi enzimi legati al metabolismo del glucosio, in particolare le esochinasi HK1 e HK2. Test successivi hanno mostrato che questa interazione dipende dall’attività catalitica di USP30 e avviene in modo diretto, non solo tramite partner indiretti.
Una presa molecolare precisa sull’esochinasi 2
Approfondendo, i ricercatori hanno scoperto che USP30 rimuove tipi specifici di catene di ubiquitina—le cosiddette connessioni atipiche—da HK1 e HK2. Per HK2, questa modifica avviene su un singolo amminoacido cruciale, la lisina 144 (K144). Quando K144 è mutata in modo da non poter più portare ubiquitina, HK2 diventa più stabile, si lega più saldamente a una proteina canale chiamata VDAC1 sui mitocondri e mostra un’attività enzimatica maggiore. Cellule ingegnerizzate per portare questa mutazione K144 indirizzavano più HK2 verso i mitocondri, bruciavano più glucosio, rilasciavano più lattato e mostravano crescita e movimento più rapidi in coltura. Nei topi, i tumori derivati da cellule con HK2 mutato in K144 crescevano più grandi e più rapidamente rispetto a quelli con HK2 normale, evidenziando la potenza di questo piccolo interruttore molecolare. 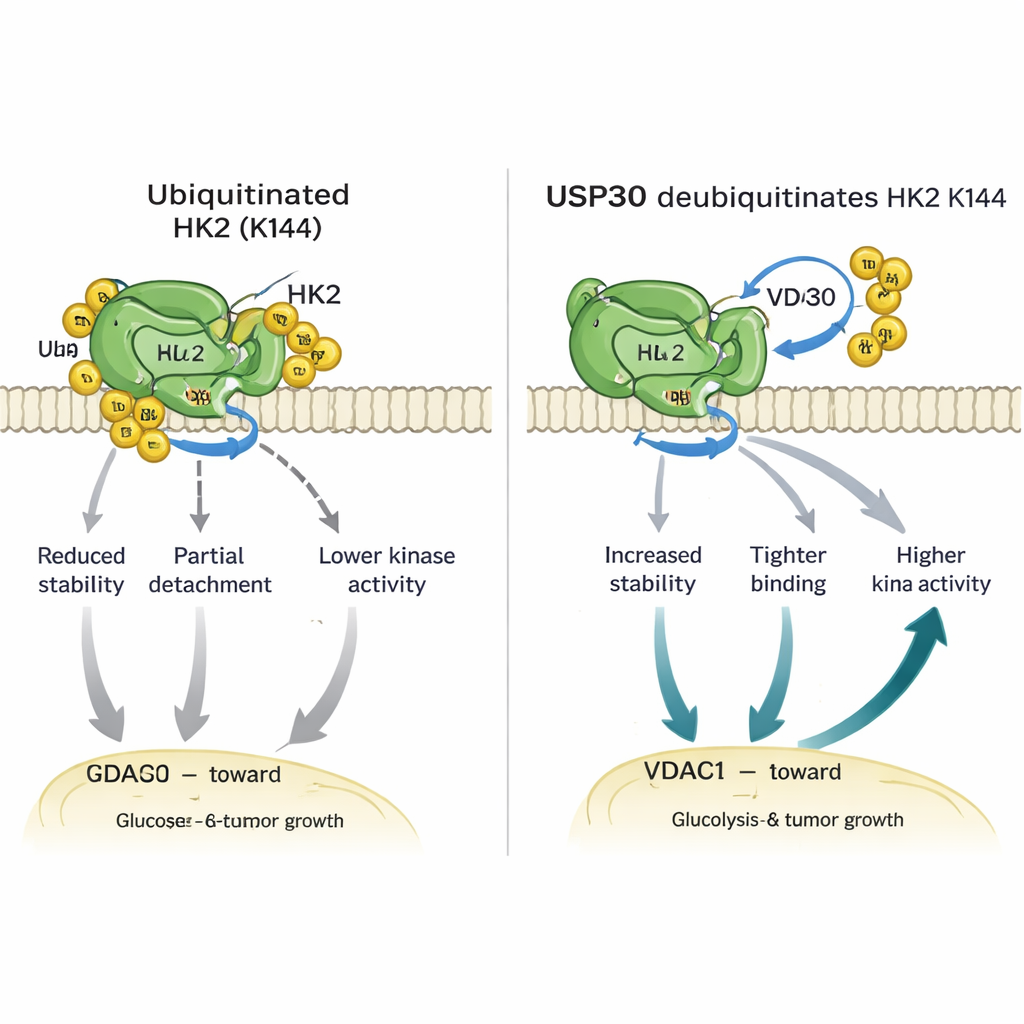
Trasformare un interruttore metabolico in un vantaggio di crescita
Questi risultati delineano una catena di eventi chiara: USP30 si lega a HK2, rimuove le etichette di ubiquitina da K144 e, così facendo, mantiene HK2 attiva e ancorata ai mitocondri. Questo potenzia la glicolisi, alimenta la divisione e la migrazione delle cellule tumorali e accelera infine la crescita tumorale. Quando USP30 manca o è inattivo, HK2 diventa meno stabile e meno efficace, e le cellule cancerose perdono parte del loro vantaggio metabolico. In termini non specialistici, USP30 agisce come un meccanico che mantiene il motore zuccherino della cellula tumorale ben regolato e saldamente fissato—rimuovi il meccanico e il motore inceppa.
Cosa significa per i futuri trattamenti contro il cancro
Per un non esperto, il messaggio principale è che le cellule tumorali dipendono da un controllo finemente regolato di come bruciano lo zucchero, e USP30 è una manopola appena scoperta su quel pannello di controllo. Stabilizzando HK2 in un sito specifico, USP30 aiuta i tumori a mantenere un metabolismo affamato di glucosio e a crescere più aggressivamente. Farmaci che inibiscono USP30, o che interrompono la sua presa su HK2 alla lisina 144, potrebbero indebolire i tumori affamando il loro motore zuccherino senza necessariamente danneggiare le cellule normali allo stesso grado. Questo lavoro aggiunge quindi un tassello importante al puzzle di come il cancro riorganizzi il metabolismo e suggerisce un nuovo e promettente approccio per terapie mirate.
Citazione: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Parole chiave: metabolismo del cancro, glicolisi, eso chinasi 2, USP30, effetto Warburg