Clear Sky Science · it
RNA circolari nella salute metabolica: colmare il divario tra biologia molecolare e terapia
Perché piccoli anelli di RNA potrebbero influire su peso e salute
L’obesità viene spesso presentata come un problema semplice di forza di volontà e calorie, eppure molte persone faticano nonostante dieta e attività fisica. Questo articolo spiega come una classe di molecole genetiche di recente riscoperta—le RNA circolari, o circRNA—contribuisca a controllare se le nostre cellule adipose immagazzinano energia o la bruciano. Convertendo il grasso bianco “di deposito” verso il grasso bruno produttrice di calore, questi anelli di RNA potrebbero un giorno ispirare trattamenti di precisione per l’obesità e le malattie correlate, dal diabete di tipo 2 alla steatosi epatica.
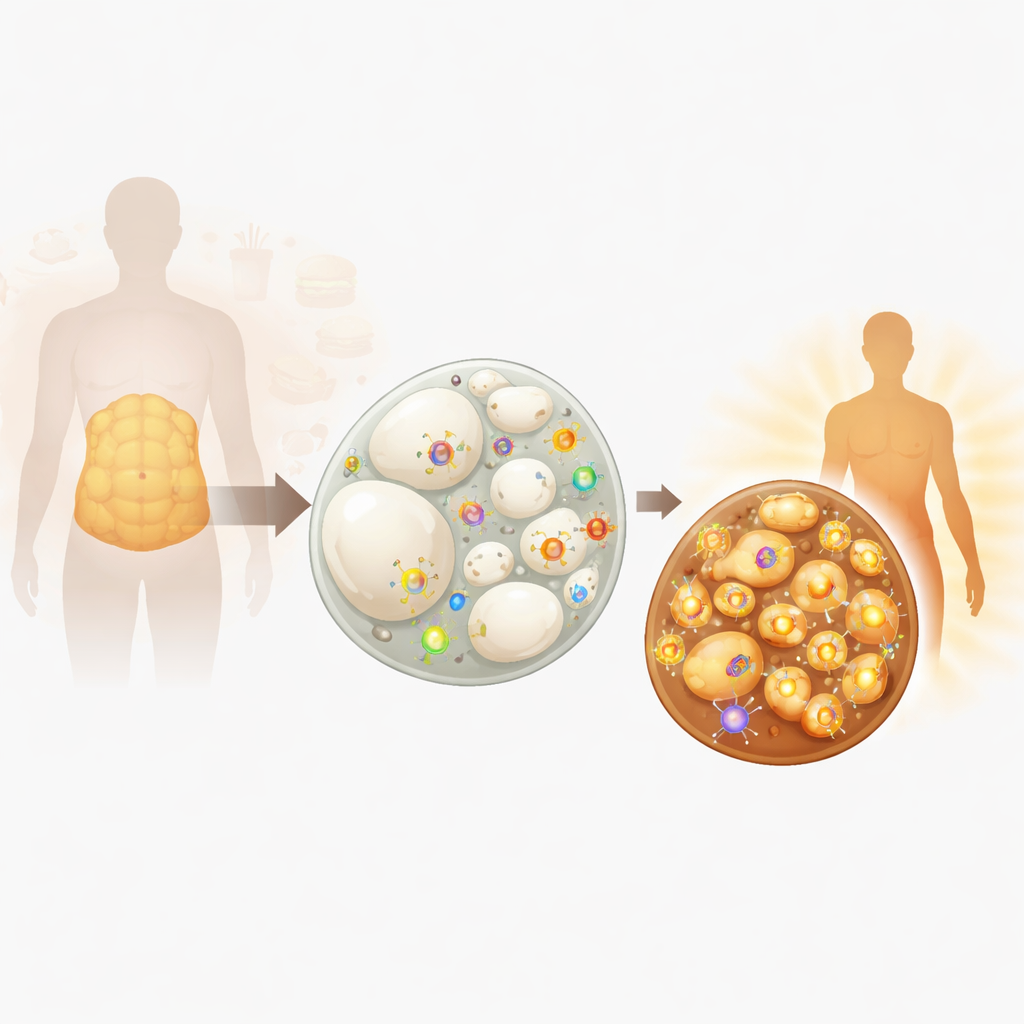
Le due facce del grasso corporeo
Tutto il grasso corporeo non si comporta allo stesso modo. Il grasso bianco, che ammortizza gli organi e si accumula intorno alla vita, funziona principalmente come un magazzino di energia: le sue cellule contengono una grande goccia lipidica e relativamente pochi mitocondri, le centrali energetiche della cellula. Il grasso bruno, concentrato nella parte superiore della schiena e del collo, è ricco di mitocondri che bruciano carburante per produrre calore, aiutandoci a mantenere la temperatura e limitando l’aumento di peso. In certe condizioni—come l’esposizione al freddo, l’eccesso di cibo o segnali indotti dall’esercizio—il grasso bianco può rimodellarsi in grasso “beige”, un tipo intermedio che acquisisce l’abilità del grasso bruno di bruciare calorie. Questo rimodellamento, chiamato brunicamento del grasso, è oggi visto come una strategia promettente per contrastare le malattie metaboliche.
Cosa rende speciali gli RNA circolari
L’RNA è solitamente pensato come una catena lineare che trasporta istruzioni genetiche dal DNA alle proteine. I circRNA sfidano quell’immagine scolastica: le loro estremità sono unite a formare anelli. Questa struttura chiusa li rende insolitamente stabili e in grado di sopravvivere all’interno delle cellule e persino nel sangue e in altri fluidi corporei. Lontani dall’essere scarti genetici, i circRNA possono legare microRNA (piccoli regolatori che silenziano i geni), ospitare specifiche proteine, influenzare l’attivazione genica e, in alcuni casi, indirizzare la produzione di brevi peptidi. Poiché particolari circRNA sono arricchiti nel tessuto adiposo e rispondono a dieta e ormoni, stanno emergendo come coordinatori chiave di come le cellule adipose usano e immagazzinano energia.
Come gli RNA circolari spingono il grasso bianco verso il bruno
Nel grasso bruno e beige molti circRNA mostrano attività diversa rispetto al grasso bianco. Alcuni agiscono come spugne molecolari, legando microRNA che altrimenti bloccherebbero geni necessari per la degradazione dei grassi o per la costruzione dei mitocondri. Per esempio, certi circRNA liberano geni che guidano la lipolisi (la rottura dei grassi) o attivano vie come AMPK e mTOR che riorientano il modo in cui le cellule gestiscono zuccheri e lipidi. Altri si legano direttamente a proteine che controllano la sintesi dei lipidi, l’ossidazione o la produzione di calore, stabilizzando enzimi utili o indirizzandoli verso nuovi compiti. Un numero crescente di circRNA codifica persino piccoli peptidi che modulano la funzione mitocondriale o cambiano il metabolismo cellulare, spingendo le cellule di grasso bianco verso uno stato più bruno e con maggiore consumo energetico.
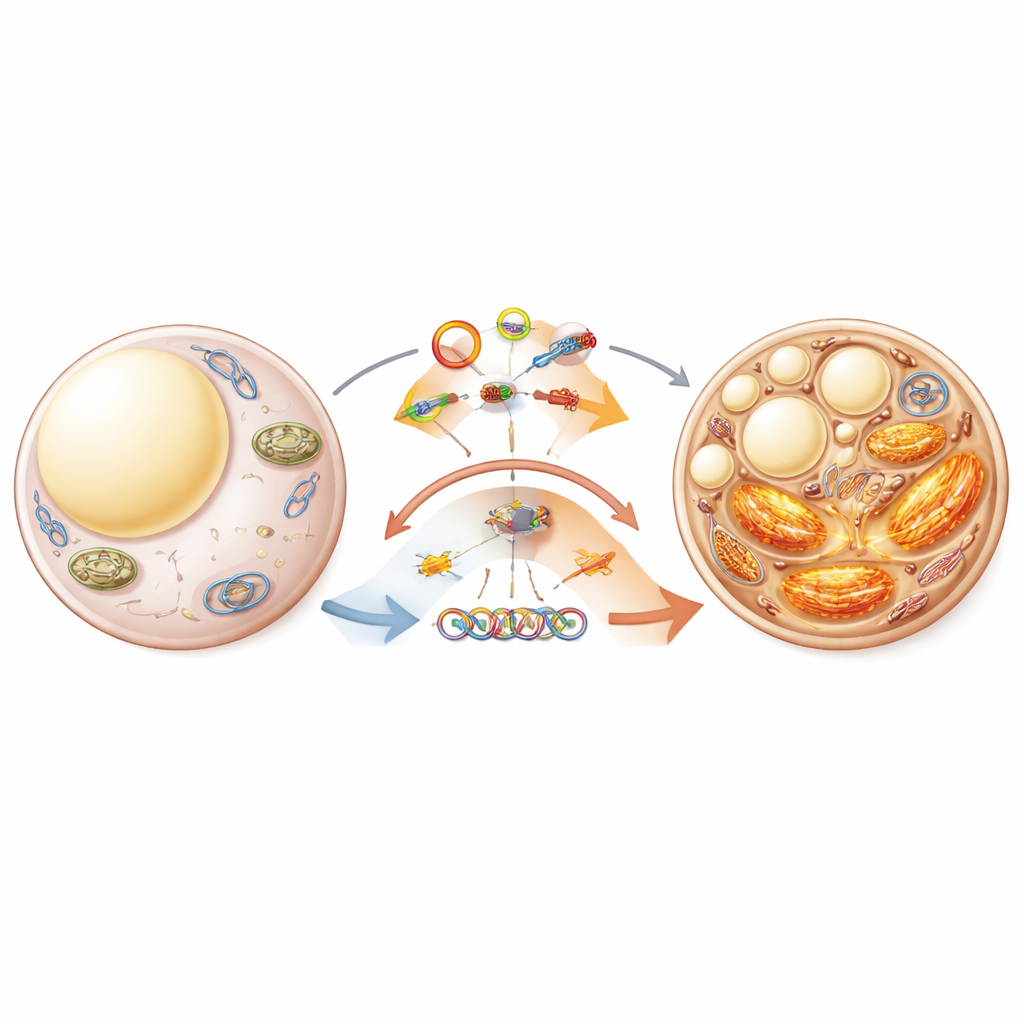
Regolare le centrali cellulari e i sistemi di stress
Il brunicamento del grasso dipende fortemente dai mitocondri e dal reticolo endoplasmatico, una rete di membrane che aiuta a gestire lo stress all’interno delle cellule. La rassegna mette in evidenza come i circRNA influenzino queste strutture interne. Alcuni circRNA proteggono i mitocondri promuovendo la rimozione ordinata di quelli danneggiati, mentre altri modulano questo processo interagendo con proteine sulla superficie mitocondriale. I circRNA modellano anche la risposta del reticolo endoplasmatico al sovraccarico, che può ostacolare o favorire il programma di brunicamento. Poiché mitocondri e reticolo endoplasmatico cooperano fisicamente e funzionalmente, i circRNA che operano a questo crocevia possono agire come interruttori principali per decidere se le cellule adipose accumulano energia o la dissipano sotto forma di calore.
Dalla scoperta in laboratorio alle terapie future
Grazie alla loro durabilità e precisione, i circRNA attirano attenzione come marcatori diagnostici, bersagli farmacologici e persino come molecole terapeutiche. I circRNA ingegnerizzati possono essere progettati per produrre peptidi benefici, modulare l’attività genica o fungere da vaccini a lunga durata, e si stanno sviluppando vettori come nanoparticelle o esosomi per veicolarli in tessuti come grasso e fegato. L’articolo avverte però che molti circRNA differiscono tra specie, gli strumenti di consegna sono ancora grezzi e la sicurezza a lungo termine è sconosciuta. Nel complesso, gli autori sostengono che comprendere e sfruttare i circRNA offre un modo per andare oltre le visioni dell’obesità incentrate solo sulle calorie, aprendo strade a trattamenti che rieduchino le nostre cellule adipose a comportarsi più come il grasso bruno e a ripristinare l’equilibrio metabolico.
Citazione: Huang, Y., He, T., Zheng, J. et al. Circular RNAs in metabolic health: bridging the gap between molecular biology and therapy. Cell Death Dis 17, 258 (2026). https://doi.org/10.1038/s41419-026-08450-5
Parole chiave: RNA circolare, brunicamento del grasso, obesità, malattia metabolica, tessuto adiposo bruno