Clear Sky Science · it
Cancellazione specifica nelle ovociti delle subunità di eIF2 provoca apoptosi degli ovociti di topo nei follicoli in accrescimento precoce tramite disfunzioni mitocondriali e danno al DNA
Perché conta la vita delle cellule uovo
Le donne nascono con tutte le cellule uovo che avranno mai, conservate all’interno di minuscole strutture nell’ovaio chiamate follicoli. Quando questi follicoli vanno persi troppo rapidamente, le donne possono sviluppare insufficienza ovarica prematura (POI), una condizione che porta a infertilità precoce e spesso a sintomi simili alla menopausa in giovane età. Questo studio sul topo pone una domanda fondamentale ma cruciale: cosa succede all’interno delle cellule uovo quando viene compromesso un passaggio chiave nella sintesi proteica, e come questo può portare alla perdita precoce della fertilità?
L’interruttore d’avvio della sintesi proteica
Per mantenersi sane, le cellule uovo devono continuamente produrre le proteine giuste al momento giusto. Una parte centrale di questo processo è una macchina molecolare composta da tre subunità chiamata eIF2, che aiuta ad avviare la produzione di proteine a partire dai messaggi genetici. I ricercatori hanno spento selettivamente due delle subunità di eIF2, chiamate eIF2α ed eIF2β, solo negli ovociti dei topi nelle fasi iniziali di crescita follicolare. Quando una delle due subunità mancava, le femmine diventavano completamente sterili. Le loro ovaie erano più piccole e la normale progressione dai follicoli precoci a quelli maturi, che rilasciano l’ovocita, si bloccava in gran parte, con molti meno follicoli a ogni stadio successivo. Nel tempo, praticamente tutti i follicoli venivano esauriti, riproducendo una condizione grave simile a una POI di insorgenza precoce.
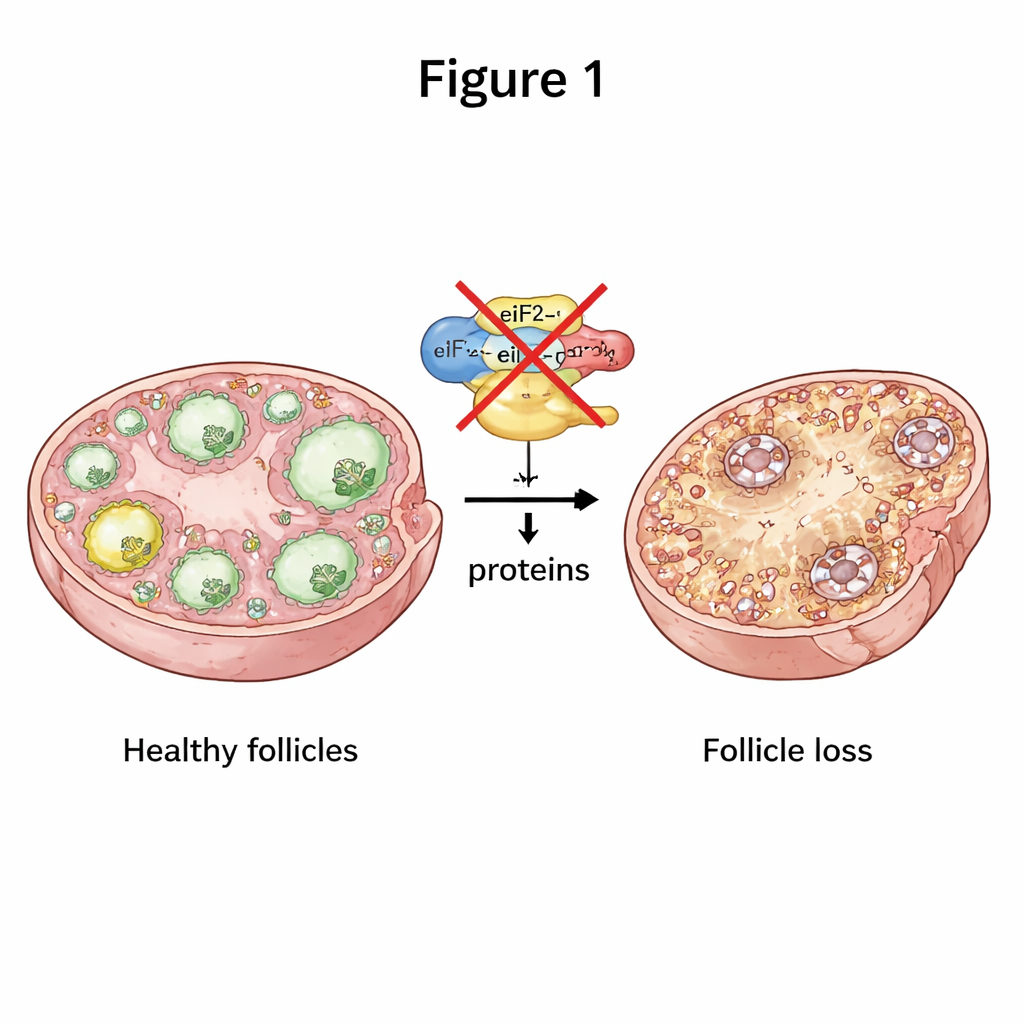
Quando la comunicazione nell’ovaio si rompe
I follicoli non sono solo ovociti isolati; sono stretti partenariati tra un ovocita e le cellule circostanti “di supporto” chiamate cellule della granulosa. Il gruppo ha osservato che senza eIF2β gli ovociti producevano molto meno di diverse proteine segnale cruciali che normalmente sostengono la crescita delle cellule della granulosa e la fornitura di nutrienti. I ponti fisici tra ovocita e cellule della granulosa risultavano disorganizzati e accorciati, e le microvilli sulla superficie dell’ovocita apparivano atrofizzate e danneggiate al microscopio elettronico. Le cellule della granulosa in questi follicoli si dividevano meno e morivano più frequentemente. Questo cedimento nella comunicazione bidirezionale impediva ai follicoli di crescere correttamente, spingendo l’ovaio verso la perdita dei follicoli.
Blackout nelle “pile” dell’ovocita
I mitocondri, spesso chiamati centrali energetiche della cellula, sono particolarmente importanti negli ovociti perché forniscono l’energia necessaria per la crescita e per lo sviluppo embrionale successivo. Negli ovociti carenti di eIF2β il tasso complessivo di nuova sintesi proteica è diminuito e molte proteine associate ai mitocondri erano ridotte. I mitocondri diventavano anormalmente lunghi, si raggruppavano vicino alla superficie cellulare e mostravano un potenziale di membrana più debole, livelli energetici (ATP) inferiori e un numero ridotto di copie del DNA mitocondriale. Contemporaneamente, le cellule accumulavano alti livelli di specie reattive dell’ossigeno (ROS), molecole ossigeno‑reattive aggressive che possono danneggiare componenti cellulari. Nel complesso, questi cambiamenti rivelano un profondo collasso della dinamica e della funzione mitocondriale.
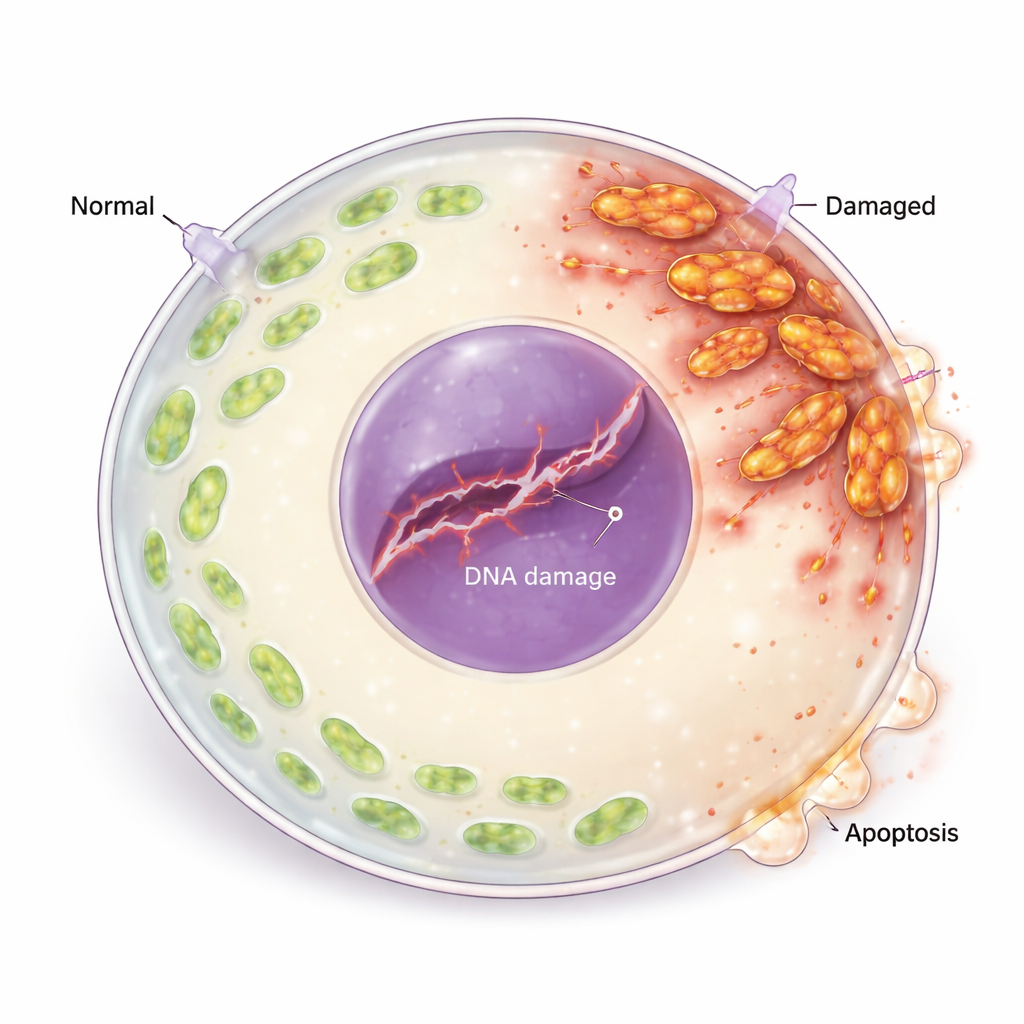
Dallo stress ossidativo al danno al DNA e alla morte cellulare
Le ROS eccessive non danneggiavano solo i mitocondri; ferivano anche il materiale genetico dell’ovocita. I ricercatori hanno osservato l’aumento di marcatori di rottura dei filamenti di DNA e l’attivazione della risposta cellulare al danno del DNA, incluse proteine che rilevano e segnalano lesioni genetiche. Una proteina chiave per la riparazione risultava ridotta, suggerendo che i danni non venivano riparati in modo efficiente. A valle, l’equilibrio dei regolatori di vita e morte si spostava: le proteine pro‑apoptotiche aumentavano mentre quelle protettive diminuivano, e gli ovociti mostravano segni chiari di morte programmata (apoptosi). Quando il gruppo ha trattato gli ovociti con un antiossidante (N‑acetilcisteina), i livelli di ROS sono diminuiti, i marcatori di danno al DNA e di apoptosi si sono ridotti e la maturazione degli ovociti è migliorata, collegando direttamente lo stress ossidativo alla perdita degli ovociti.
Cosa significa per l’insufficienza ovarica precoce
Seguendo gli eventi da un singolo complesso molecolare (eIF2) alla sintesi proteica difettosa, al collasso mitocondriale, allo stress ossidativo, al danno al DNA e infine alla morte delle cellule uovo, questo lavoro delinea una catena dettagliata di eventi che può distruggere la riserva ovarica. Lo studio rafforza l’idea che mutazioni nei fattori che avviano la traduzione, già osservate in alcune donne con POI, possono danneggiare direttamente gli ovociti attraverso questa via. Indica inoltre possibili strategie di intervento: antiossidanti, modulatori della risposta allo stress o trattamenti che proteggono i follicoli precoci (come l’ormone anti‑Mülleriano, che ha parzialmente preservato i follicoli dormienti in questi topi) potrebbero un giorno sostenere la fertilità in pazienti le cui ovaie sono vulnerabili a stress analoghi.
Citazione: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Parole chiave: insufficienza ovarica prematura, apoptosi degli ovociti, disfunzione mitocondriale, traduzione proteica, specie reattive dell'ossigeno