Clear Sky Science · it
Gli epatociti diploidi resistono al danno epatico indotto da acetaminofene grazie alla soppressione della segnalazione JNK
Perché alcuni fegati resistono meglio ai sovradosaggi
L’acetaminofene (paracetamolo) è presente in numerosi armadietti dei medicinali, eppure l’assunzione eccessiva è una delle principali cause di insufficienza epatica acuta. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: tutte le cellule del fegato rispondono allo stesso modo a un sovradosaggio? I ricercatori mostrano che un tipo particolare di cellula epatica, chiamata epatocita diploide, è sorprendentemente capace di sopravvivere e riparare il danno dopo un sovradosaggio di acetaminofene, grazie a un percorso di stress interno attenuato.
Due tipi di cellule epatiche, due destini diversi
Il fegato è insolito perché la maggior parte delle sue cellule funzionanti (epatociti) possiede set aggiuntivi di cromosomi, risultando così poliploide. Una frazione più piccola rimane diploide, con solo due set di cromosomi come la maggior parte delle cellule del corpo. Gli scienziati sapevano che questi gruppi differiscono nel modo in cui si dividono e rigenerano, ma il loro ruolo nel danno da farmaci era poco chiaro. Gli autori hanno usato topi appositamente allevati i cui fegati sono ricchi di cellule diploidi pur funzionando normalmente, e li hanno confrontati con topi tipici i cui fegati sono per lo più poliploidi. Entrambi i gruppi hanno ricevuto dosi basse e alte di acetaminofene per osservare come i loro fegati rispondevano nel tempo.
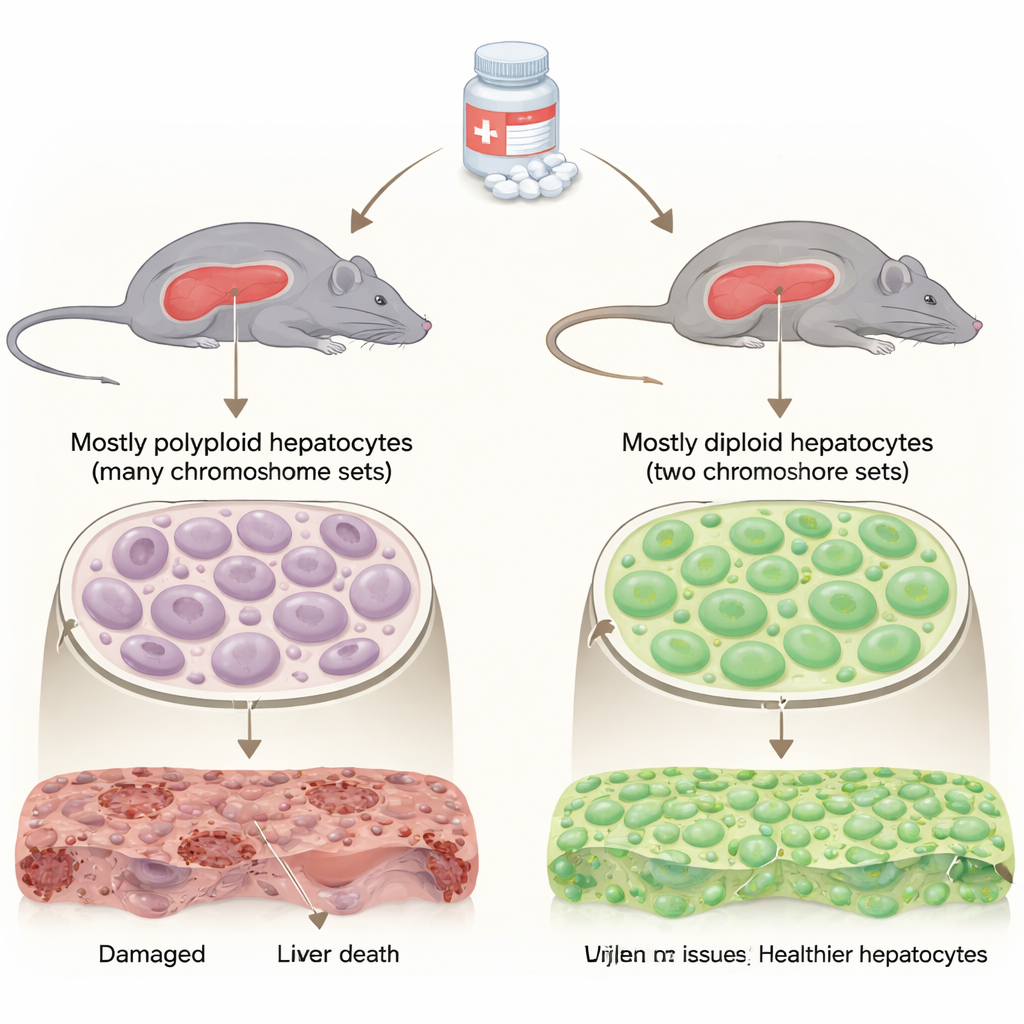
I fegati ricchi di diploidi sopravvivono ai sovradosaggi e si riprendono più rapidamente
Quando i topi ricevevano un sovradosaggio “rigenerativo” di acetaminofene, entrambi i gruppi mostravano danno epatico, ma i topi ricchi di diploidi andavano molto meglio. Avevano una maggiore sopravvivenza, livelli più bassi di enzimi epatici nel sangue (segno di minore danno) e aree più piccole di tessuto necrotico e DNA frammentato al microscopio. Anche a una dose più severa, “non rigenerativa” — che di solito causa danno persistente e morte — oltre la metà dei topi ricchi di diploidi sopravvisse, rispetto a meno di uno su dieci nei controlli. Nonostante questa protezione, i fegati ricchi di diploidi non restavano inattivi: attivavano le proteine della divisione cellulare prima, suggerendo che sia resistono al danno sia iniziano la ricostruzione più rapidamente.
Non il farmaco in sé, ma il wiring dello stress
Un’ipotesi ovvia era che i fegati ricchi di diploidi semplicemente metabolizzassero l’acetaminofene in modo diverso. Il team ha misurato gli enzimi chiave che convertono il farmaco nel suo sottoprodotto tossico, i livelli della molecola protettiva glutatione e la quantità di farmaco legata alle proteine epatiche. Tutto era simile tra i due tipi di topi, il che significa che entrambi producevano e gestivano la stessa quantità di tossina. La differenza cruciale è emersa più tardi, in come le cellule rispondevano a quella tossina. Nei fegati tipici, ricchi di poliploidia, geni e proteine coinvolti nello stress cellulare, nel danno al DNA e nelle lesioni mitocondriali erano fortemente attivati. Nei fegati ricchi di diploidi, queste risposte erano attenuate e si risolvevano prima, mentre i geni legati alla rigenerazione si attivavano prima.
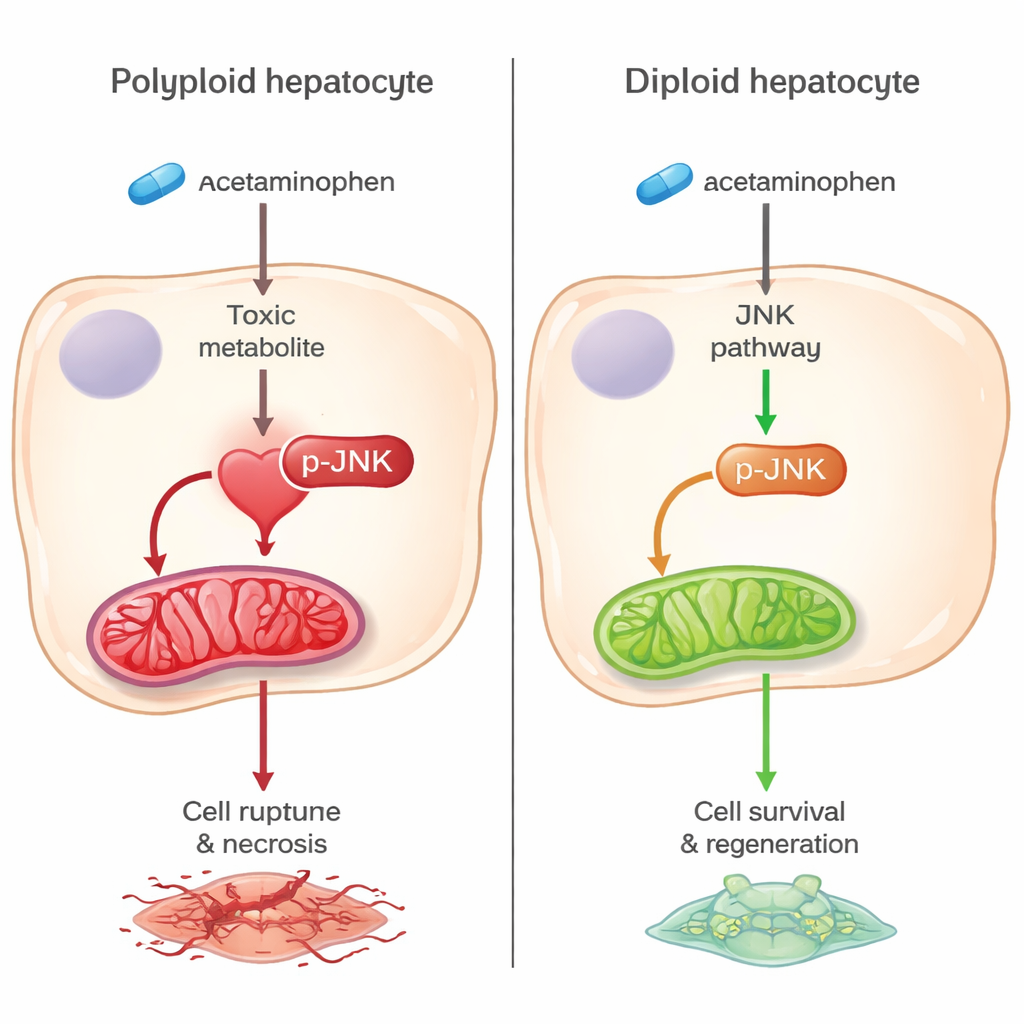
Una via di morte più silenziosa protegge le cellule diploidi
Il protagonista centrale di questa differenza è una via di segnalazione dello stress nota come via JNK. Nei fegati standard, il sottoprodotto tossico dell’acetaminofene attiva enzimi a monte che accendono JNK, il quale poi si sposta nei mitocondri, le centrali energetiche della cellula, promuovendo danno ossidativo e morte cellulare. Nei fegati ricchi di diploidi, l’attivazione di questi enzimi a monte e della JNK stessa era fortemente ridotta, e molta meno JNK raggiungeva i mitocondri. Anche i marcatori di stress ossidativo e di disgregazione mitocondriale risultavano inferiori, indicando che queste centrali energetiche restavano più integre. È importante notare che, quando gli stessi geni venivano eliminati solo nel fegato adulto senza modificare la ploidia cellulare, non si osservava protezione, indicando che la chiave è l’abbondanza di cellule diploidi — non la manipolazione genetica in sé.
Perché il tipo cellulare conta nel danno epatico umano
Per verificare se questo schema vale più in generale, i ricercatori hanno esposto in coltura cellule epatiche normali di topo all’acetaminofene. Le cellule con molti set cromosomici (altamente poliploidi) morivano più facilmente, mentre le cellule diploidi e a bassa ploidia erano più propense a sopravvivere. Insieme, i risultati sostengono un modello in cui gli epatociti diploidi sono i “primi soccorritori” del fegato di fronte a un danno tossico improvviso: attenuano una principale via di morte, preservano i mitocondri ed entrano rapidamente in rigenerazione. Le cellule poliploidi possono comunque essere utili in altri contesti, come la protezione dal cancro o l’adattamento a danni cronici a lungo termine. Ma per un sovradosaggio singolo, avere più epatociti diploidi potrebbe fare la differenza tra la guarigione e l’insufficienza epatica.
Citazione: Wilson, S.R., Delgado, E.R., Alencastro, F. et al. Diploid hepatocytes resist acetaminophen-induced liver injury through suppressed JNK signaling. Cell Death Dis 17, 203 (2026). https://doi.org/10.1038/s41419-026-08448-z
Parole chiave: sovradosaggio di acetaminofene, danno epatico, ploidia degli epatociti, segnalazione JNK, rigenerazione epatica