Clear Sky Science · it
La transglutaminasi 2 aggrava la sopravvivenza del cancro ovarico inattivando direttamente GSK3β
Perché questa ricerca conta per la salute delle donne
Il cancro ovarico è uno dei tumori femminili più letali perché viene spesso diagnosticato in fase avanzata e tende a recidivare anche dopo chemioterapie intensive. Questo studio mette in luce come una proteina poco conosciuta, la transglutaminasi 2 (TGase 2), aiuti le cellule del cancro ovarico a sopravvivere al trattamento e a diffondersi nell’organismo. Svelando questo alleato nascosto del tumore, il lavoro indica nuove strade per rendere più efficaci i farmaci esistenti e rallentare o fermare le metastasi letali.
Un motore nascosto all’interno dei tumori aggressivi
I medici osservano da tempo che molti tumori ovarici diventano resistenti alla chemioterapia e si diffondono ampiamente nella cavità addominale. Uno dei principali responsabili è un processo chiamato transizione epiteliale–mesenchimale (EMT), in cui le cellule tumorali perdono le loro connessioni, diventano più mobili e si comportano più da «esploratrici» invasive che da cellule di tessuto organizzato. Gli autori mostrano che la TGase 2, presente a livelli molto bassi nell’ovaio normale ma molto più elevata nei tumori ovarici, è fortemente associata a questo cambiamento. In un ampio pannello di campioni umani, i livelli di TGase 2 aumentavano progressivamente dalle lesioni iniziali ai tumori avanzati e metastatici, e la sua abbondanza corrispondeva strettamente all’attività di molti geni legati all’EMT che controllano il movimento cellulare, la crescita e la formazione dei vasi sanguigni. 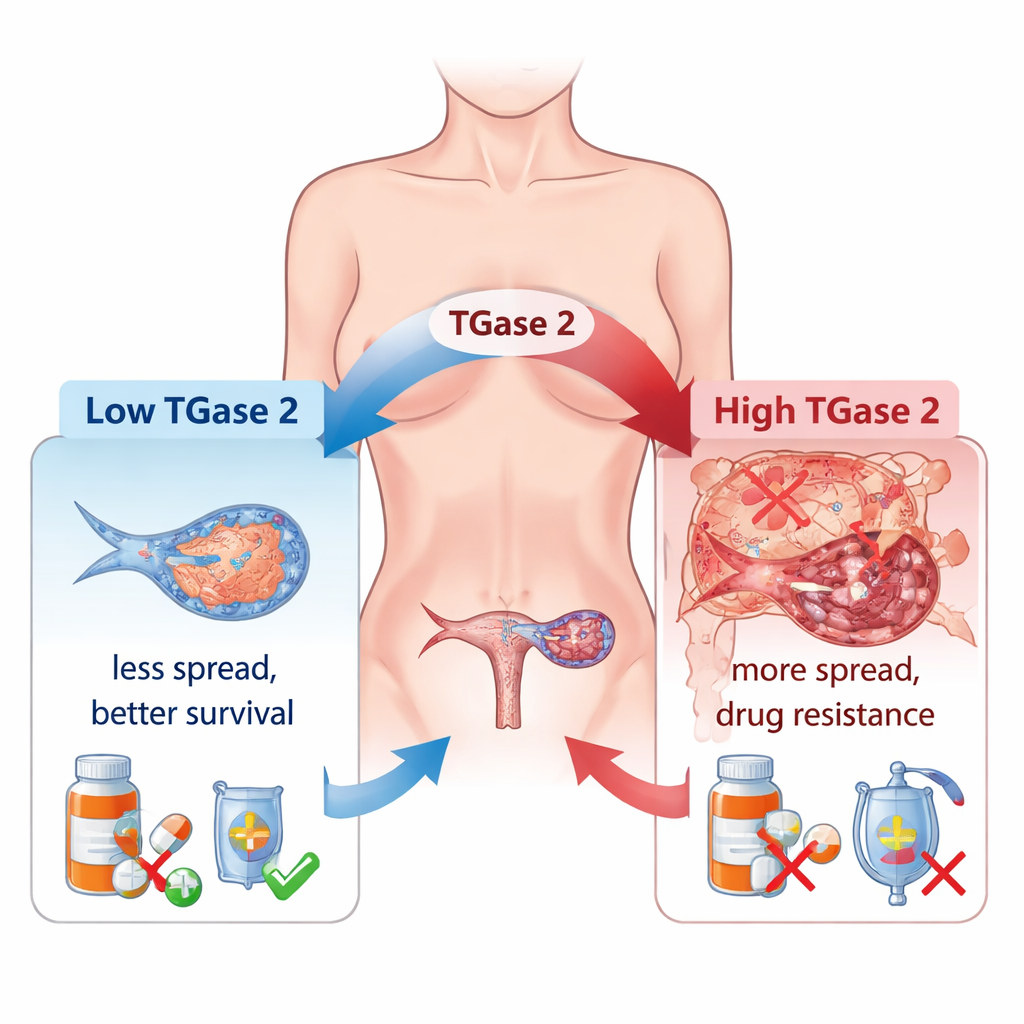
Come la TGase 2 disattiva un interruttore di sicurezza chiave
Per capire cosa fa concretamente la TGase 2 nelle cellule tumorali, i ricercatori si sono concentrati sulla sua relazione con un’altra proteina, GSK3β. In condizioni sane, GSK3β funziona come un freno all’invasione: mantiene bassi i livelli di una molecola di segnalazione chiamata β-catenina, che a sua volta limita l’attivazione dei geni che guidano l’EMT. Il gruppo ha scoperto che la TGase 2 si lega fisicamente a GSK3β e ne riduce sia l’attività sia la stabilità, indirizzandola verso la degradazione tramite il sistema di riciclaggio cellulare, un percorso chiamato autofagia. Quando la TGase 2 era abbondante, le cellule del cancro ovarico migravano più facilmente e mostravano livelli più alti di marcatori classici dell’EMT come fibronectina, vimentina e β-catenina. Riducendo la TGase 2 con strumenti genetici, queste caratteristiche invasive diminuivano e la segnalazione di β-catenina si attenuava, dimostrando che la TGase 2 disinnesca un cruciale interruttore di sicurezza contro le metastasi.
Dalle cellule tumorali agli animali vivi
Il gruppo ha quindi verificato se bloccare la TGase 2 potesse effettivamente rallentare il tumore negli animali. Hanno ingegnerizzato cellule di cancro ovarico privi del gene TGase 2 e le hanno impiantate nei topi. Rispetto ai topi inoculati con cellule tumorali normali, gli animali che ricevevano cellule carenti di TGase 2 sviluppavano un carico tumorale minore e vivevano più a lungo. In un modello separato che simula la diffusione del cancro tramite il flusso sanguigno, i topi iniettati con cellule prive di TGase 2 svilupparono molte meno e più piccole metastasi polmonari. Importante, questi depositi metastatici mostravano livelli più alti di GSK3β, coerente con l’idea che rimuovere la TGase 2 ripristini il freno naturale all’invasione e contribuisca a contenere la malattia.
Da un indizio di laboratorio a una strategia farmacologica
Poiché eliminare un gene non è praticabile nei pazienti, gli autori hanno testato una piccola molecola chiamata streptonigrina, nota in precedenza per legarsi allo stesso estremo della TGase 2 usato per afferrare altre proteine. Hanno trovato che la streptonigrina poteva interrompere l’interazione TGase 2–GSK3β nelle cellule, ridurne la colocalizzazione e limitare la migrazione delle cellule tumorali. In modelli murini di cancro ovarico, il trattamento orale con streptonigrina rallentò la crescita tumorale, ridusse le lesioni metastatiche e prolungò la sopravvivenza. Ancor più significativo, quando la streptonigrina veniva combinata con chemioterapici standard come cisplatino o paclitaxel, i topi vissero settimane in più rispetto alla sola chemioterapia. La chemioterapia da sola tendeva ad aumentare i livelli di TGase 2 e ad abbassare quelli di GSK3β, spingendo indirettamente le cellule verso l’EMT, ma l’aggiunta dell’inibitore di TGase 2 invertiva questa tendenza e frenava la nuova mobilità delle cellule. 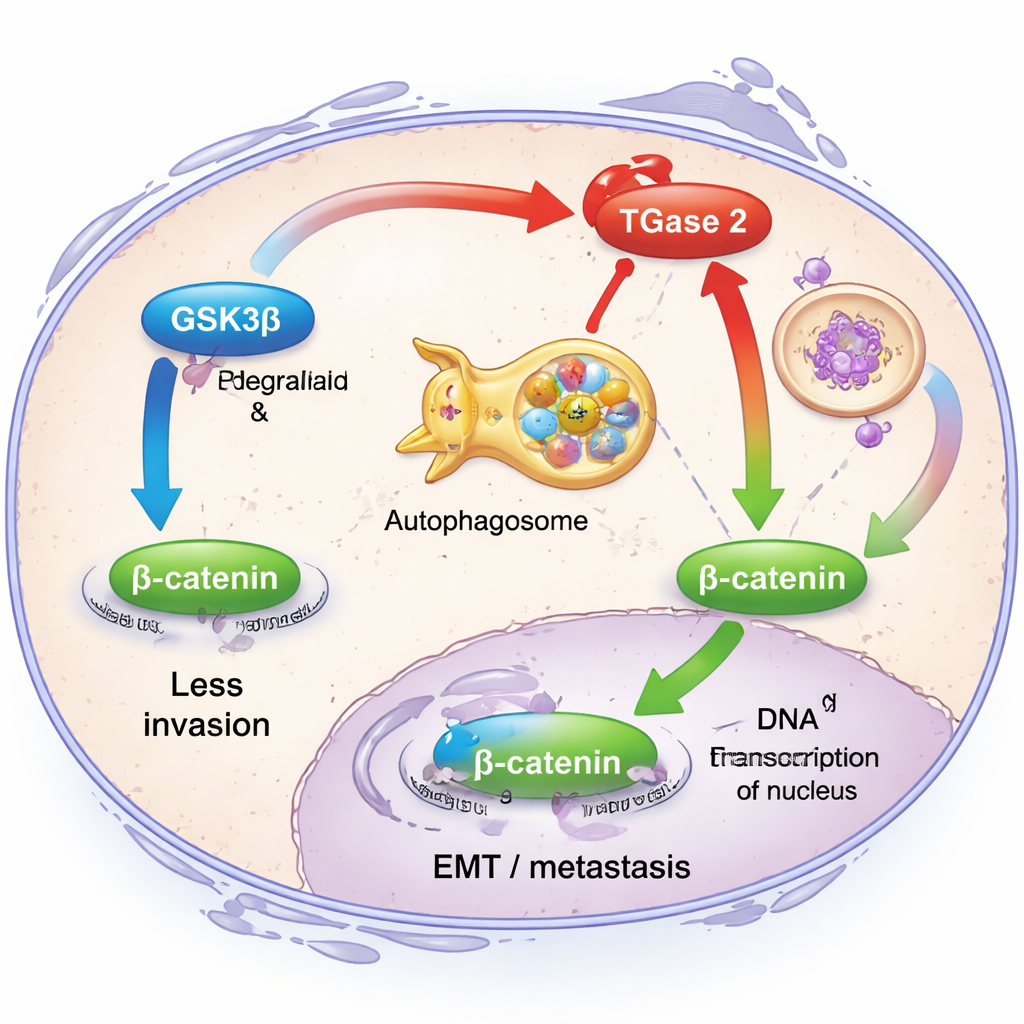
Cosa potrebbe significare per i trattamenti futuri
Per il pubblico non specialista, il messaggio principale è che le cellule del cancro ovarico sfruttano la TGase 2 per disattivare un freno innato contro le metastasi e per resistere agli effetti della chemioterapia. Disattivando direttamente GSK3β e stabilizzando β-catenina, la TGase 2 agevola la trasformazione dei tumori in forme più invasive e resistenti ai farmaci. Questo lavoro suggerisce che farmaci mirati alla regione N-terminale della TGase 2—come la streptonigrina o futuri composti più sicuri modellati su di essa—potrebbero rendere più efficaci le chemioterapie esistenti, ridurre il rischio di recidiva e migliorare la sopravvivenza. In termini semplici, colpire la TGase 2 potrebbe chiudere una «via di fuga» del cancro, mantenendo i tumori ovarici più sensibili ai trattamenti e meno capaci di diffondersi.
Citazione: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Parole chiave: cancro ovarico, resistenza ai farmaci, metastasi, transizione epiteliale mesenchimale, terapia mirata