Clear Sky Science · it
Inibizione dell’internalizzazione del recettore delle cellule B (BCR) indotta da autoantigene come strategia terapeutica nel linfoma diffuso a grandi cellule B (DLBCL)
Perché questo è importante per i pazienti
Il linfoma diffuso a grandi cellule B (DLBCL) è il tumore ematologico a crescita rapida più comune negli adulti e molti pazienti recidivano dopo la chemioterapia immunologica standard. Questo studio esplora un punto debole sorprendente in un sottoinsieme importante di questi tumori: la loro dipendenza da un’antenna di superficie cellulare chiamata recettore delle cellule B (BCR). Dimostrando che bloccare il modo in cui questa antenna viene internalizzata può compromettere la sopravvivenza delle cellule tumorali, il lavoro apre la strada al riposizionamento di farmaci antiemetici e antipsicotici di lunga data come coadiuvanti mirati contro il linfoma.
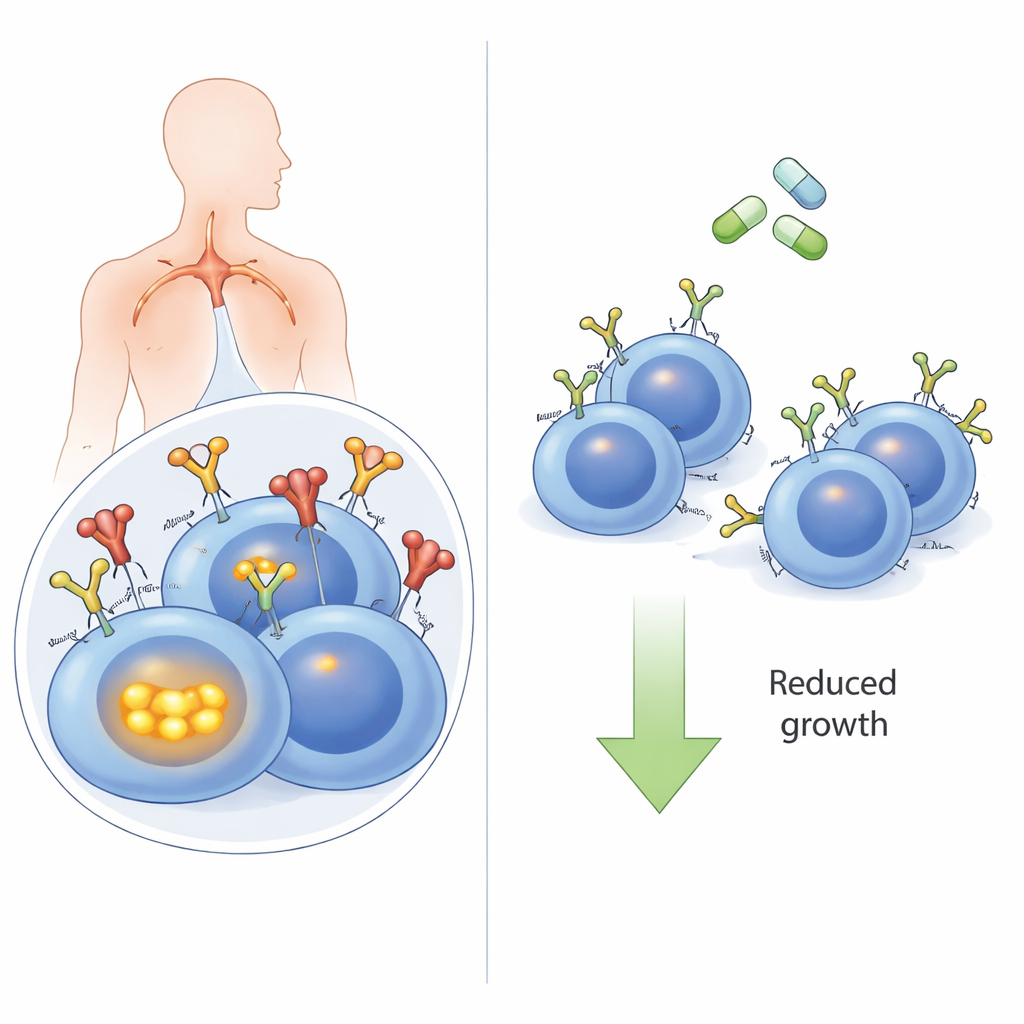
L’antenna della cellula tumorale
Le cellule B, un tipo di globulo bianco, usano il recettore delle cellule B sulla loro superficie per riconoscere le minacce. In molti DLBCL, specialmente nel sottotipo ad alto rischio “activated B‑cell” (ABC), questo stesso recettore viene dirottato per inviare segnali costanti di “sopravvivi e prolifera”. Spesso questi BCR riconoscono le molecole proprie dell’organismo (autoantigeni), che funzionano come un campanello difettoso. Quando gli autoantigeni si legano, il BCR fa più che segnalare in superficie: viene tirato dentro la cellula e si unisce a un aggregato proteico interno che include sensori come TLR9 e MYD88. Questo super‑complesso attiva quindi NFκB, una potente via di segnalazione che promuove la crescita. Fino a ora non era chiaro se questo viaggio verso l’interno del recettore fosse effettivamente necessario per i segnali che guidano il tumore.
Riprogettare l’antenna per testarne i limiti
Per rispondere a questa domanda, i ricercatori hanno usato l’editing genico CRISPR per modificare con precisione le “punte” del BCR in linee cellulari di linfoma. Hanno sostituito le regioni di riconoscimento naturali autoreattive con versioni che riconoscono l’ovalbumina, una proteina dell’uovo innocua usata come strumento di laboratorio. Questi recettori modificati non riconoscevano più i loro autoantigeni abituali, ma potevano comunque essere attivati in modo controllato con l’ovalbumina aggiunta. Nelle cellule di linfoma di tipo ABC, che normalmente dipendono dal legame con autoantigene, questo cambio ha ridotto nettamente l’attività di molti enzimi di segnalazione chiave e ha attenuato i geni rispondenti a NFκB. Le cellule crescevano più lentamente, nonostante avessero in realtà più BCR esposti in superficie, dimostrando che l’impegno costante da parte degli autoantigeni e la successiva segnalazione interna sono critici per la loro sopravvivenza.
Portare i recettori all’interno: un passo cruciale
Il gruppo ha quindi esaminato direttamente cosa succede al BCR dopo l’incontro con il suo antigene. Nei loro modelli ingegnerizzati, sia i trigger basati su anticorpi sia l’ovalbumina causavano la scomparsa del recettore dalla superficie cellulare in pochi minuti, confermando una rapida internalizzazione. Questo avveniva non solo quando l’antigene galleggiava all’esterno della cellula, ma anche quando era artificialmente esposto sulla membrana della stessa cellula, imitando alcune situazioni tumorali reali. Bloccare questo traffico verso l’interno geneticamente, usando una forma dominante‑negativa di una proteina chiamata dynamin‑2 essenziale per l’endocitosi mediata da clatrina, manteneva il BCR in superficie, riduceva gli aggregati interni BCR–TLR9–NFκB, diminuiva i geni bersaglio di NFκB e rallentava la crescita cellulare. È interessante che, quando l’endocitosi era bloccata, alcuni segnali “di fondo” del BCR in superficie aumentassero, suggerendo che le cellule tumorali possano cercare di compensare attivando una modalità di segnalazione tonica più debole.
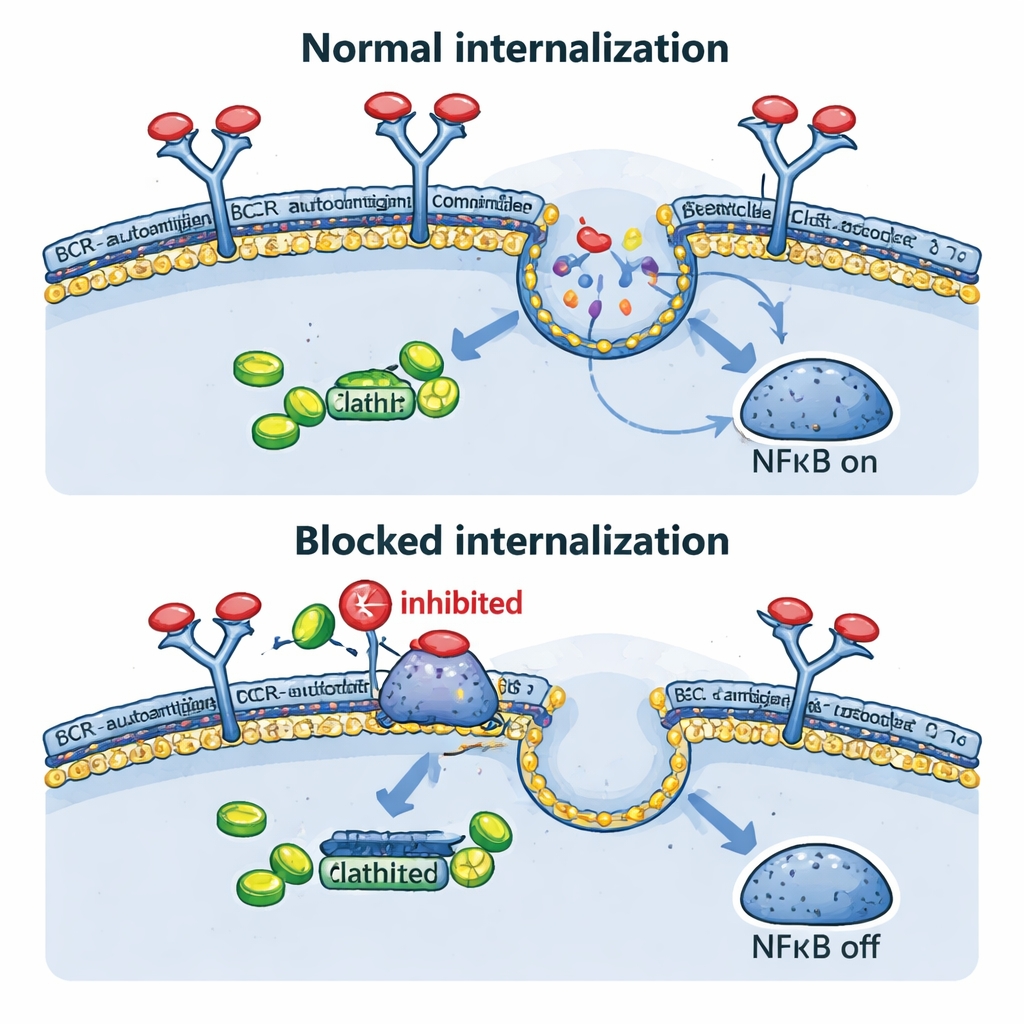
Vecchi farmaci, nuovi trucchi
Poiché sviluppare nuovi farmaci è lento e costoso, gli autori si sono chiesti se i medicinali esistenti che bloccano l’endocitosi potessero mimare gli esperimenti genetici. Le fenotiazine, una famiglia di farmaci antipsicotici e antiemetici, sono note per inibire dynamin‑2 e l’assorbimento clatrina‑dipendente dei recettori. Nelle cellule di linfoma, composti come proclorperazina e clorpromazina aumentavano i livelli di BCR in superficie e riducevano fortemente l’internalizzazione indotta dall’antigene. Questo portava a una ridotta attività genica guidata da NFκB e a una ridotta vitalità delle cellule DLBCL di tipo ABC, in particolare di quelle con componenti BCR intatti. In topi portatori di innesti di linfoma umano, la proclorperazina a dosi raggiungibili clinicamente rallentava significativamente la crescita tumorale. Inoltre, la combinazione di fenotiazine con farmaci che bloccano altri enzimi collegati al BCR, come SYK e PI3Kδ, produceva effetti antitumorali più forti rispetto a ciascun trattamento da solo.
Cosa potrebbe significare per la terapia
Complessivamente, lo studio mostra che per un sottogruppo sostanziale di DLBCL i segnali che guidano il tumore non provengono semplicemente dai recettori sulla superficie cellulare; dipendono in modo critico dall’internalizzazione del complesso BCR–antigene attraverso una specifica via di endocitosi. Interrompere questo passaggio—sia con stratagemmi genetici sia con farmaci fenotiazine—indebolisce la segnalazione NFκB e compromette la sopravvivenza delle cellule tumorali, potenzialmente rendendole più sensibili agli inibitori già esistenti della via BCR. Poiché le fenotiazine hanno già profili di dosaggio e sicurezza ben noti come antiemetici, questo lavoro fornisce un progetto realistico per studi clinici che le testino, da sole o in combinazione, in pazienti i cui linfomi mostrano attività BCR dipendente da autoantigene.
Citazione: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Parole chiave: linfoma diffuso a grandi cellule B, recettore delle cellule B, <keyword>fenotiazine, segnalazione NFkB