Clear Sky Science · it
Analisi multi‑omica temporale dell’esposizione a paclitaxel in neuroni sensoriali umani derivati da iPSC rivela i meccanismi della neuropatia periferica indotta dalla chemioterapia
Perché alcuni farmaci antitumorali danneggiano i nervi
La chemioterapia ha aiutato milioni di persone a sopravvivere al cancro, ma molti pazienti pagano un prezzo nascosto: mesi o anni di dolore bruciante, formicolio e intorpidimento alle mani e ai piedi. Questo studio pone una domanda semplice ma importante: che cosa fa esattamente il diffuso farmaco antitumorale paclitaxel alle cellule nervose sensoriali umane, e capire questi cambiamenti può indicare strade migliori per prevenire e trattare questo danno nervoso?
Dalle cellule dei pazienti ai neuroni sensoriali coltivati in laboratorio
Invece di affidarsi a esperimenti sugli animali, i ricercatori hanno iniziato con cellule di cinque donatori umani, inclusi pazienti con carcinoma mammario che avevano ricevuto paclitaxel. Hanno riprogrammato queste cellule in cellule staminali pluripotenti indotte e poi le hanno indirizzate a diventare neuroni sensoriali — lo stesso tipo di cellula nervosa che trasmette segnali tattili e dolorifici dalla pelle al midollo spinale. Questi neuroni coltivati in laboratorio hanno formato fibre lunghe e delicate e hanno mostrato attività elettrica molto simile ai nervi sensoriali reali del corpo. Il gruppo li ha quindi esposti a dosi crescenti di paclitaxel, imitando i livelli di farmaco osservati nei pazienti, e ha monitorato la salute cellulare per diversi giorni. A basse concentrazioni i neuroni se la cavavano bene, ma a una dose clinicamente rilevante (100 nM) la loro sopravvivenza ha iniziato a diminuire dopo circa due giorni, segnando l’inizio del danno tossico ai nervi.
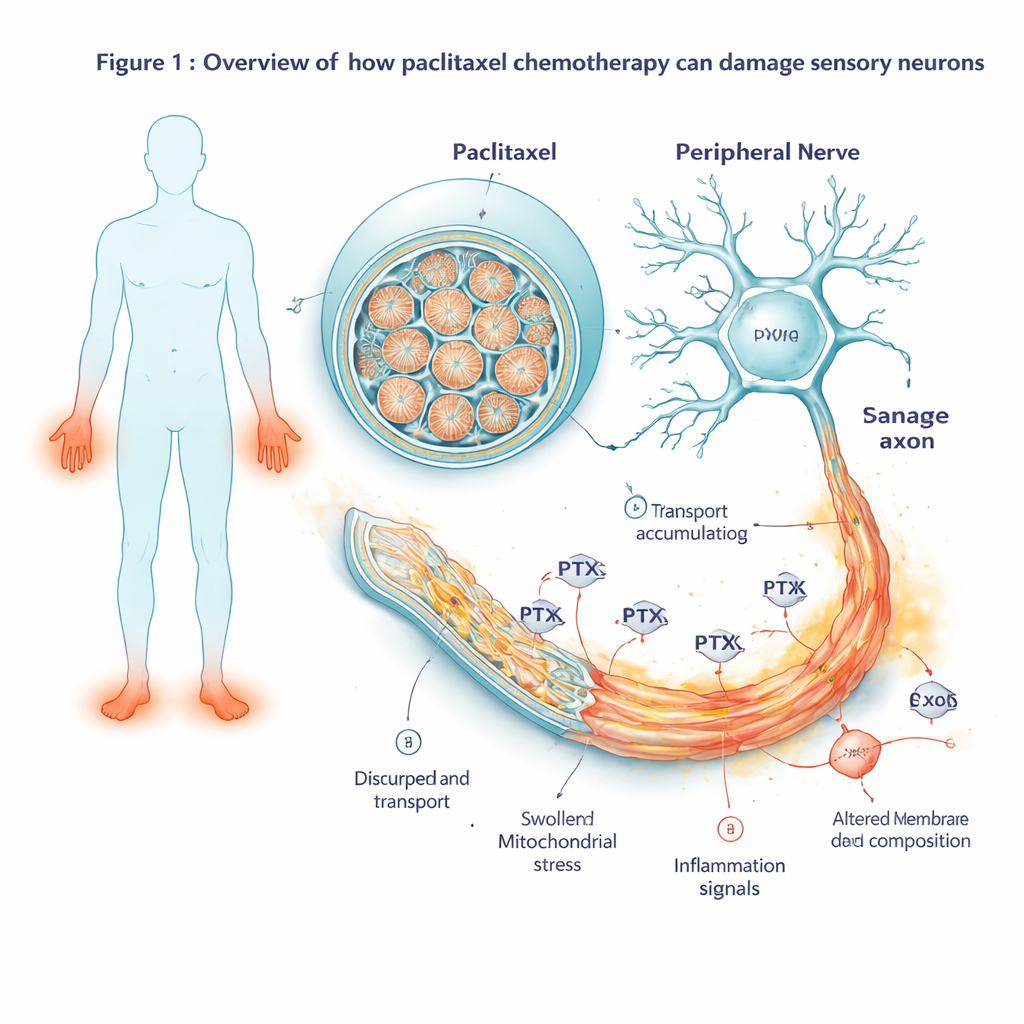
Osservare come cambia l’attività genica nel tempo
Per vedere come le cellule rispondevano prima di deteriorarsi visibilmente, gli scienziati hanno misurato quali geni si attivavano o si spegnevano in più punti temporali, da due ore dopo l’esposizione al farmaco fino a diversi giorni dopo il lavaggio del farmaco. All’inizio hanno osservato l’attivazione di un classico programma di stress cellulare centrato su un gene chiamato JUN. Con il proseguire dell’esposizione, questo segnale di stress si è ampliato in una vera e propria cascata autodistruttiva: i geni che spingono le cellule verso la morte programmata sono risultati fortemente attivati, mentre i partner protettivi sono stati sovrastati. Allo stesso tempo, i geni legati all’infiammazione e alla trasmissione del dolore sono diventati più attivi. I neuroni hanno iniziato a produrre più messaggeri infiammatori, peptidi correlati al dolore e recettori che rendono le cellule più sensibili agli stimoli nocivi, cambiamenti che rispecchiano quanto osservato nei disturbi nervosi dolorosi.
Uno sguardo approfondito a proteine e lipidi nei neuroni
Poiché i geni sono solo progetti, il gruppo ha esaminato anche le proteine effettivamente presenti nei neuroni, così come la loro composizione lipidica (dei grassi). Dopo 48 ore di esposizione al paclitaxel, molti degli stessi segnali di stress e infiammatori rilevati a livello di RNA sono comparsi anche come proteine aumentate, confermando che i neuroni stavano eseguendo questi programmi dannosi. In modo sorprendente, le proteine necessarie per il trasporto assonale — i motori molecolari e gli impalcati che spostano il carico lungo le lunghe fibre nervose — sono risultate fortemente ridotte. Ciò includeva chinesine e proteine regolatorie che mantengono stabili le scie microtubulari. A livello lipidico, i neuroni hanno mostrato una diminuzione di blocchi costitutivi chiave per il colesterolo e i lipidi di membrana, insieme a un aumento dei grassi immagazzinati chiamati triacilgliceroli. Insieme, questi cambiamenti suggeriscono che il paclitaxel non solo attiva vie di morte cellulare ma indebolisce anche la struttura fisica e l’equilibrio energetico delle fibre nervose.
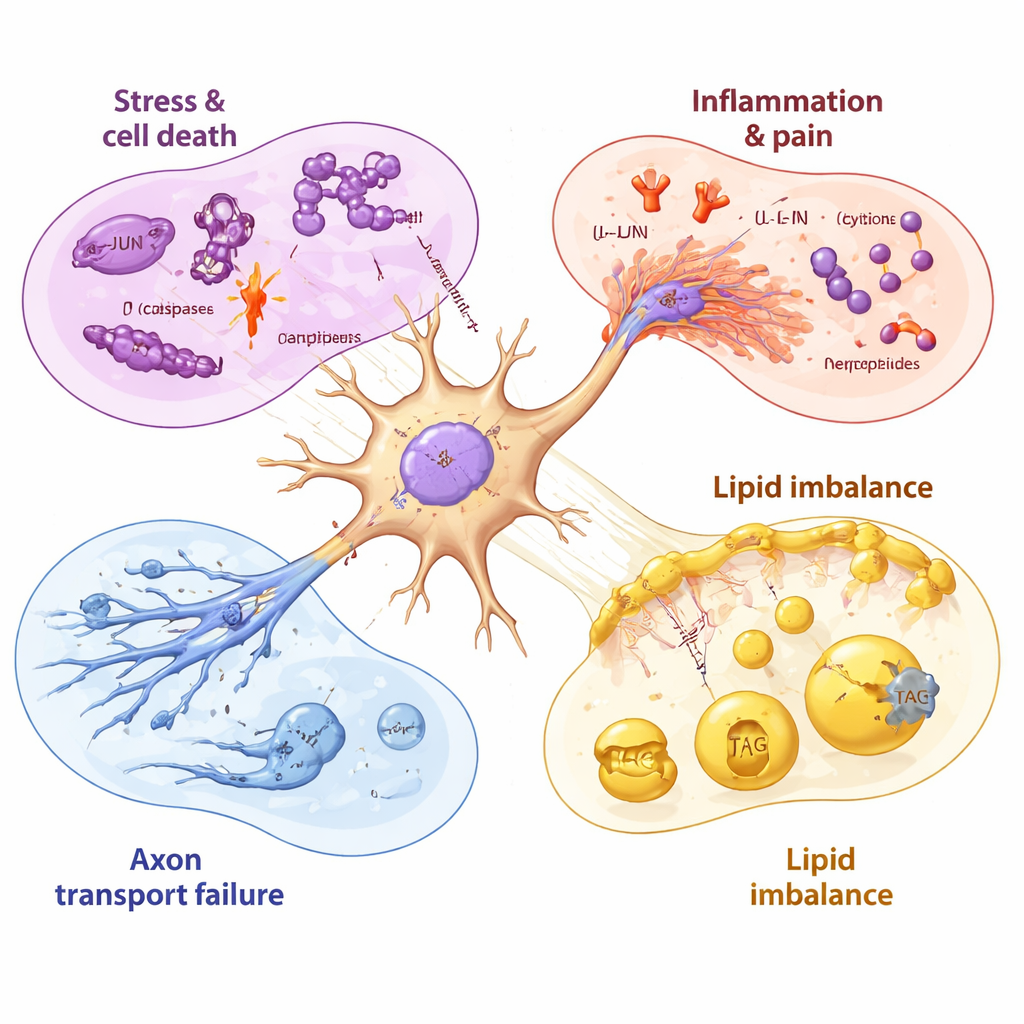
Una cronologia del danno nervoso e di un recupero incompleto
Campionando i neuroni prima, durante e dopo l’esposizione al farmaco, i ricercatori hanno potuto ordinare questi eventi nel tempo. I geni mitocondriali (relativi all’energia) sono stati perturbati nell’arco di poche ore, seguiti dal gene di stress JUN, quindi da un’attivazione più marcata dei programmi di morte cellulare e infiammatori mentre la vitalità iniziava a calare. Anche dopo la rimozione del paclitaxel, molti segnali nocivi sono rimasti elevati per giorni, mentre i geni necessari per produrre lipidi di membrana sani hanno continuato a diminuire. Alcune molecole che aumentano più tardivamente, come una pompa di efflusso farmacologico in grado di espellere il paclitaxel e certi fattori di crescita, suggerivano che i neuroni stavano tentando di proteggersi e ripararsi — ma queste risposte sono apparse relativamente lente e incomplete rispetto alla spinta rapida ed iniziale verso il danno.
Cosa significa per i pazienti che convivono con il dolore nervoso
Per un lettore non specialistico, il messaggio è che il paclitaxel danneggia i nervi sensoriali attraverso una serie coordinata di colpi: stressa i loro sistemi energetici, attiva interruttori genetici verso la morte cellulare, scatena infiammazione e segnali del dolore, interrompe le “autostrade” di trasporto interne alle fibre nervose e altera i grassi che mantengono stabili le membrane nervose. Mappando questi cambiamenti in neuroni di origine umana con grande dettaglio, lo studio evidenzia bersagli concreti e farmacologicamente indirizzabili — come specifici regolatori dello stress, recettori infiammatori ed enzimi per la sintesi lipidica — che potrebbero essere bloccati o sostenuti per proteggere i nervi senza indebolire il trattamento del cancro. Sebbene nuove terapie richiederanno ulteriori studi, questo lavoro offre una mappa più chiara per prevenire o attenuare il danno nervoso indotto dalla chemioterapia, migliorando la qualità della vita dei sopravvissuti al cancro.
Citazione: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Parole chiave: neuropatia periferica indotta da chemioterapia, paclitaxel, neuroni sensoriali, neuroinfiammazione, degenerazione assonale