Clear Sky Science · it
La metilazione reversibile dell’arginina regola l’attività mitocondriale di IDH2: controllo coordinato da CARM1 e KDM3A/4A
Affinare le centrali energetiche della cellula
I mitocondri, spesso definiti le centrali energetiche delle nostre cellule, fanno molto più che produrre energia. Regolano costantemente il modo in cui consumano carburante per soddisfare le esigenze dell’organismo e, quando questo sistema si guasta, può contribuire a malattie come il diabete, l’insufficienza cardiaca e il cancro. Questo studio svela un “dimmer” nascosto all’interno dei mitocondri: un minuscolo segnale chimico su un singolo mattoncino di un enzima chiave, IDH2, che aiuta a decidere se i mitocondri restano in modalità bassa o aumentano la loro produzione energetica.
Un piccolo segno con grandi conseguenze
Le proteine nelle nostre cellule non sono statiche; vengono spesso modificate con piccoli gruppi chimici che ne alterano il comportamento. Sebbene molte di queste modifiche nel nucleo e nel citoplasma siano ben note, quelle all’interno dei mitocondri sono meno esplorate. Gli autori si sono concentrati su un tipo particolare di segnale chiamato metilazione dell’arginina e hanno chiesto se potesse controllare l’attività degli enzimi mitocondriali. Hanno individuato l’enzima IDH2, un protagonista del ciclo degli acidi tricarbossilici (TCA), che aiuta a trasformare i nutrienti in energia e in blocchi metabolici essenziali. Con strumenti biochimici e spettrometria di massa hanno scoperto che IDH2 porta un marchio metilico specifico su un amminoacido, l’arginina 188, e che questo marchio è aggiunto da un enzima chiamato CARM1 che, in modo sorprendente, agisce anche all’interno dei mitocondri.
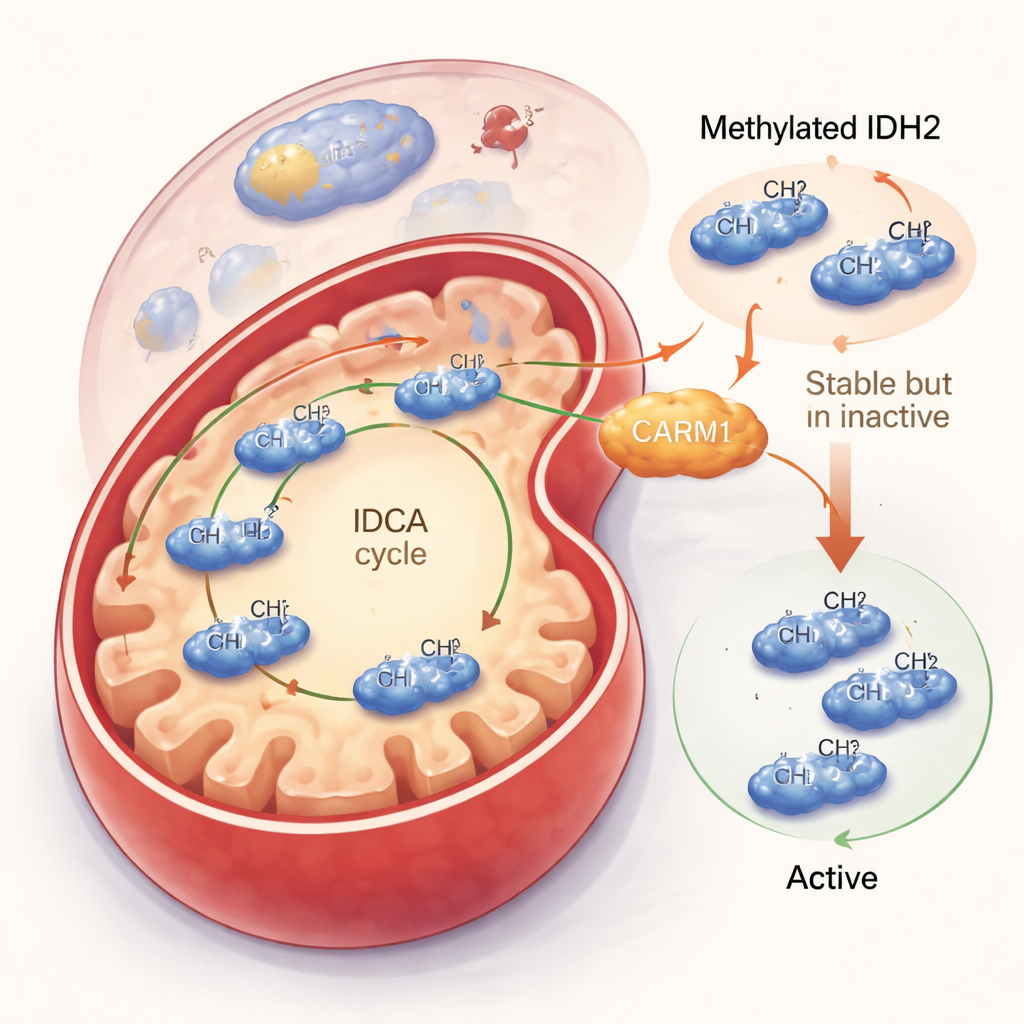
Ridurre l’attività di IDH2 ma aumentarne la durata
Il team ha quindi indagato cosa faccia realmente questo segno metilico. Quando CARM1 era attivo e in grado di metilare IDH2, la proteina IDH2 diventava più stabile e restava più a lungo nella cellula. Ma questo apparente vantaggio comportava un compromesso: l’IDH2 metilato risultava meno attivo. In esperimenti su cellule e su proteina purificata, l’IDH2 metilato produceva meno del suo prodotto principale, l’alfa-chetoglutarato, e generava meno della molecola protettiva NADPH. Al contrario, una versione di IDH2 che non poteva essere metilata sull’arginina 188 formava maggiormente il dimero attivo, funzionava più velocemente e aumentava sia i livelli di alfa-chetoglutarato sia di NADPH. Anche se la quantità complessiva di questa forma non metilata era minore, ogni singola molecola lavorava di più, portando a un incremento netto dell’attività mitocondriale.
Un interruttore reversibile con due ‘cancellatori’
Elemento cruciale, questo marchio metilico non è permanente. I ricercatori hanno mostrato che due enzimi noti per rimuovere un diverso tipo di segnale, le demetilasi della lisina KDM3A e KDM4A, possono anche cancellare il marchio di metilazione sull’arginina di IDH2. Quando queste demetilasi erano presenti, l’arginina metilata alla posizione 188 perdeva i gruppi chimici aggiunti, IDH2 diventava meno stabile ma più attivo, e la sua forma dimero aumentava. Cellule con KDM3A o KDM4A più attive mostravano un potenziale di membrana mitocondriale più elevato e consumavano più ossigeno, segni che i loro mitocondri funzionavano a maggior rendimento ossidativo. Quando questi enzimi venivano ridotti, accadeva l’opposto: l’attività di IDH2 calava e le prestazioni mitocondriali diminuivano, a sottolineare che si tratta di un sistema di controllo reversibile e non di un cambiamento monodirezionale.
Collegare metabolismo e malattia
Poiché IDH2 è stato associato al cancro e ad altri disturbi, gli autori hanno esaminato come questo interruttore di metilazione possa influire in contesti simili alla malattia. In diverse linee cellulari normali e tumorali, hanno osservato che livelli proteici più elevati di IDH2 spesso correvano di pari passo con maggiore metilazione e sorprendentemente con minore attività enzimatica, suggerendo che “più proteina” non significa necessariamente “più funzione”. Nei set di dati sul cancro al seno, i pazienti con livelli proteici più alti di IDH2 tendevano ad avere una sopravvivenza peggiore, anche se l’espressione genica di IDH2 non era correlata all’esito. I risultati sostengono un modello in cui la metilazione guidata da CARM1 rallenta il ciclo TCA e spinge le cellule verso modalità alternative di utilizzo dei nutrienti favorevoli al cancro, mentre demetilasi come KDM3A e KDM4A possono riportare le cellule verso una produzione energetica più efficiente.
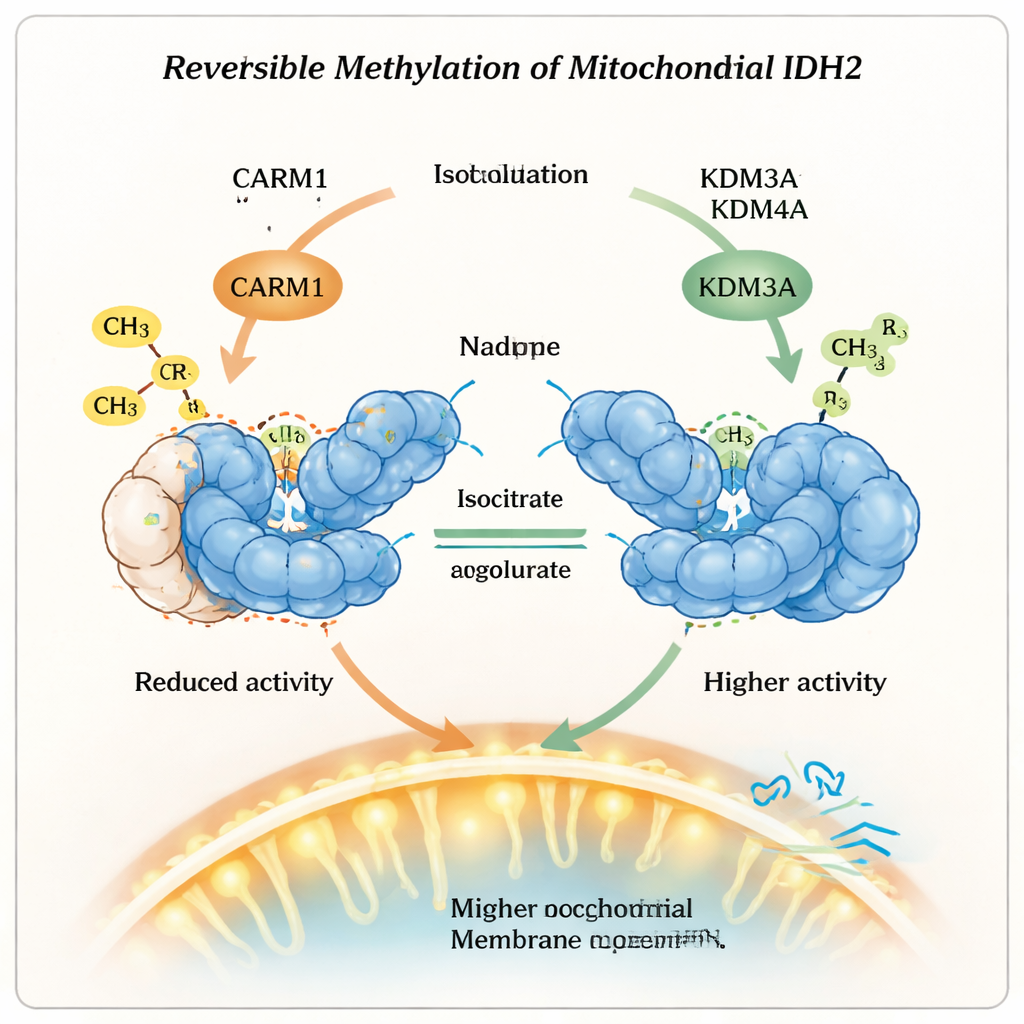
Cosa significa per salute e terapia
In termini pratici, questo lavoro mostra che i mitocondri non si limitano a spegnere o accendere gli enzimi, ma usano segnali chimici reversibili come manopole finemente regolate. Aggiungendo un gruppo metile, CARM1 trasforma IDH2 in una forma più longeva ma meno attiva; rimuovendo quel segno, KDM3A e KDM4A sacrificano parte della stabilità per guadagnare maggiore potenza. Questo equilibrio influenza la scelta cellulare tra una combustione rapida ma inefficiente degli zuccheri e una produzione energetica più lenta e più efficiente. Comprendere questo “dimmer” di metilazione su IDH2 apre nuove possibilità terapeutiche per correggere il metabolismo mitocondriale difettoso in condizioni come il cancro e le malattie metaboliche, mirando agli enzimi che scrivono e cancellano questi piccoli ma potenti segni chimici.
Citazione: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Parole chiave: mitocondri, IDH2, metilazione dell’arginina, metabolismo cellulare, CARM1