Clear Sky Science · it
Un circuito infiammatorio MIF-p38-GSDMD nei cheratinociti alla base del lupus cutaneo indotto da UVB
Perché la luce solare può essere un problema serio nel lupus
Per la maggior parte delle persone il sole provoca semplicemente un’abbronzatura o, nella peggiore delle ipotesi, una scottatura. Ma per molti pazienti con lupus anche pochi minuti di luce ultravioletta B (UVB) possono scatenare eruzioni dolorose e durature e persino peggiorare l’intera malattia. Questo studio scopre un nascosto “circuito di retroazione” all’interno delle cellule cutanee che aiuta a spiegare la forte sensibilità della pelle alla luce — e indica nuovi trattamenti molto locali che potrebbero attenuare la reazione senza sopprimere l’intero sistema immunitario.
Le cellule della pelle come colpevoli inattesi
I medici sapevano da tempo che il lupus eritematoso cutaneo (CLE) comporta infiammazione cronica e cicatrizzazione della pelle, ma l’attenzione si concentrava spesso sulle cellule immunitarie infiltranti. Usando il sequenziamento dell’RNA a singola cellula, gli autori hanno invece osservato più da vicino le cellule costitutive della pelle — i cheratinociti nello strato esterno e i fibroblasti sottostanti. Hanno scoperto che nei pazienti con lupus alcuni sottogruppi di cheratinociti sono ampliati e mostrano una marcata “firma interferonica”, un pattern di geni di allarme antivirale permanentemente attivato. All’interno di questi cheratinociti anomali è emerso un messaggero proteico: il fattore inibitore della migrazione dei macrofagi, o MIF, prodotto a livelli molto più alti rispetto a molecole infiammatorie più note come TNF o IL‑6.
Un messaggero nascosto rilasciato dalla luce solare
Rilevare alte quantità di MIF all’interno dei cheratinociti non spiegava ancora perché la luce solare fosse così pericolosa. Quando il team ha esposto cheratinociti coltivati a luce UVB, ha scoperto che la quantità totale di MIF nelle cellule cambiava di poco — ma la proteina veniva rilasciata nel fluido circostante in modo dipendente dalla dose. Più UVB veniva somministrata, più MIF fuoriusciva, in stretta correlazione con un marcatore di danno alla membrana. Quando questo fluido ricco di MIF è stato applicato a cheratinociti e fibroblasti freschi, ha indotto cambiamenti tipici del CLE: un aumento di citochine infiammatorie ed enzimi che degradano e rimodellano la matrice di sostegno della pelle. Silenziare MIF con strumenti genetici o bloccarlo con un farmaco a piccola molecola ha ridotto nettamente queste reazioni dannose, dimostrando che il MIF derivato dai cheratinociti non è solo uno spettatore ma un amplificatore chiave del danno indotto da UVB. 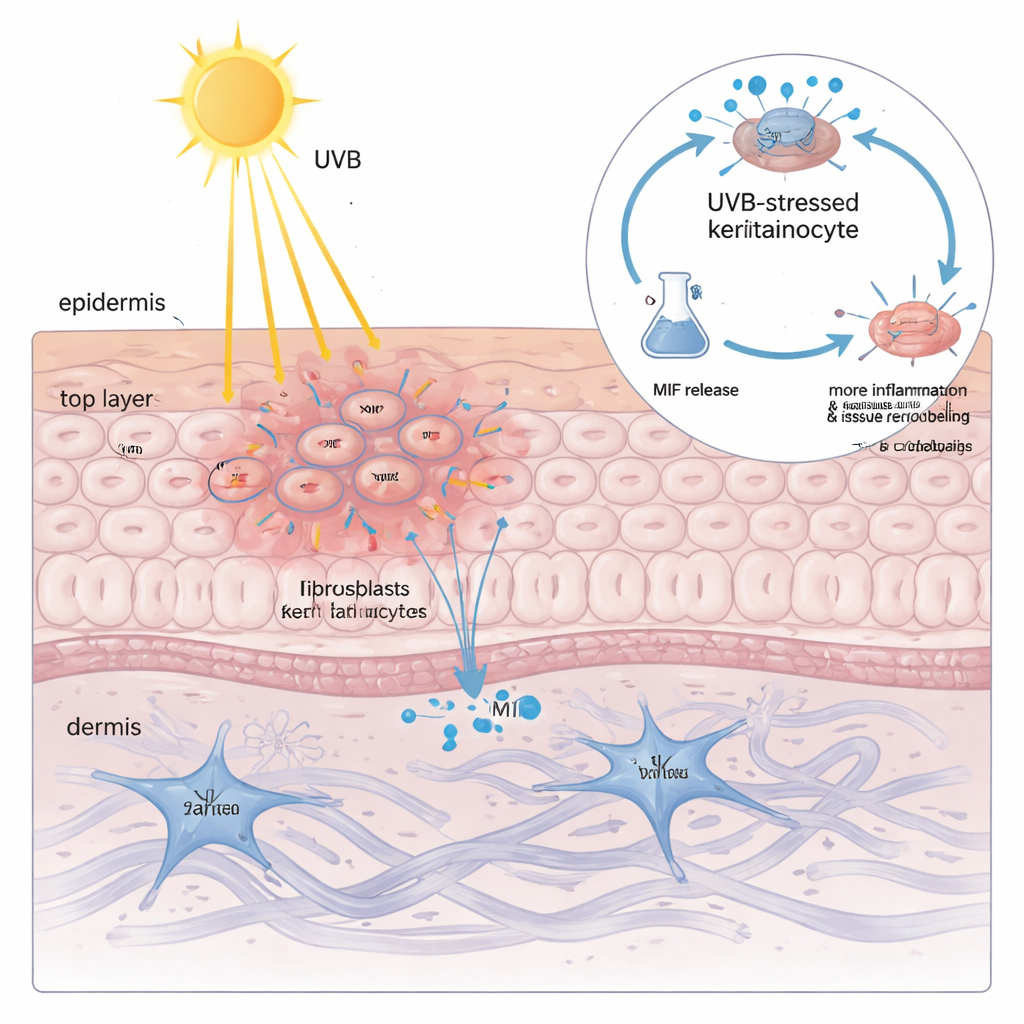
Un circuito infiammatorio autosostenuto all’interno dei cheratinociti
Per capire come gli UVB inducano i cheratinociti a rilasciare MIF, i ricercatori hanno costruito un modello di cheratinociti “simile al lupus” caricando le cellule con il loro DNA e RNA, emulando i detriti genetici mal gestiti osservati nel lupus. In questo stato primed, gli UVB hanno attivato una cosiddetta risposta da stress ribotossico: un segnale di danno dai ribosomi che ha attivato una chinasi chiamata ZAKα e, a sua volta, l’enzima di stress p38. Questa via ha aumentato un’altra proteina, il fattore di trascrizione C/EBPβ, che si è legata alla regione di controllo del gene NLRP3 e ne ha aumentato l’espressione. NLRP3 ha quindi promosso la scissione di GSDMD, una proteina che forma pori e apre buchi nella membrana cellulare causando una forma infiammatoria di morte cellulare nota come piroptosi. È fondamentale che il MIF sia fuoriuscito principalmente attraverso questi pori formati da GSDMD — non tramite le normali vescicole secretorie. Una volta all’esterno, il MIF si è legato al suo recettore di superficie CD74 sui cheratinociti, riattivando p38, NLRP3 e GSDMD e chiudendo così un circolo vizioso: UVB → p38 → NLRP3 → pori GSDMD → rilascio di MIF → ulteriore attivazione di p38.
Dalla scoperta molecolare a nuovi trattamenti locali
Questo circuito non era solo una curiosità da laboratorio. In una linea murina predisposta al lupus, l’esposizione a UVB ha prodotto lesioni cutanee severe con alti livelli di MIF, attivazione di p38, NLRP3 e GSDMD clivato nell’epidermide. Quando i ricercatori hanno usato un virus per terapia genica per silenziare specificamente il gene Mif nella pelle, le eruzioni indotte da UVB sono risultate molto più lievi e i marcatori di infiammazione e rimodellamento tissutale sono diminuiti sia nei cheratinociti sia nei fibroblasti. Per evitare effetti collaterali sistemici dei farmaci, hanno anche ingegnerizzato cerotti con microaghi solubili caricati con l’inibitore di MIF ISO‑1. Premuti brevemente sulla pelle, questi minuscoli aghi hanno somministrato il farmaco senza dolore negli strati superiori. I topi predisposti al lupus trattati con questi microaghi hanno sviluppato molte meno lesioni e di minore gravità dopo UVB, e la firma molecolare del circuito MIF‑p38‑GSDMD è risultata notevolmente attenuata. 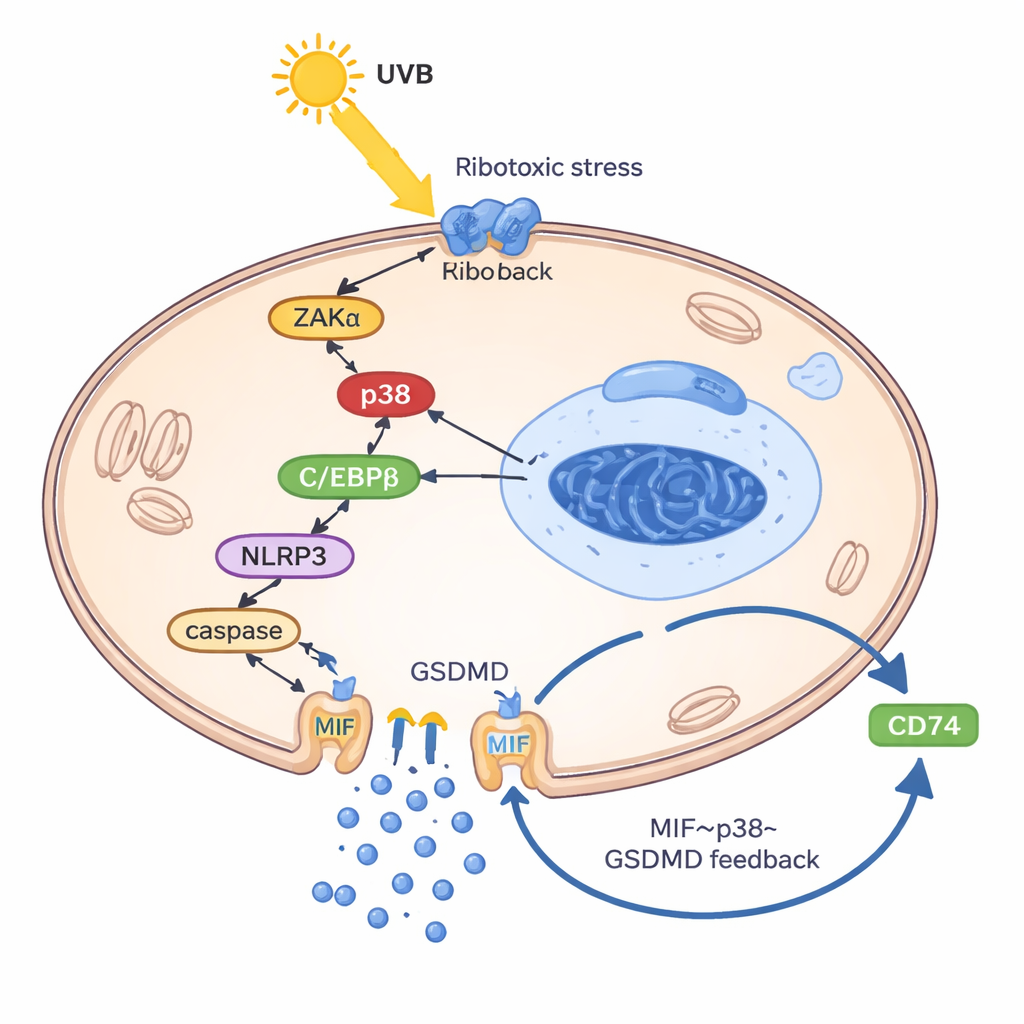
Cosa significa per le persone con lupus
In termini semplici, questo lavoro mostra che nel lupus alcune cellule cutanee sono programmate per reagire eccessivamente agli UVB rilasciando una potente molecola “amplificatrice”, il MIF, attraverso pori nella membrana autoinflitti. Questo impulso poi ricompatta il circuito infiammatorio, mantenendolo attivo anche dopo la cessazione dell’esposizione luminosa iniziale. Mappando questo circuito passo dopo passo, lo studio suggerisce che bloccare il MIF direttamente nella pelle — mediante silenziamento genico o sistemi di somministrazione intelligenti come i cerotti con microaghi — potrebbe interrompere il ciclo delle riacutizzazioni fotosensibili senza spegnere in modo diffuso il sistema immunitario. Se strategie simili si dimostrassero sicure ed efficaci negli esseri umani, potrebbero offrire alle persone con lupus nuovi modi per convivere più serenamente con la luce.
Citazione: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Parole chiave: lupus cutaneo, fotosensibilità, cheratinociti, circuito infiammatorio, terapia con microaghi