Clear Sky Science · it
Polmonite correlata a inibitori del checkpoint immunitario: progressi attuali e il possibile ruolo della terapia con cellule staminali mesenchimali
Quando il trattamento del cancro si ritorce contro i polmoni
I farmaci che liberano il sistema immunitario contro il cancro hanno trasformato la cura di malattie come il cancro polmonare e il melanoma. Ma questo nuovo potere ha un prezzo: in alcuni pazienti lo stesso attacco immunitario che colpisce i tumori può rivolgersi contro i polmoni, causando una condizione chiamata polmonite correlata agli inibitori del checkpoint immunitario (ICIP). Questa rassegna spiega cos'è l'ICIP, perché si manifesta, come viene trattata oggi e perché un tipo speciale di cellule staminali — le cellule staminali mesenchimali (MSC) — potrebbe un giorno offrire un modo più sicuro e mirato per calmare la tempesta senza compromettere il controllo del tumore. 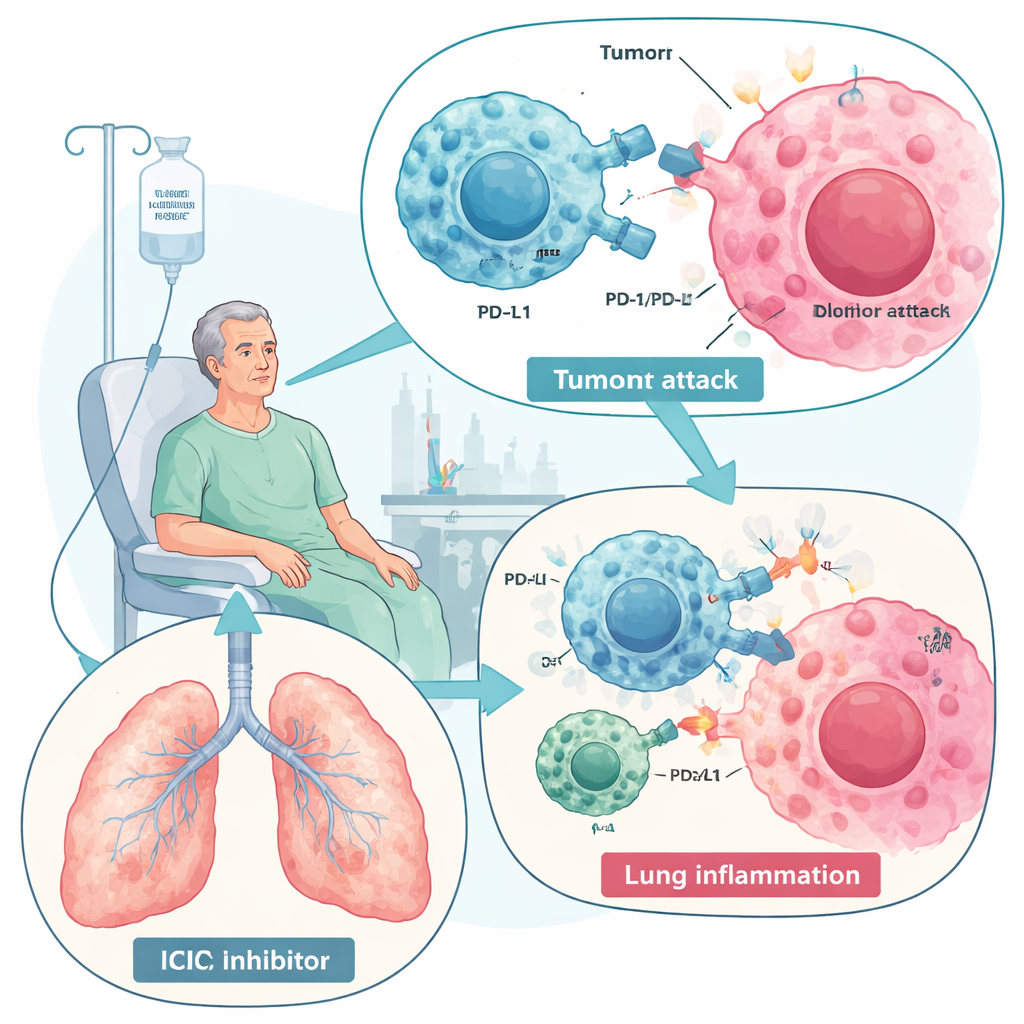
Potenti farmaci antitumorali con un rischio nascosto per i polmoni
Gli inibitori del checkpoint immunitario, in particolare quelli che bloccano PD-1 e PD-L1, agiscono rimuovendo i "freni" molecolari che normalmente tengono sotto controllo le risposte immunitarie. Con i freni tolti, le cellule T possono riconoscere e distruggere meglio le cellule tumorali, migliorando la sopravvivenza in molti tipi di tumore. Ma questo potenziamento può infrangere la tolleranza normale e scatenare effetti avversi immunomediati in diversi organi. L'ICIP è la complicanza polmonare più grave associata a questi farmaci ed è una delle principali cause di morte correlate a reazioni immunitarie da trattamento. Colpisce da una piccola percentuale fino a quasi un terzo dei pazienti in alcuni studi real-world, particolarmente quelli con tumore polmonare o malattie polmonari preesistenti come BPCO o malattia polmonare interstiziale. I sintomi variano da tosse lieve e respiro corto fino a insufficienza respiratoria potenzialmente letale.
Come il sistema immunitario danneggia il polmone
La rassegna descrive l'ICIP come il risultato di un equilibrio immunitario alterato all'interno dei polmoni. Cellule "combattenti" iperattive — cellule T CD8, alcuni linfociti T helper, macrofagi infiammatori, neutrofili e cellule natural killer — invadono il tessuto polmonare e rilasciano proteine segnalatrici aggressive, tra cui interferone-gamma, TNF-alpha e interleuchine come IL-6 e IL-17. Allo stesso tempo, le cellule normalmente protettive che attenuano l'infiammazione, come le cellule T regolatorie e i macrofagi orientati alla riparazione, risultano ridotte. Alcuni pazienti mostrano anche un aumento di anticorpi autoreattivi prima o durante il trattamento, suggerendo che l'ICIP possa in parte somigliare a una malattia autoimmune. Nel liquido di lavaggio bronco‑alveolare i medici riscontrano un quadro infiammatorio ricco di cellule T e un mix di citochine distinto da quello dell'infezione o della progressione tumorale, elemento che può aiutare nella diagnosi.
Rilevare, classificare e trattare il danno
Alle TC, l'ICIP si presenta più spesso come aree sfumate in "vetro smerigliato" o consolidazioni a chiazze sparse in entrambi i polmoni, pattern che differiscono dal danno da radioterapia, il quale resta confinato al campo irradiato. La diagnosi di ICIP si basa sulla combinazione dei reperti radiologici, dei sintomi e sull'esclusione accurata di infezioni e altre cause. Le linee guida internazionali classificano quindi la gravità da 1 (lieve, spesso solo radiologico) a 4 (insufficienza respiratoria pericolosa per la vita). Il trattamento principale oggi è costituito dai glucocorticoidi — steroidi anti-infiammatori potenti — talvolta combinati con altri farmaci immunomodulatori come tocilizumab (che blocca IL-6) o infliximab (che blocca TNF-alpha) nei casi gravi o resistenti agli steroidi. Questi approcci possono salvare la vita, ma sono strumenti imprecisi: gli steroidi hanno molti effetti collaterali, alcuni pazienti non rispondono e la soppressione immunitaria generalizzata può indebolire la risposta antitumorale che questi farmaci volevano potenziare.
Perché le cellule staminali entrano in gioco
Le cellule staminali mesenchimali, che possono essere prelevate dal midollo osseo, dal tessuto adiposo o dalla corda ombelicale, sono emerse come promettenti "modulatrici immunitarie" più che come semplici costruttrici di tessuto. Quando infuse in circolo, molte di queste cellule rimangono temporaneamente intrappolate nei piccoli vasi polmonari — il cosiddetto effetto di primo passaggio — che è uno svantaggio per trattare organi lontani ma un potenziale vantaggio per le malattie polmonari. In modelli animali e in trial umani precoci per condizioni come polmonite grave, sindrome da distress respiratorio acuto, malattia infiammatoria intestinale e malattia da trapianto contro l'ospite, le MSC attenuano risposte immunitarie iperattive, spostano le cellule immunitarie verso uno stato più equilibrato e secernono fattori di crescita che favoriscono la riparazione tissutale limitando la fibrosi. È importante che i loro benefici spesso derivino non dal trasformarsi direttamente in cellule polmonari, ma dalla miscela di molecole segnalatrici e piccole vescicole che rilasciano. 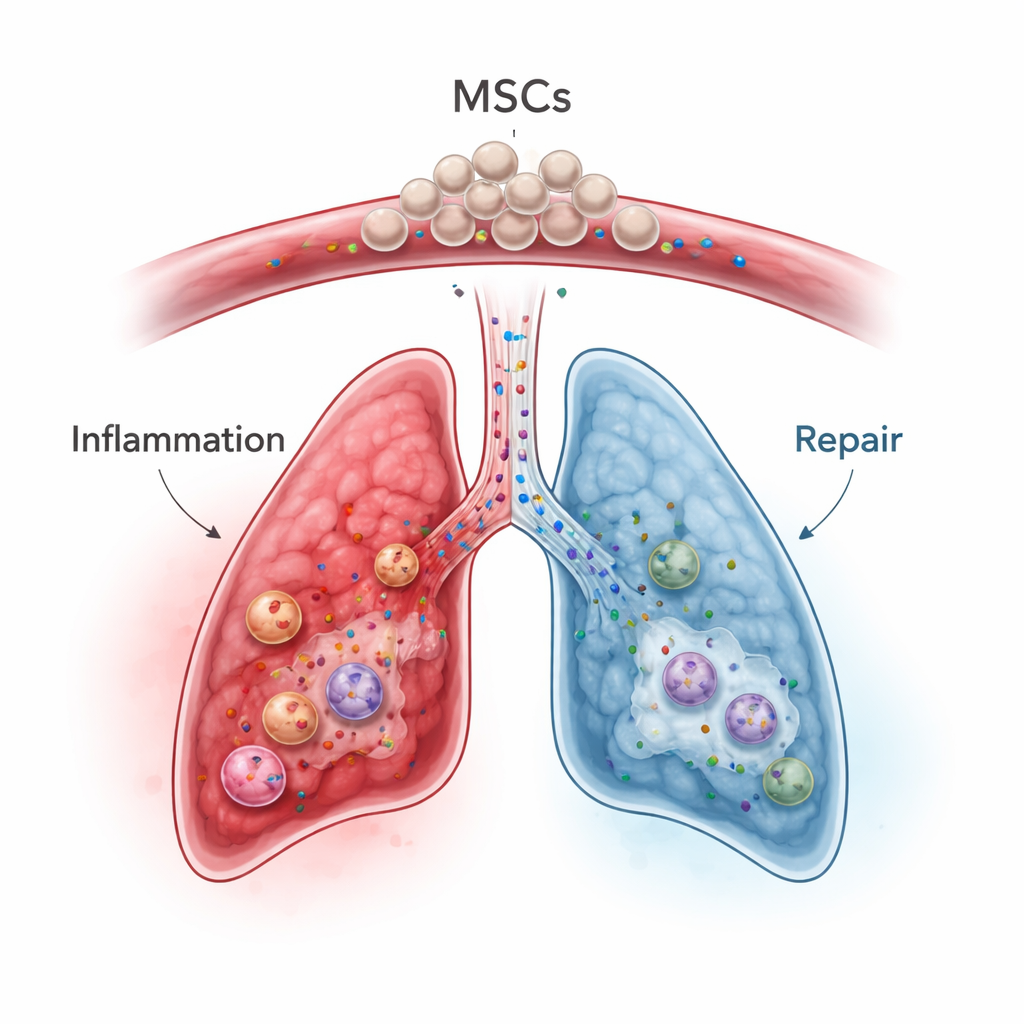
Come le MSC potrebbero placare l'ICIP senza compromettere la cura
Nel contesto dell'ICIP, le MSC potrebbero, in teoria, affrontare vari problemi contemporaneamente. Possono frenare direttamente le cellule T attivate, promuovere la crescita e la funzione delle cellule T regolatorie e spingere i macrofagi lontano da uno stato aggressivo e lesivo verso uno orientato alla guarigione. Abbassano anche messaggeri infiammatori chiave come IL-6, IL-1β e TNF-alpha, e aumentano fattori anti-infiammatori e proteine protettive come TSG-6 che aiutano a limitare il danno polmonare e la fibrosi. Studi preclinici suggeriscono che le MSC o esosomi derivati da MSC ingegnerizzati possono ridurre le tempeste di citochine e il danno d'organo indotti da inibitori del checkpoint o da radiazioni, preservando in alcuni contesti l'attività antitumorale meglio degli immunosoppressori standard. Tuttavia, gli autori avvertono che le MSC possono anche interagire con i tumori e con la coagulazione in modi complessi, e che i loro effetti dipendono fortemente dall'ambiente infiammatorio circostante e persino dalla fonte delle MSC (midollo osseo, tessuto adiposo o cordone ombelicale).
Prospettive: promessa con test rigorosi
Per i pazienti il cui trattamento oncologico è interrotto o minacciato da una grave tossicità polmonare, le terapie a base di MSC potrebbero infine offrire un modo più mirato per spegnere l'infiammazione, riparare il tessuto polmonare e prevenire la cicatrizzazione a lungo termine — idealmente senza annullare i benefici salvavita dell'inibizione del checkpoint immunitario. Tuttavia, non sono ancora stati completati trial specifici con MSC per l'ICIP. Gli autori sostengono che sono urgentemente necessari studi animali ben progettati e trial clinici per definire quale tipo di MSC o prodotto a base di esosomi funzioni meglio, quanto somministrare, quando somministrarlo rispetto a steroidi e immunoterapia e come monitorare rischi come la crescita tumorale o la formazione di coaguli. Fino ad allora, le MSC restano un'opzione promettente ma ancora sperimentale all'orizzonte per gestire questo grave effetto collaterale della moderna cura oncologica.
Citazione: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Parole chiave: effetti collaterali dell'immunoterapia, polmonite, inibitori del checkpoint, cellule staminali mesenchimali, infiammazione polmonare