Clear Sky Science · it
c-Myc/GRPEL1 mantiene la sintesi degli acidi grassi tramite FASN per sostenere la proliferazione delle cellule PDAC
Perché il bisogno di grassi delle cellule tumorali conta
Il cancro pancreas è uno dei tumori più letali, in parte perché le sue cellule sono esperte nel riprogrammare il proprio metabolismo per sopravvivere e crescere. Questo studio esamina una parte sorprendente di quella storia: come le cellule tumorali pancreatiche potenziano le loro “fabbriche dei grassi” interne per alimentare una crescita incessante, e come bloccare questo processo potrebbe aprire nuove opzioni terapeutiche per i pazienti.
Un cancro difficile con un vantaggio metabolico
La maggior parte dei tumori pancreatici è un tipo chiamato adenocarcinoma duttale pancreatico (PDAC), che viene solitamente rilevato in fase avanzata e risponde male alle terapie attuali. Le cellule di PDAC vivono in un ambiente ostile con poco ossigeno e nutrienti scarsi, eppure prosperano riorganizzando l’uso di zuccheri, grassi e altri combustibili. I loro mitocondri — minuscole centrali elettriche all’interno delle cellule — giocano un ruolo centrale in questa riorganizzazione. Per mantenere questi impianti in funzione, le cellule monitorano e riparano costantemente migliaia di proteine mitocondriali, un processo noto come controllo di qualità delle proteine mitocondriali. Fino ad ora non era chiaro come questo sistema di controllo di qualità si collegasse al modo in cui i tumori pancreatici si procurano nutrienti.
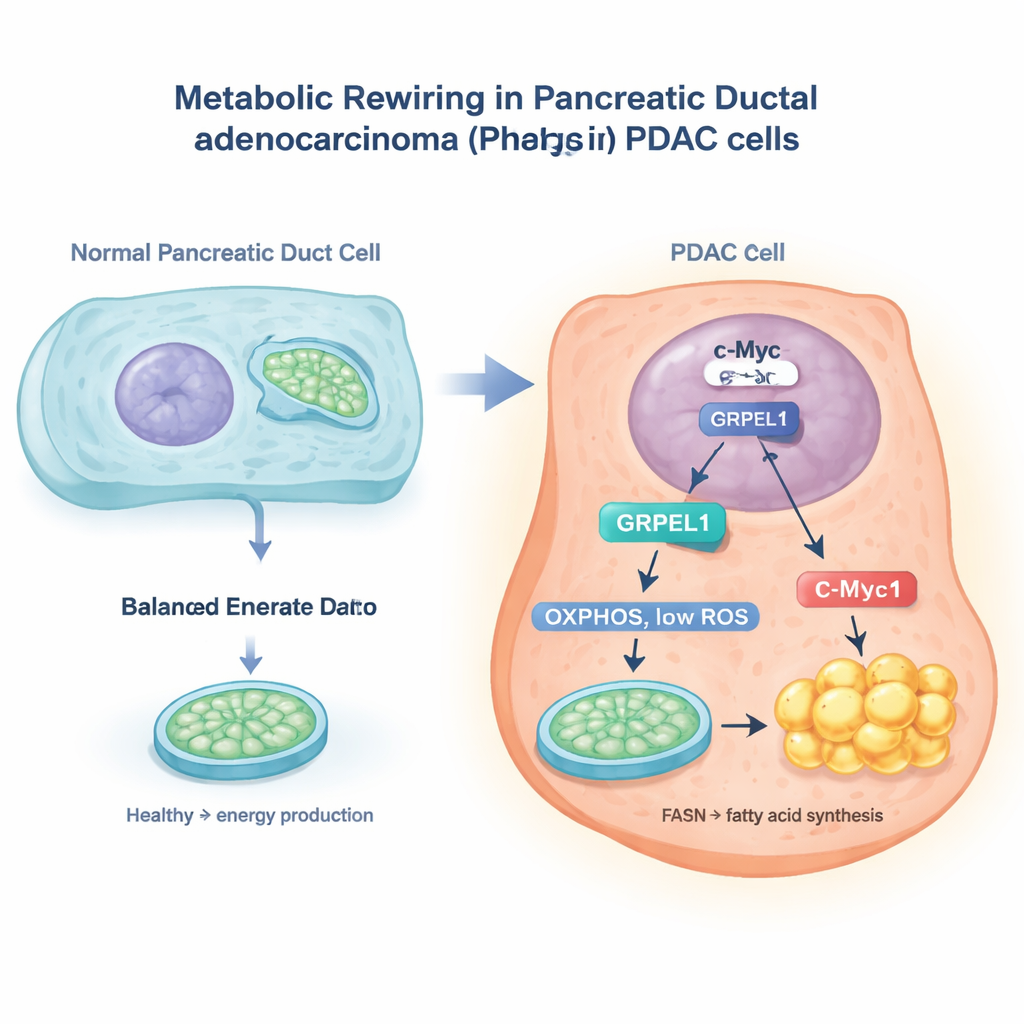
Il commutatore c-Myc e un aiuto mitocondriale
I ricercatori hanno sfruttato grandi banche dati sul cancro e esperimenti su cellule di cancro pancreatico per concentrarsi su una proteina chiamata GRPEL1, un fattore che aiuta nella gestione delle proteine mitocondriali. Hanno scoperto che un noto gene oncogene, c-Myc, funziona come un interruttore molecolare nel nucleo cellulare che attiva il gene GRPEL1. Quando i livelli di c-Myc diminuivano, anche quelli di GRPEL1 calavano; quando c-Myc veniva aumentato, GRPEL1 saliva. Nei campioni tumorali dei pazienti si osservava inoltre che c-Myc e GRPEL1 tendono ad essere espressi entrambi ad alti livelli, e questo si correlava con esiti peggiori. In colture cellulari di PDAC, ridurre GRPEL1 rallentava la divisione cellulare e la formazione di colonie, mentre un eccesso di GRPEL1 favoriva la proliferazione, soprattutto quando c-Myc era altrimenti bloccato.
Dal mitocondrio alla produzione di grassi
Approfondendo, il team ha scoperto che GRPEL1 fa più che mantenere l’omeostasi delle proteine mitocondriali. Quando GRPEL1 veniva depletato, i mitocondri nelle cellule PDAC diventavano meno efficienti nella produzione di energia, perdevano la loro morfologia normale e producevano più specie reattive dell’ossigeno (ROS) — sottoprodotti chimici reattivi talvolta chiamati “ruggine” cellulare. Questo aumento di ROS aveva un effetto a catena: riduceva i livelli di FASN (fatty acid synthase), un enzima chiave che costruisce nuovi acidi grassi all’interno delle cellule. Con FASN ridotto, le cellule sintetizzavano meno grassi, immagazzinavano meno lipidi e la loro crescita rallentava. Quando i ricercatori neutralizzavano i ROS con un antiossidante, i livelli di FASN tornavano, mostrando che il legame GRPEL1–FASN è mediato dai ROS. È interessante che c-Myc stesso non sembrasse attivare direttamente il gene FASN in questo sistema, ma lo influenzasse indirettamente attraverso GRPEL1 e lo stress mitocondriale.
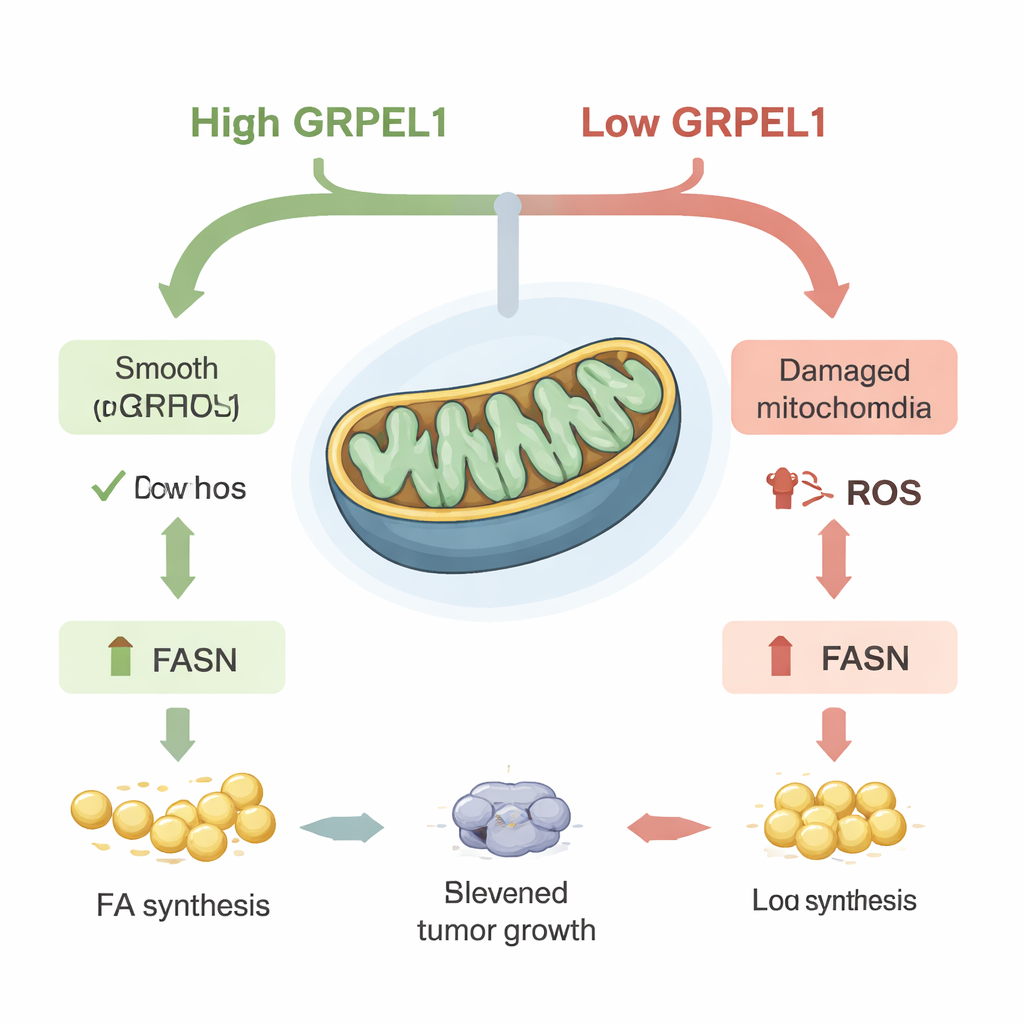
I grassi come combustibile per la crescita tumorale
Poiché FASN è al centro della costruzione dei grassi, gli scienziati hanno chiesto se ripristinarlo potesse salvare la crescita delle cellule tumorali quando GRPEL1 era basso. Nelle colture cellulari, forzare l’espressione di FASN ha in parte invertito il rallentamento della crescita e la ridotta formazione di colonie causati dalla perdita di GRPEL1. Lo stesso è avvenuto nei topi: i tumori generati da cellule deplete di GRPEL1 crescevano più lentamente, ma la reintroduzione di FASN ha ripristinato sia le dimensioni tumorali sia il contenuto lipidico. Analisi dettagliate di metaboliti e lipidi hanno mostrato ampie riduzioni in molte molecole correlate ai grassi quando GRPEL1 o c-Myc venivano ridotti. Importante, la somministrazione esterna di acidi grassi o di una miscela lipidica ha in parte ripristinato la crescita sia nelle linee cellulari tumorali sia negli organoidi di cancro pancreatico derivati da pazienti — mini-tumori coltivati in 3D — suggerendo che il problema principale era la perdita di grassi prodotti de novo.
Trasformare una vulnerabilità in terapia
Complessivamente, il lavoro delinea un quadro chiaro: nel cancro pancreatico, c-Myc induce GRPEL1, che aiuta i mitocondri a funzionare senza intoppi e mantiene i ROS sotto controllo. Questo ambiente mitocondriale stabile permette alle cellule di conservare alti livelli di FASN, producendo nuovi acidi grassi che fungono da mattoni per le membrane, riserve energetiche e segnali di crescita. Quando GRPEL1 viene bloccato, i mitocondri vacillano, i ROS aumentano, FASN diminuisce e le cellule tumorali faticano a proliferare — un effetto che può essere in parte bypassato se i grassi vengono forniti dall’esterno. Per il lettore non specialista, la conclusione è che i tumori pancreatici dipendono da un circuito interno di “fabbrica dei grassi”, guidato da c-Myc, GRPEL1 e FASN. Farmaci che interrompono questa asse di sintesi degli acidi grassi, specialmente nei tumori in cui è molto attiva, potrebbero offrire un nuovo modo promettente per “affamare” le cellule del cancro pancreatico lasciando i tessuti normali meno colpiti.
Citazione: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Parole chiave: cancro pancreatico, metabolismo tumorale, sintesi degli acidi grassi, mitocondri, c-Myc