Clear Sky Science · it
BCL-xL come bersaglio terapeutico nel cancro colorettale refrattario al cetuximab
Perché è importante per le persone con tumore del colon
Il cancro colorettale (colon e retto) è uno dei tumori più comuni al mondo, e molti pazienti con malattia avanzata ricevono un anticorpo mirato chiamato cetuximab. Questo farmaco può inizialmente far regredire i tumori, ma nella maggior parte dei pazienti il cancro trova modi per sfuggire nel giro di mesi, lasciando ai medici poche opzioni efficaci. Questo studio affronta una domanda urgente: quando i tumori del colon smettono di rispondere al cetuximab, esiste un altro punto debole che nuovi farmaci possano sfruttare per indurre la morte delle cellule tumorali?
Quando un farmaco mirato smette di funzionare
Il cetuximab agisce bloccando un’antenna di superficie sulle cellule tumorali chiamata recettore del fattore di crescita epidermico (EGFR), che guida la loro crescita. Il gruppo ha creato un modello di laboratorio di resistenza esponendo una linea cellulare colorettale sensibile (LIM1215) a dosi progressivamente crescenti di cetuximab per sei mesi. Sono emerse due popolazioni cellulari resistenti ottenute indipendentemente che continuavano a crescere anche in presenza di alte concentrazioni del farmaco, ma apparivano ugualmente vitali e proliferative come le cellule originali quando il farmaco veniva rimosso. È importante che le cellule resistenti conservassero ancora l’obiettivo del farmaco sulla loro superficie e che il cetuximab potesse ancora legarsi ad esso, suggerendo che il cancro non avesse semplicemente “nascosto” o alterato il recettore.
Le cellule resistenti riallacciano i segnali di crescita
Per comprendere come le cellule eludessero il cetuximab, i ricercatori hanno esaminato le vie chiave di crescita intracellulari. Nelle cellule parentali, il cetuximab normalmente attenuava la via MAPK, un motore principale della divisione cellulare. Nelle cellule resistenti, l’attività MAPK rimaneva elevata anche quando l’EGFR era bloccato, dimostrando che il segnale di crescita si era disaccoppiato dal recettore originale. Il sequenziamento dell’RNA cellulare ha rivelato nuove mutazioni attivanti in un altro gene RAS, HRAS, in sottopopolazioni delle cellule resistenti, ma non in altri soliti sospetti come KRAS, NRAS o BRAF. I tentativi di porre fine a questa segnalazione di bypass con un inibitore di MEK (che agisce a valle di RAS) hanno ridotto la crescita solo modestamente. Ciò ha sottolineato che, piuttosto che inseguire ogni nuova mutazione, potrebbe essere più efficace attaccare la macchina cellulare della vita-o-morte condivisa tra i diversi cloni resistenti. 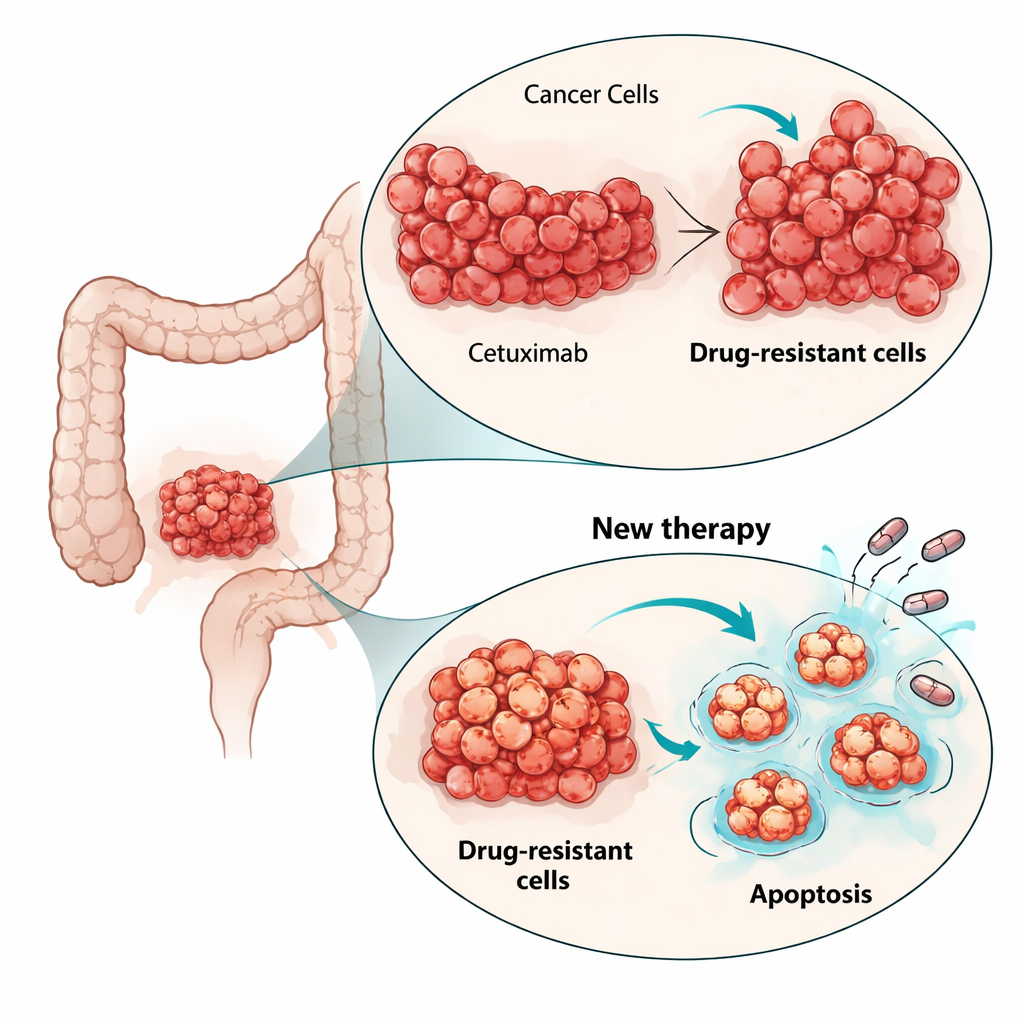
Colpire il sistema di supporto vitale del cancro
I ricercatori hanno concentrato la loro attenzione sull’apoptosi, il programma interno di suicidio cellulare che i tumori spesso sopprimono. L’analisi dell’espressione genica ha mostrato che le vie correlate all’apoptosi erano alterate nelle cellule resistenti. In particolare, la proteina anti-morte BCL-xL risultava più alta in una popolazione resistente e moderatamente aumentata nell’altra, mentre un’altra proteina di sopravvivenza, MCL-1, era anch’essa presente. Il gruppo ha testato piccole molecole chiamate BH3 mimetici, progettate per bloccare queste proteine di sopravvivenza e liberare il macchinario della morte. Nei saggi in colture bidimensionali, tutte e tre le linee cellulari—parentale e resistenti—erano sensibili ai farmaci che bloccano BCL-xL o MCL-1, ma, in modo sorprendente, dosi più basse uccidevano più efficacemente le cellule resistenti al cetuximab. L’aggiunta di una bassa dose dell’inibitore del proteasoma bortezomib, che favorisce l’accumulo di segnali pro-morte, potenziava ulteriormente l’effetto letale, soprattutto in combinazione con l’inibitore di MCL-1.
Dalle piastre piatte ai mini-tumori 3D e ai tessuti dei pazienti
Poiché gli strati cellulari piatti non possono imitare completamente i tumori nell’organismo, il gruppo ha coltivato le cellule come sferoidi tridimensionali incorporati in un gel, riflettendo meglio l’architettura e le sfide di penetrazione dei farmaci nei tumori reali. Anche in questo caso, bloccare BCL-xL o MCL-1 riduceva la vitalità degli sferoidi, e la combinazione di questi farmaci con bortezomib determinava cali drammatici dell’attività metabolica e chiari segni di morte cellulare. Per verificare se questa vulnerabilità esistesse in materiale tumorale umano più realistico, hanno utilizzato fette sottili di tumori colorettali resistenti al cetuximab cresciuti nei topi a partire da tumori di pazienti (xenotrapianti derivati da pazienti). Questi modelli erano tutti KRAS wild-type come le cellule LIM1215 originali, ma presentavano ulteriori mutazioni varie, inclusi BRAF e TP53, rispecchiando la varietà genetica osservata in clinica. 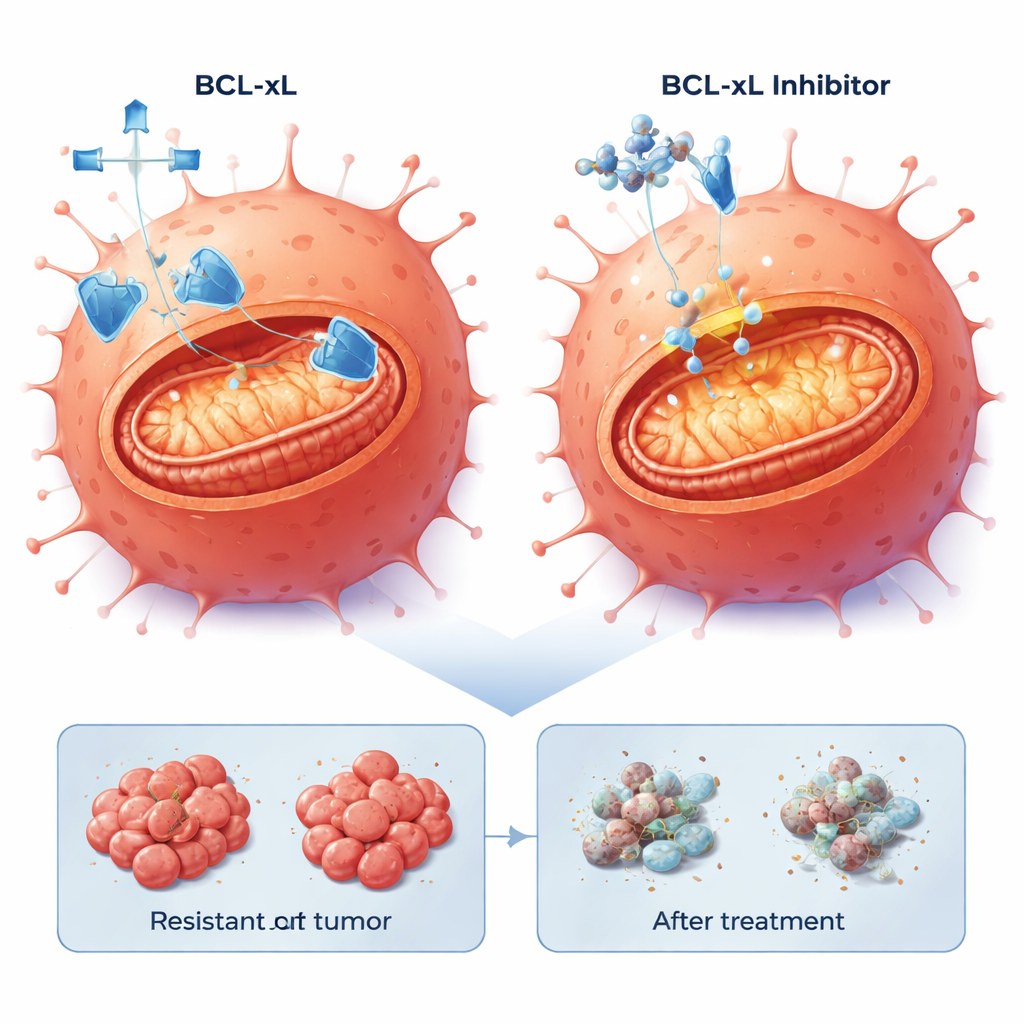
Mirare a BCL-xL funziona su tumori resistenti diversi
In queste fette tumorali derivate da pazienti, la combinazione di un inibitore di BCL-xL con bassa dose di bortezomib ha costantemente scatenato una robusta morte cellulare nel 20–40% delle cellule tumorali in quattro modelli diversi, inclusi quelli con mutazioni BRAF aggressive. Al contrario, il blocco di MCL-1 con bortezomib ha prodotto effetti forti solo in un sottogruppo di tumori. È importante notare che la capacità delle cellule resistenti di andare incontro ad apoptosi era preservata: una volta rimosso la rete di sicurezza rappresentata da BCL-xL, il programma interno di morte poteva ancora essere attivato, indipendentemente dalla specifica via genetica che il tumore aveva seguito per sfuggire al cetuximab.
Cosa significa per i pazienti
Per le persone il cui cancro colorettale smette di rispondere al cetuximab, questo studio offre un cauto ottimismo. Suggerisce che anche dopo che i tumori diventano resistenti alla terapia mirata contro l’EGFR, molte cellule tumorali restano pronte a morire se una proteina chiave di sopravvivenza, BCL-xL, viene bloccata. Sebbene gli inibitori di BCL-xL possano avere effetti collaterali, in particolare sulle piastrine del sangue, il lavoro indica strategie di combinazione e ottimizzazione delle dosi che potrebbero limitare la tossicità sfruttando al contempo un tallone d’Achille condiviso dei tumori difficili da trattare. In futuro, i farmaci che disinnescano BCL-xL potrebbero costituire la spina dorsale di nuovi trattamenti di seconda linea per il cancro colorettale refrattario al cetuximab, meno dipendenti dal paesaggio mutazionale in continuo cambiamento del tumore.
Citazione: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Parole chiave: cancro colorettale, resistenza ai farmaci, cetuximab, inibizione di BCL-xL, apoptosi